铁死亡之父最新Cell论文:这种稀有脂肪酸是铁死亡关键驱动因素
来源:生物世界 2024-03-05 11:15
这些发现揭示了PC-PUFA2在控制线粒体稳态和不同情况下的铁死亡中的关键作用,并解释了游离脂肪酸对铁死亡的调控机制。PC-PUFA2可能作为调控铁死亡的诊断和治疗靶点。
多细胞生物在发育过程中,存在着多种预定的、受到精确控制的细胞程序性死亡,例如细胞凋亡(Apoptosis)、程序性坏死(Necroptosis)、细胞焦亡(Pyroptosis),以及铁死亡(Ferroptosis)等。
铁死亡是2012年由哥伦比亚大学 Brent Stockwell 实验室发现的一种铁依赖性的新型细胞程序性死亡方式,由过度堆积的过氧化脂质(peroxidized lipids)诱导发生,其形态特征,作用方式以及分子机制与其他程序性死亡方式截然不同。同时,细胞中也有多个对抗铁死亡的防御途径,其中最主要的一个是由谷胱甘肽过氧化物酶4(GPX4)所介导的,通过谷胱甘肽(GSH)特异性催化过氧化脂质来抑制铁死亡的发生。
2024年2月15日,哥伦比亚大学 Brent Stockwell 教授团队在 Cell 期刊发表了题为:Phospholipids with two polyunsaturated fatty acyl tails promote ferroptosis 的研究论文。
该研究发现了一种罕见脂肪酸——PC-PUFA2,是铁死亡的关键驱动因素。揭示了PC-PUFA2在控制线粒体稳态和不同情况下的铁死亡中的关键作用,解释了游离脂肪酸对铁死亡的调控机制。并进一步指出PC-PUFA2可能作为调控铁死亡的诊断和治疗靶点。
这项研究提供了细胞铁死亡过程中的新细节,进而提高了我们对铁死亡相关疾病的理解,例如可帮助阻止神经退行性疾病中的细胞铁死亡,以及帮助诱导癌细胞铁死亡。

含单个多不饱和脂肪酸酰基尾部的磷脂(PL-PUFA1)被认为是铁死亡(Ferroptosis)背后的驱动力,而含两个多不饱和脂肪酸酰基尾部的磷脂(PL-PUFA2)则鲜有研究。膳食脂肪酸可调节铁死亡,但脂质代谢和铁死亡敏感性调控机制尚不清楚。
在这项研究中,研究团队发现,脂肪酸或磷脂处理后,含两个多不饱和脂肪酸酰基尾部的磷脂酰胆碱(PC-PUFA2)显著积累,这与癌细胞对铁死亡的敏感性相关。衰老和亨廷顿症的脑组织中存在PC-PUFA2的缺失,与铁死亡有关。值得注意的是,PC-PUFA2与线粒体电子传递链相互作用,产生活性氧(ROS),引发脂质过氧化。线粒体靶向抗氧化剂保护细胞免受PC-PUFA2诱导的线粒体活性氧(mtROS)、脂质过氧化和细胞死亡。
核心发现:
-
膳食PC-PUFA2诱导多种癌细胞株发生铁死亡;
-
膳食PUFA选择性增加细胞内PC-PUFA2的积累;
-
PL-PUFA2与线粒体电子传递链复合物I相互作用;
-
PC-PUFA2诱导线粒体ROS产生,对铁死亡至关重要。
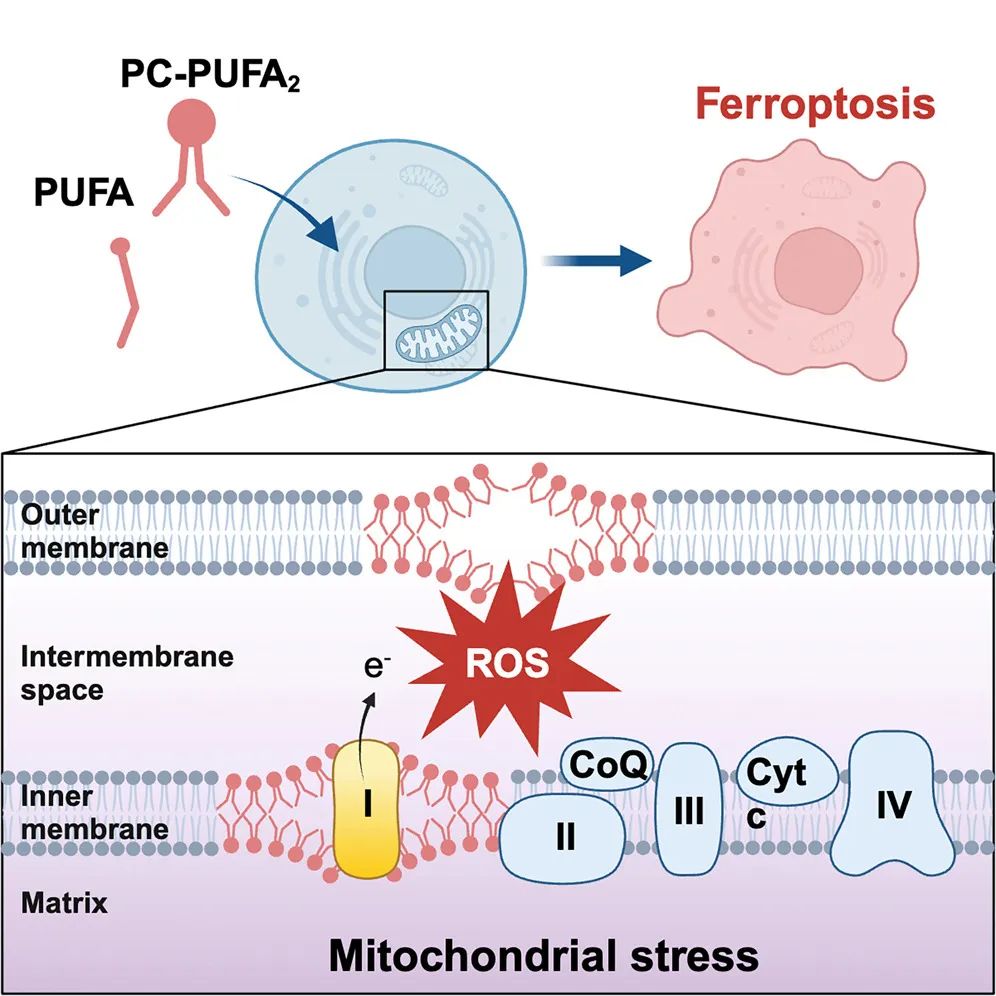
这些发现揭示了PC-PUFA2在控制线粒体稳态和不同情况下的铁死亡中的关键作用,并解释了游离脂肪酸对铁死亡的调控机制。PC-PUFA2可能作为调控铁死亡的诊断和治疗靶点。

PC-PUFA2在细胞死亡时会穿透细胞外脂质层,该研究发现,它是铁死亡的关键驱动因素
Brent Stockwell 教授表示,发现这些二聚体脂肪酸(PC-PUFA2)是铁死亡的重要驱动因素,加深了我们对这种细胞死亡形式的理解,以及这些脂质在控制细胞稳态中的作用。利用这些脂质可能最终帮助我们识别铁死亡发生的位置,并有意地操纵它们来诱导细胞死亡或阻止细胞死亡。从而帮助我们开始理解和拥有控制细胞死亡的能力。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


