Nature子刊:转化生长因子-β和NUR77在结肠肿瘤发生中的相互作用
来源:生物谷 2021-05-27 15:05
2021年5月26日讯/生物谷/BIOON/---厦门大学研究者在NATURE COMMUNICATIONS杂志上发表了题为"Interplay between transforming growth factor-β and Nur77 in dual regulations of inhibitor of differentiation 1 for co
2021年5月26日讯/生物谷/BIOON/---厦门大学研究者在NATURE COMMUNICATIONS杂志上发表了题为"Interplay between transforming growth factor-β and Nur77 in dual regulations of inhibitor of differentiation 1 for colonic tumorigenesis"的研究性文章。转化生长因子-β(转化生长因子-β)信号转导和核受体Nur77在结肠癌发生中的矛盾作用已为人所知,但其内在机制尚不清楚。分化抑制因子1(Id1)是转化生长因子β的靶基因,是结肠癌进展的关键促进剂。因此,该研究确定了NUR77和转化生长因子β信号在调节ID1表达中的整合二重性,并对转化生长因子β和NUR77在结肠癌进展中的矛盾作用提供了机械性的见解。
图片来源:https://doi.org/10.1038/s41467-021-23048-5
结肠癌的发生发展过程依次受不同信号通路的调控,其中转化生长因子-β(TGF-β)信号通路在结肠癌发生发展的不同阶段发挥着独特的作用,发挥着相反的作用。在早期癌症中,转化生长因子β发挥肿瘤抑制作用,包括细胞周期阻滞和诱导凋亡。然而,它促进肿瘤的发生,包括晚期癌症的转移和化疗耐药。在典型的转化生长因子β信号转导中,转化生长因子β与质膜上的转化生长因子βⅡ型受体(TβRII)结合,然后募集并激活I型受体(TβRI)。激活的TβRI磷酸化细胞质中的smad2和smad3,导致它们与smad4结合形成一个复合体,该复合体移位到细胞核内并结合同源dna元件来调节基因转录。
尽管转化生长因子β在晚期促进癌症进展,但很大一部分高级别结肠癌缺乏规范的转化生长因子β信号,这主要是由于受体或smad4的突变所致。转化生长因子β在smad4缺陷性癌症中的促肿瘤作用尚不完全清楚,但smad4的缺失可能使癌细胞逃脱转化生长因子β介导的生长抑制和免疫监视。上述功能丧失机制反映了转化生长因子β信号在促癌过程中的被动作用模式。转化生长因子β是否能有效促进Smad4缺陷结肠癌的进展尚不清楚。
分化抑制因子1(Id1)的异常高表达促进了包括结肠癌在内的多种肿瘤的生长、自我更新和转移。Id1主要通过结合螺旋-环-螺旋转录因子来阻止其诱导分化基因。在癌细胞中,转化生长因子β/smad3信号上调id1转录。Smad特异性E3泛素蛋白连接酶2(SMurf2)催化Smad3多重单泛素化抑制其转录激活能力。有趣的是,SMurf2还介导ID1的多泛素化和降解。然而,目前还不清楚S-2的这些不同功能是如何调控的。
Nur77是核受体超家族的孤儿成员,在多种细胞内外刺激下的生长、存活、分化和凋亡等生物学过程中发挥重要作用。除转录调控外,Nur77还具有非基因组活性,如定位于线粒体,调节细胞凋亡和有丝分裂。据报道,Nur77在结肠癌中既有抑制肿瘤的作用,也有促进肿瘤的作用。它被认为是转化生长因子β信号的正调节因子,与乳腺癌的进展有关。Nur77是否调节转化生长因子β/ID1轴,以及为什么Nur77在结肠癌的发生发展中扮演相反的角色仍不清楚。
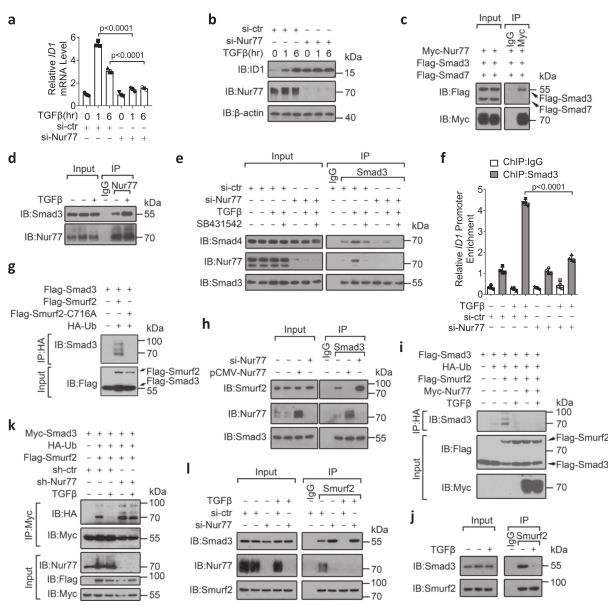
Nur77通过抑制S-MURF-2介导的Smad3单泛素化上调转化生长因子β诱导的Id1表达
图片来源:https://doi.org/10.1038/s41467-021-23048-5
Nur77在ID1调控中的基因组和非基因组综合作用表明,Nur77是ID1表达的关键调控因子,也是下调ID1表达的潜在药物靶点。重要的是,Nur77的功能受到其小分子配体的严格调控。未来的研究将评估Nur77配体下调ID1表达的潜力,从而为结肠癌的治疗提供临床意义。总之,从作者的研究中发现的机制原理强调了Nur77和转化生长因子β信号在调节ID1表达中紧密结合的双重性,以及它在结肠癌发生和治疗中的意义。(生物谷Bioon.com)
参考资料
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->



