ACS Nano:清华大学蒯锐团队制备“洋葱式”多层脂质体,提高STING激动剂的抗肿瘤免疫应答
来源:生物世界 2024-11-11 10:14
该研究报道了一种利用透明质酸和脂质分子层物理交联形成多层脂质体的方法,克服了传统纳米粒在系统给药时难以兼顾稳定性和细胞质递送效率的不足。
近日,清华大学药学院蒯锐课题组(俞锦超博士为第一作者)在 ACS Nano 期刊发表了题为:Single-Dose Physically Cross-Linked Hyaluronic Acid and Lipid Hybrid Nanoparticles Containing Cyclic Guanosine Monophosphate−Adenosine Monophosphate Eliminate Established Tumors 的研究论文。
该研究报道了一种基于透明质酸和脂质分子物理交联获得的“洋葱式”多层脂质体,阐明了纳米结构调控对小分子STING激动剂的释放和递送行为的影响,并基于此平台建立了一种能够高效激活抗肿瘤免疫应答的方法。

受到洋葱多层结构的启发,将具有高效细胞质递送但稳定性差的脂质制备成多层结构有望在保留细胞质递送优势的前提下兼顾稳定性。然而,目前适用于系统给药的小分子缓释多层脂质体(粒径100纳米或以下)依然非常缺乏。此外,传统的维持多层脂质结构的方法多为化学交联的形式,而化学交联剂的使用容易引发安全风险,同时也极大增加了工艺的复杂性。
基于以上背景,蒯锐课题组开发了一种基于透明质酸(HA)和脂质分子物理交联制备的多层脂质体,用于高效递送STING激动剂cGAMP,该制剂被命名为HLHC(HA-lipid hybrid nanoparticles encapsulating cGAMP)。使用微流控装置将HA、脂质分子、cGAMP按特定比例混合后可连续大量制备具有多层结构的脂质体HLHC。电镜下HLHC呈现出典型的“洋葱式”断面结构。
体外研究表明相比于含有cGAMP的普通脂质体对照组LC(Liposomal cGAMP),HLHC具有更好的稳定性和缓释特性,能将更多的小分子递送到细胞质中激活STING通路,进而显著增强细胞分泌I型干扰素的能力。体内研究表明HLHC的多层结构可以显著延长cGAMP的循环时间,增加其在肿瘤部位的蓄积,更好激活瘤内APCs的STING通路。
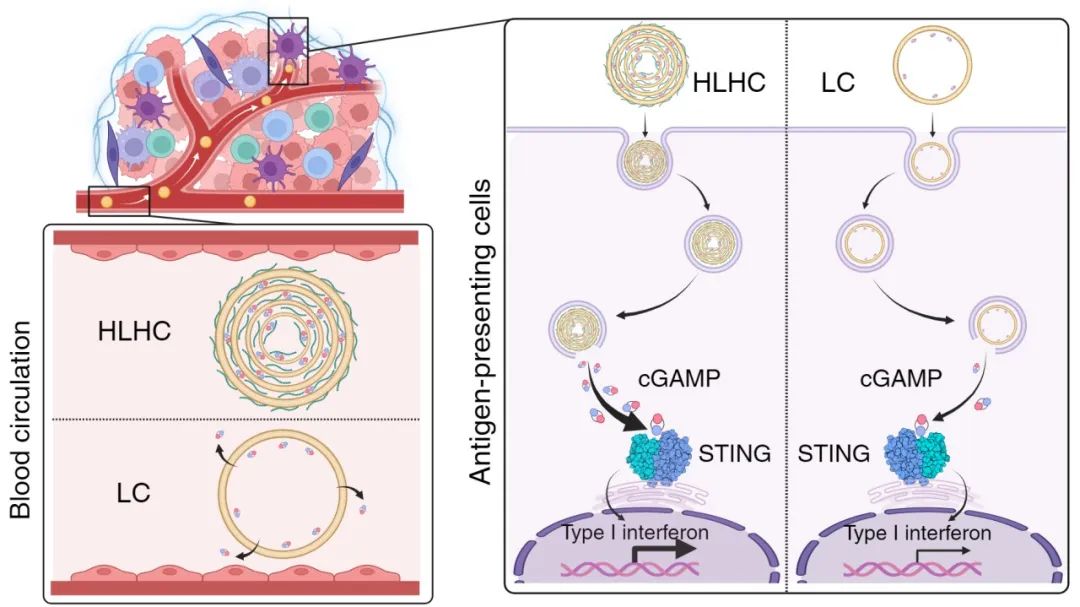
普通脂质体(LC)和物理交联的多层脂质体(HLHC)的作用过程示意图
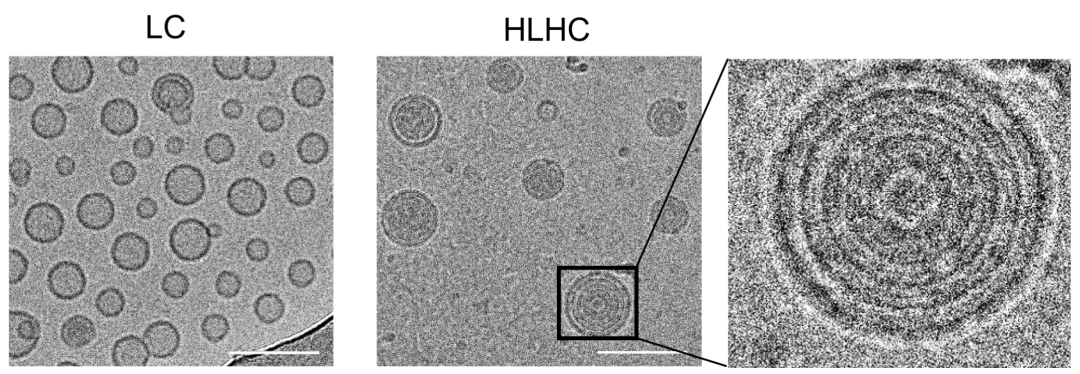
普通脂质体(LC)和物理交联的多层脂质体(HLHC)的电镜结构(比例尺为100纳米)
单次静脉注射HLHC即可在小鼠体内引发强大的抗肿瘤免疫应答并消退皮下MC38肿瘤,与检查点抑制剂联合后能消退B16F10黑色素瘤。此外,经过治疗的小鼠可建立长期的免疫记忆并免于肿瘤复发。
总的来说,该研究报道了一种利用透明质酸和脂质分子层物理交联形成多层脂质体的方法,克服了传统纳米粒在系统给药时难以兼顾稳定性和细胞质递送效率的不足。单次静脉注射HLHC即可产生强大的抗肿瘤免疫反应,消退肿瘤并建立持久的免疫记忆。此外,该制剂具有简单易于制备的特点,有望用于其他小分子的高效递送。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


