Cell Rep:科学家揭示胰腺癌扩散的新型分子机制
来源:生物谷原创 2023-12-28 13:26
来自梅奥诊所等机构的科学家们通过对胰腺癌进一步研究揭示了其发生转移背后的分子机制,研究人员识别出了一种特殊的细胞信号蛋白,其能驱动胰腺癌细胞的生长,这或许有望作为一种潜在的治疗性靶点。
癌症如何扩散或发生转移对于癌症研究人员和患者而言一直是一个大问题,近日,一篇发表在国际杂志Cell Reports上题为“Ectopic expression of DOCK8 regulates lysosome-mediated pancreatic tumor cell invasion”的研究报告中,来自梅奥诊所等机构的科学家们通过对胰腺癌进一步研究揭示了其发生转移背后的分子机制,研究人员识别出了一种特殊的细胞信号蛋白,其能驱动胰腺癌细胞的生长,这或许有望作为一种潜在的治疗性靶点。
研究者Gina Razidlo说道,我们的最终目标是找到引发转移的诱因并及时对其进行阻断,同时结合减少肿瘤生长的疗法,我们就有望改善患者的治疗结果。肿瘤往往会生长在营养匮乏的环境中,因此癌细胞就必须重新修饰其细胞代谢从而来满足其能量需求。癌细胞劫持代谢通路的其中一种方式就是通过溶酶体(lysosomes),其就好像细胞的胃部一样发挥功能,其中充满了消化酶,溶酶体能分解促进细胞生长的蛋白质、脂质和营养物质,此前有研究表明,溶酶体活性的扩增或许就是多种癌症发生的标志。
这一认识或许就促使研究者Razidlo等人开始密切关注因癌基因KRAS突变所驱动的胰腺癌细胞中的溶酶体的特征,文章中,研究人员比较了表达癌基因KRAS的胰腺癌细胞所表达的溶酶体与携带健康KRAS的细胞所表达的溶酶体的差异,旨在阐明其二者之间的差异,在研究人员发现的胰腺癌细胞溶酶体表面发生改变的52种蛋白中,有一种名为胞质分裂贡献体8(DOCK8,dedicator of cytokinesis 8)的蛋白质表现非常突出。
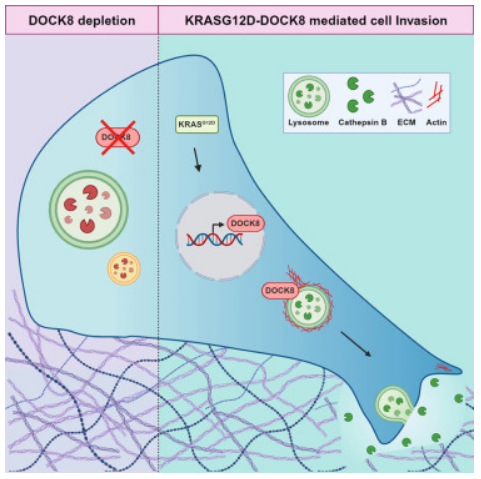
科学家揭示胰腺癌扩散的新型分子机制。
图片来源:Cell Reports (2023). DOI:10.1016/j.celrep.2023.113042
DOCK8能产生入侵的突起,就好像小手臂一样能穿过细胞并改变细胞的结构,同时还能降解其周围的环境,DOCK8通常存在于健康的免疫细胞中,其能帮助细胞导航并挤压致密组织,促进细胞对感染产生反应并抵御感染,让研究人员意外的是,他们发现,DOCK8竟然也存在于胰腺癌细胞的溶酶体上。那么癌细胞的入侵和扩散如何类似于DOCK8帮助免疫细胞浸润到组织中,研究人员进一步研究观察了胰腺癌细胞的图像和视频,结果发现,DOCK8能利用溶酶体来分解癌细胞周围的细胞外环境,并帮助其扩散。
为了证实这种蛋白能参与到肿瘤进展过程中,研究人员利用基因编辑工具CRISPR消除了胰腺癌细胞中的DOCK8,结果在临床前模型中发现,剔除了DOCK8的溶酶体移动地较慢,肿瘤生长和转移也会发生减缓,随后他们进一步研究发现,DOCK8存在于大约20%的胰腺癌患者机体的细胞中。如今研究人员发现,DOCK8能调节胰腺癌细胞的转移过程,其或能作为一种潜在的治疗性靶点来帮助预防或停止胰腺癌的转移。
综上,本文研究结果表明,DOCK8的异位表达或许能作为胰腺癌细胞中KRAS驱动的溶酶体调节和侵袭的关键驱动因素。(生物谷Bioon.com)
原始出处:
Omar L. Gutierrez-Ruiz,Katherine M. Johnson,Eugene W. Krueger, et al. Ectopic expression of DOCK8 regulates lysosome-mediated pancreatic tumor cell invasion, Cell Reports (2023). DOI:10.1016/j.celrep.2023.113042
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


