我国科学家成功研发出新型纳米光敏剂,用于肿瘤的光动力治疗
来源:科技部 2019-12-10 13:01
肿瘤的光动力治疗是光敏剂在肿瘤组织选择性吸收和滞留,在利用特定波长的光激发后,产生活性氧自由基(ROS),达到杀伤肿瘤细胞的目的。与传统放化疗治疗肿瘤的方式相比,光动力治疗具有选择性高、不易产生耐药性以及副作用小等特点,在肿瘤的治疗中越来越受到关注。目前,临床上常用的光敏剂主要利用可见光进行激发,其组织穿透性弱,限制了光动力治疗在临床应用的范围和
肿瘤的光动力治疗是光敏剂在肿瘤组织选择性吸收和滞留,在利用特定波长的光激发后,产生活性氧自由基(ROS),达到杀伤肿瘤细胞的目的。与传统放化疗治疗肿瘤的方式相比,光动力治疗具有选择性高、不易产生耐药性以及副作用小等特点,在肿瘤的治疗中越来越受到关注。目前,临床上常用的光敏剂主要利用可见光进行激发,其组织穿透性弱,限制了光动力治疗在临床应用的范围和治疗效果。因此,寻找有效光敏剂,能够提高光动力治疗的治疗效果,并大大推动其在临床的的应用。
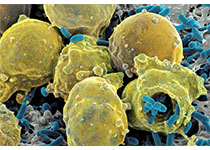
2019年10月31日,中科院遗传与发育生物学研究所和北京大学医学部研究团队在国际学术期刊ACS Nano杂志上在线发表了题为“Super-efficient in Vivo Two-Photon Photodynamic Therapy with a Gold Nanocluster as a Type Ⅰ Photosensitizer”的研究工作。这两个团队长期合作,致力于纳米材料在生物医学应用方面的研究。研究团队采用二氢硫辛酸为配体的金纳米簇(AuNC@DHLA)作为新的光敏剂。AuNC@DHLA具有优异的双光子性质,在激发光源的激发下,可以产生大量超氧负离子O2-,实现基于Ⅰ型机制的光动力治疗(传统的光动力治疗产生的自由基以单线态氧为主,为Ⅱ型机制)。
该研究的实验结果表明,AuNC@DHLA可通过细胞质膜微囊介导的内吞作用进入肿瘤细胞,并富集于溶酶体;在光照条件下产生大量超氧自由基,使溶酶体通透性增加,进而导致线粒体受损及细胞骨架断裂,最终致使肿瘤细胞凋亡和坏死。在荷瘤小鼠模型中的治疗效果也要明显优于临床在用的光敏剂。该研究团队发展的AuNC@DHLA双光子光动力治疗可以利用近红外脉冲光源进行激发,提高了组织的穿透深度,增加光动力治疗的抗肿瘤效果,减少机体的副反应,具有非常重要的临床应用价值。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


