首尔国立大学: 利用病毒和非病毒载体基因治疗血友病B
来源:生物谷原创 2023-06-12 15:33
血友病是一种遗传性疾病,涉及凝血因子缺乏,以及与手术或创伤相关的自发性和过度出血。血友病B是由凝血因子IX(FIX)缺乏引起的,其患病率为每25,000名男婴中有1名。
血友病是一种遗传性疾病,涉及凝血因子缺乏,以及与手术或创伤相关的自发性和过度出血。血友病B是由凝血因子IX(FIX)缺乏引起的,其患病率为每25,000名男婴中有1名。已经开发了各种血友病治疗方法,但在有效性、安全性、治疗简易性和成本方面仍存在未得到满足的需求。

图片来源: https://doi.org/10.1016/j.omtn.2023.03.008.
近日,来自首尔国立大学的研究者们在Molecular Therapy: Nucleic Acids杂志上发表了题为“In vivo genome editing for hemophilia B therapy by the combination of rebalancing and therapeutic gene knockin using a viral and non-viral vector”的文章,该研究揭示了利用病毒和非病毒载体通过再平衡和治疗性基因敲击相结合的体内基因组编辑用于血友病B治疗。
最近血友病的治疗策略包括使用腺相关病毒(AAV)进行长期治疗性基因表达,以及通过下调抗凝途径来重新平衡治疗。然而,这些方法在免疫反应方面存在局限性,或者不足以控制急性出血。因此,研究者开发了一种利用脂质纳米粒(LNP)和AAV进行再平衡和人类因子9(HF9)基因敲击(KI)相结合的治疗血友病B的策略。
抗凝血酶(AT;Serpin家族C成员1[Serpinc1])被选为KI基因的靶向抗凝途径。首先,LNP聚集的规则间隔短回文重复序列(CRISPR)和AAV供体的联合使用导致了Serpinc1中20%的插入或缺失(Indels)和67%的血小鼠AT浓度下降。其次,hF9编码序列被整合到大约3%的靶基因座中。
HF9KI产生约1,000 ng/mL人凝血因子IX(HFIX),并将凝血活性恢复到正常水平。注射LNP-CRISPR导致AT持续下调和hFIX产生长达63周。在肝部分切除的情况下,AT抑制和hFIX蛋白生产能力可以通过基因编辑的肝细胞的增殖来维持。
AAV和LNP联合给药,除随机积分外,未见严重副作用。本研究结果证明了血友病B的治疗是通过使用LNP和AAV的再平衡和hF9KI相结合的方法。
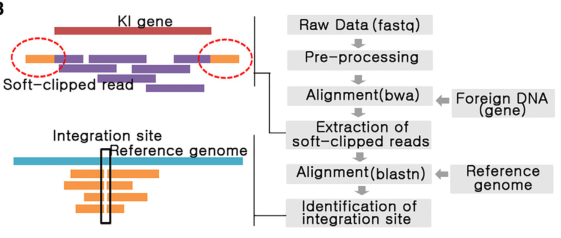
AAV供体与LNP-CRISPR联合体内KI未见严重副作用
图片来源: https://doi.org/10.1016/j.omtn.2023.03.008.
综上所述,本研究证实了AT靶向和hF9KI联合策略可恢复凝血活性。使用AAV和LNP杂交体获得了较高的体内治疗基因Ki,其治疗效果似乎持续了63周。此外,与双AAV策略相比,AAV-LNP组合可能有利于降低AAV剂量,并可作为开发基于基因编辑的蛋白质缺乏相关遗传疾病高级治疗策略的基础。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


