Sci Transl Med:新型策略或能通过靶向作用白血病干细胞来抵御人类急性髓性白血病
来源:生物谷原创 2024-08-04 12:00
本文研究结果强调了NCOA4介导的铁死亡在维持LSC静息和功能方面的重要角色,并表明,靶向作用这一通路或许能作为AML患者有效的治疗性策略。
急性髓性白血病(AML)是成年人发生的一种最常见的血液和骨髓癌症,其是由未成熟细胞的增加所引起的,这些细胞能快速破坏和替代健康的血液细胞(红细胞、白细胞和血小板),AML在60岁以下的患者中有一半是致命的,在60岁以上的患者中由85%是致命的。近日,一篇发表在国际杂志Science Translational Medicine上题为“Targeting ferritinophagy impairs quiescent cancer stem cells in acute myeloid leukemia in vitro and in vivo models”的研究报告中,来自日内瓦大学等机构的科学家们通过研究发现,通过靶向作用自身的干细胞或能帮助抵御人类白血病的发生。
研究者表示,白血病所引起的不良预后或许是由于所谓的休眠或静息白血病干细胞(LSCs,leukemic stem cells)的存在所致,其能躲避化疗,这些细胞通常是看不见的,当在一次明显成功的治疗后,白血病干细胞就会苏醒并重新激活疾病,因此,开发一种能靶向作用这些细胞的新型疗法对于科学家们而言是一大挑战,然而,目前他们也并不太清楚控制这些干细胞背后的分子机制。
通过识别LSCs特有的遗传和代谢特征,研究人员就有望开发抵御AML的新型疗法,相关研究结果也为寻找新型治疗靶点和其临床应用铺平了道路。研究者Jérôme Tamburini博士说道,利用先进的生物信息学技术,我们首先确定了这些静息细胞含有由35个基因所组成的特殊遗传特征,当我们在AML患者的大型临床数据库中利用这一特征时,我们就能证明这种特征与患者疾病预后密切相关。该研究还强调了休眠和活性白血病干细胞之间的代谢差异,一般而言,为了生存,细胞就会诱发化学反应,从而就能促使白血病干细胞分解营养物质并产生能量。
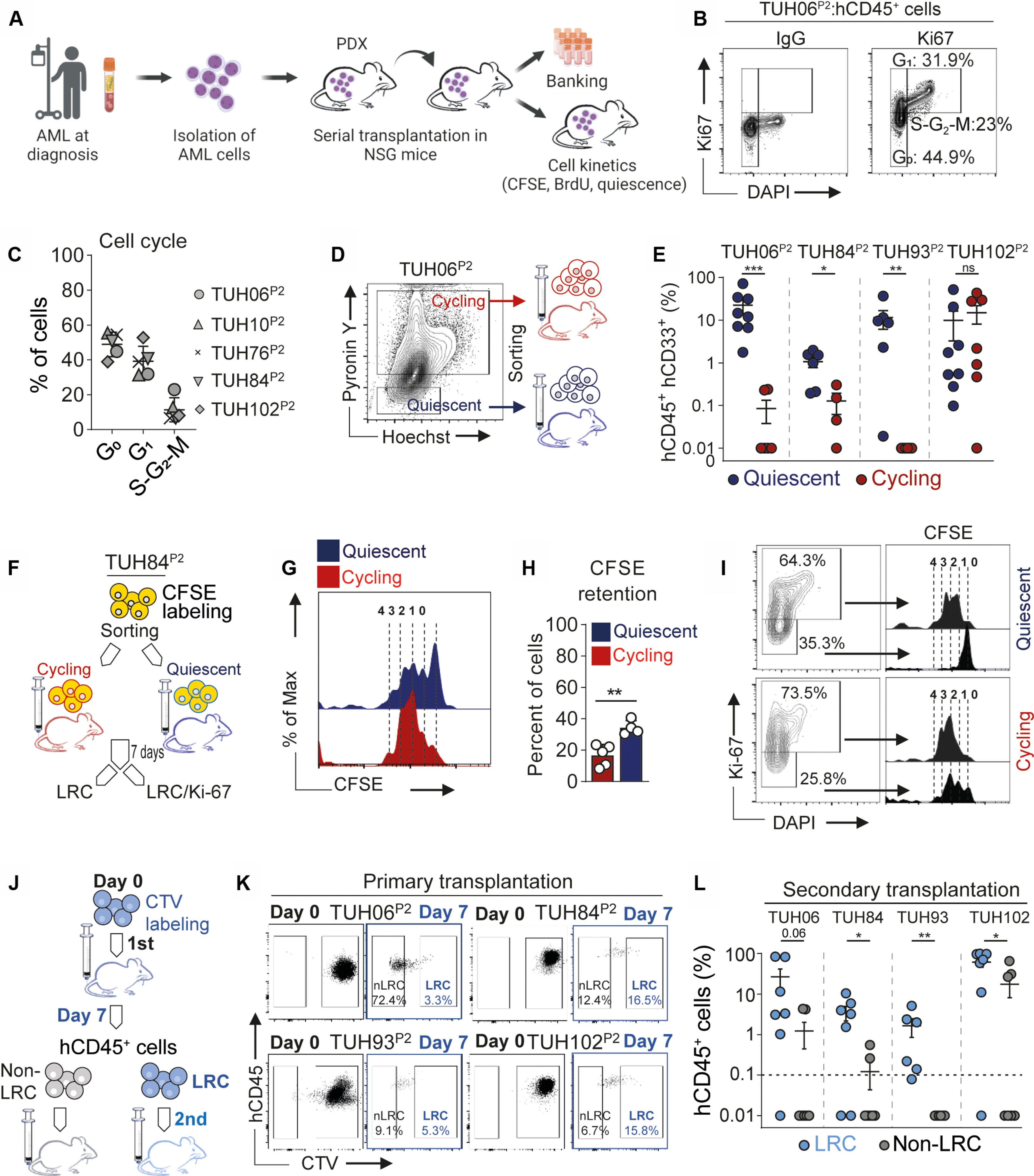
新型策略或能通过靶向作用白血病干细胞来抵御人类急性髓性白血病
图片来源:Science Translational Medicine (2024). DOI:10.1126/scitranslmed.adk1731
当然这或许也涉及自噬的过程,这一过程允许细胞再循环细胞组分从而产生新的细胞,并在缺乏外部营养的情况下提供能量,科学家们发现,休眠的白血病干细胞依赖于铁自噬(ferritinophagy),其是一种能靶向作用铁蛋白(ferritin,主要的铁储存分子)的特殊自噬形式。研究者表示,这一过程是由一种称之为NCOA4的蛋白所介导的,其能控制细胞中铁离子的可用性,通过在遗传上或化学性地抑制,研究人员观察到,白血病细胞,尤其是休眠干细胞更有可能发生死亡,而健康血液干细胞则会保持完整。
利用小鼠模型进行的实验结果证实,阻断NCOA4蛋白就能减少肿瘤生长、白血病干细胞的生存能力和自我更新,因此,通过抑制这一通路来靶向作用铁自噬或许是一种非常有前途的治疗性策略,研究者表示,用于阻断NCOA4的化合物目前正处于未来临床试验的早期开发阶段,下一步研究人员将会深入研究探究铁自噬发生的机制以及其与线粒体自噬之间的关联,这或许就是LSCs调节的一个关键机制。
综上,本文研究结果强调了NCOA4介导的铁死亡在维持LSC静息和功能方面的重要角色,并表明,靶向作用这一通路或许能作为AML患者有效的治疗性策略;同时该研究还强调了抑制NCOA4改善AML患者治疗结局的潜力,并为未来进一步研究和临床研发铺平了道路。(生物谷Bioon.com)
参考文献:
CLEMENT LARRUE,SARAH MOUCHE,PAOLO ANGELINO, et al. Targeting ferritinophagy impairs quiescent cancer stem cells in acute myeloid leukemia in vitro and in vivo models, Science Translational Medicine (2024). DOI: 10.1126/scitranslmed.adk1731
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


