Nat Commun:揭示蛋白AKAP8抑制乳腺癌转移机制
来源:本站原创 2020-01-29 20:47
2020年1月29日讯/生物谷BIOON/---在一项新的研究中,来自美国贝勒医学院的研究人员在人类肿瘤的动物模型中发现一种在体内天然产生的称为AKAP8的蛋白抑制乳腺癌转移。
2020年1月29日讯/生物谷BIOON/---在一项新的研究中,来自美国贝勒医学院的研究人员在人类肿瘤的动物模型中发现一种在体内天然产生的称为AKAP8的蛋白抑制乳腺癌转移。他们还发现高水平的AKAP8可预示乳腺癌患者的存活率更高。这些发现表明AKAP8通过干扰促进癌细胞转移的蛋白产生来抑制乳腺癌转移,这有助于人们在未来开发出治疗转移性癌症的新策略。相关研究结果于2020年1月24日发表在Nature Communications期刊上,论文标题为“The RNA-binding protein AKAP8 suppresses tumor metastasis by antagonizing EMT-associated alternative splicing”。
论文通讯作者、贝勒医学院的Chonghui Cheng博士说,“我们的实验室研究了调节乳腺癌转移的细胞机制。在之前的研究中,我们提供了首个证据表明作为一种让细胞能够在一种蛋白的不同形式之间进行切换的细胞过程,选择性剪接(alternative splicing)能够在功能上控制肿瘤转移。”
选择性剪接是一种自然的细胞过程,可以帮助细胞执行多种功能,比如伤口愈合和胚胎发育。通过选择性剪接,细胞可以利用有限数量的基因产生大量的蛋白。在人类中,大约95%的基因是通过选择性剪接进行加工的。近期,人们已发现这个过程也与癌症有关。
在之前的一项将选择性剪接引入癌症研究领域的创新性研究中,Cheng及其同事们已发现在通过选择性剪接产生的两种不同形式的CD44蛋白--- CD44s和CD44v---中,仅CD44s促进癌细胞存活。这些发现也已在有关乳腺癌和其他类型的癌症的其他报道中得到证实。
在当前的这项新的研究中,这些研究人员通过寻找调节与癌症转移相关的选择性剪接事件的蛋白,进一步研究了选择性剪接如何促进癌症转移。
AKAP8帮助细胞处于非转移状态
Cheng和她的同事们对细胞进行了筛选,寻找作为选择性剪接调节因子发挥作用从而阻止细胞转移的蛋白。他们鉴定出一组可能对肿瘤转移调控至关重要的蛋白,并着重关注AKAP8。
Cheng说,“我们在人类患者癌细胞的转移性乳腺癌小鼠模型中研究了AKAP8。我们发现剔除人类患者癌细胞中的AKAP8蛋白促进这些小鼠模型中的乳腺癌转移。此外,给它们提供外源性的AKAP8可抑制乳腺癌转移。”
综上所述,这些结果支持AKAP8是一种与肿瘤转移相关的选择性剪接事件的重要调节因子。它不仅能够预测患者的转移性乳腺癌治疗结果,而且还能够在动物模型中抑制转移性乳腺癌进展。
Cheng和她的同事们继续进行调查,以确定AKAP8如何介导它的转移抑制作用。他们发现,除了调节CD44的选择性剪接之外,AKAP8还调节另一种称为CLSTN1的蛋白的选择性剪接。在这种情况下,针对CLSTN1蛋白的两种形式---CLSTN1S和CLSTN1L---而言,AKAP8促进CLSTN1S的产生。CLSTN1S与阻止细胞进展为转移状态有关。这CLSTN1的一种之前未知的功能。
Cheng说,“我们认为,选择性剪接调节因子参与了诸如CD44和CLSTN1之类的许多不同细胞蛋白的微妙平衡过程。两类调节因子在保持这种平衡中发挥着作用。一种类型的调节因子,比如AKAP8,对选择性剪接进行调节,以产生有助于细胞保持正常状态的蛋白。另一种类型的调节因子让这种平衡过程偏向产生促进转移性转化的蛋白。如果这种平衡受到破坏,那么就可以促进肿瘤进展。通过研究这种平衡如何得到维持和破坏这种平衡的因子,我们希望了解肿瘤转移的新调控层面,并获得可能导致开发转移性癌症治疗方法的新见解。”(生物谷 Bioon.com)
参考资料:
1.Xiaohui Hu et al. The RNA-binding protein AKAP8 suppresses tumor metastasis by antagonizing EMT-associated alternative splicing. Nature Communications, 2020, doi: 10.1038/s41467-020-14304-1.
2.Protein AKAP8 suppresses breast cancer metastasis
https://medicalxpress.com/news/2020-01-protein-akap8-suppresses-breast-cancer.html

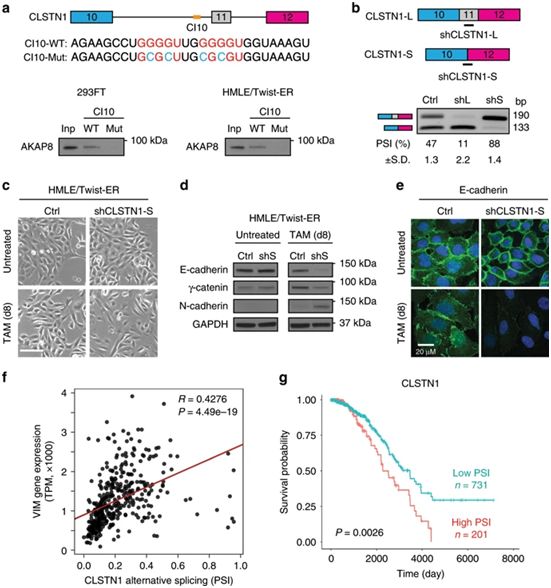
图片来自Nature Communications, 2020, doi: 10.1038/s41467-020-14304-1。
论文通讯作者、贝勒医学院的Chonghui Cheng博士说,“我们的实验室研究了调节乳腺癌转移的细胞机制。在之前的研究中,我们提供了首个证据表明作为一种让细胞能够在一种蛋白的不同形式之间进行切换的细胞过程,选择性剪接(alternative splicing)能够在功能上控制肿瘤转移。”
选择性剪接是一种自然的细胞过程,可以帮助细胞执行多种功能,比如伤口愈合和胚胎发育。通过选择性剪接,细胞可以利用有限数量的基因产生大量的蛋白。在人类中,大约95%的基因是通过选择性剪接进行加工的。近期,人们已发现这个过程也与癌症有关。
在之前的一项将选择性剪接引入癌症研究领域的创新性研究中,Cheng及其同事们已发现在通过选择性剪接产生的两种不同形式的CD44蛋白--- CD44s和CD44v---中,仅CD44s促进癌细胞存活。这些发现也已在有关乳腺癌和其他类型的癌症的其他报道中得到证实。
在当前的这项新的研究中,这些研究人员通过寻找调节与癌症转移相关的选择性剪接事件的蛋白,进一步研究了选择性剪接如何促进癌症转移。
AKAP8帮助细胞处于非转移状态
Cheng和她的同事们对细胞进行了筛选,寻找作为选择性剪接调节因子发挥作用从而阻止细胞转移的蛋白。他们鉴定出一组可能对肿瘤转移调控至关重要的蛋白,并着重关注AKAP8。
Cheng说,“我们在人类患者癌细胞的转移性乳腺癌小鼠模型中研究了AKAP8。我们发现剔除人类患者癌细胞中的AKAP8蛋白促进这些小鼠模型中的乳腺癌转移。此外,给它们提供外源性的AKAP8可抑制乳腺癌转移。”
综上所述,这些结果支持AKAP8是一种与肿瘤转移相关的选择性剪接事件的重要调节因子。它不仅能够预测患者的转移性乳腺癌治疗结果,而且还能够在动物模型中抑制转移性乳腺癌进展。
Cheng和她的同事们继续进行调查,以确定AKAP8如何介导它的转移抑制作用。他们发现,除了调节CD44的选择性剪接之外,AKAP8还调节另一种称为CLSTN1的蛋白的选择性剪接。在这种情况下,针对CLSTN1蛋白的两种形式---CLSTN1S和CLSTN1L---而言,AKAP8促进CLSTN1S的产生。CLSTN1S与阻止细胞进展为转移状态有关。这CLSTN1的一种之前未知的功能。
Cheng说,“我们认为,选择性剪接调节因子参与了诸如CD44和CLSTN1之类的许多不同细胞蛋白的微妙平衡过程。两类调节因子在保持这种平衡中发挥着作用。一种类型的调节因子,比如AKAP8,对选择性剪接进行调节,以产生有助于细胞保持正常状态的蛋白。另一种类型的调节因子让这种平衡过程偏向产生促进转移性转化的蛋白。如果这种平衡受到破坏,那么就可以促进肿瘤进展。通过研究这种平衡如何得到维持和破坏这种平衡的因子,我们希望了解肿瘤转移的新调控层面,并获得可能导致开发转移性癌症治疗方法的新见解。”(生物谷 Bioon.com)
参考资料:
1.Xiaohui Hu et al. The RNA-binding protein AKAP8 suppresses tumor metastasis by antagonizing EMT-associated alternative splicing. Nature Communications, 2020, doi: 10.1038/s41467-020-14304-1.
2.Protein AKAP8 suppresses breast cancer metastasis
https://medicalxpress.com/news/2020-01-protein-akap8-suppresses-breast-cancer.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


