Current Opinion In Immunology:过继细胞疗法的安全开关
来源:生物谷 2021-08-27 17:06
基于过继细胞转移(ACT)的癌症免疫疗法涵盖广泛的方法,包括使用受体修饰和非修饰免疫细胞,它们的共同目标是提供肿瘤反应性免疫细胞区室。
基于过继细胞转移(ACT)的癌症免疫疗法涵盖广泛的方法,包括使用受体修饰和非修饰免疫细胞,它们的共同目标是提供肿瘤反应性免疫细胞区室。与嵌合抗原受体/工程化(CAR/TCR)T细胞疗法相关的主要不良事件包括细胞因子释放综合征(CRS)、神经毒性和靶向肿瘤外毒性,而移植物抗宿主病(GVHD)是供体淋巴细胞输注(DLI)的主要限制因素,这些毒性的一部分可以通过调节免疫活性的干预措施来减少,而对输注的细胞产品没有特异性。
图片来源:https://doi.org/10.1016/j.coi.2021.07.002
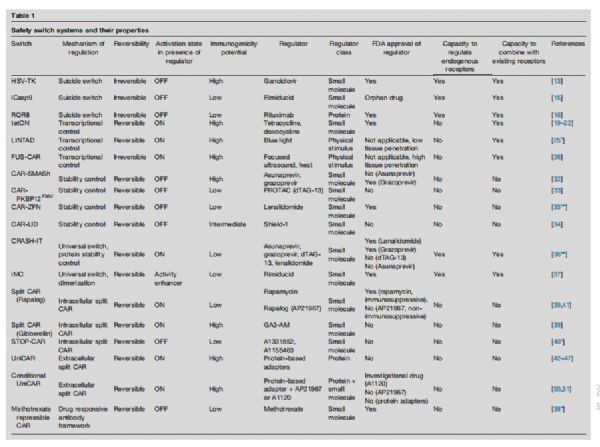
为了在保留宿主免疫活性的同时控制注入的细胞产品,已经开发了许多安全开关系统。不可逆地灭活输注的T细胞群的安全开关的早期例子已用于DLI疗法,其中移植物抗宿主病(GVHD)的发生与输注的T细胞数量相关,基于单纯疱疹病毒胸苷激酶(HSV-TK)的自杀开关在DLI治疗GVHD的疗效已在临床研究中得到充分证实。然而,细胞耗竭系统的不可逆性质意味着任何治疗活性在触发开关系统时都会丧失,早期开关系统的这种局限性促使设计新颖的平台以可逆和可滴定的方式控制ACT产品的活性。该研究根据它们采用的调节机制将这些新型开关系统分为五个主要类别,此外,还讨论了它们在潜在免疫原性、临床兼容性、改造现有抗原受体的能力和激活模式方面的优势和劣势。
通过抗原受体的条件表达调节T细胞活性 图片来源:https://doi.org/10.1016/j.coi.2021.07.002
小分子响应性合成转录因子是广泛使用的研究工具,用于控制位于相应合成启动子下游的目标基因(GOI)的表达,合成转录因子与此类启动子的可逆结合既可以通过构象变化(基于四环素、库马酸盐和米非司酮的系统),也可以通过小分子诱导的二聚化(基于蜕皮激素、他克莫司环孢素A[FKCsA]、脱落酸和雷帕霉素的系统)。有研究采用物理刺激的平台,如光和聚焦超声敏感(FUS)系统,用于驱动嵌合抗原受体的表达,在光诱导核易位和二聚化(LINTAD)系统中,蓝光诱导的合成转录因子的二聚化和核转运允许通过定向光控制基因表达,从而控制免疫细胞活性。LINTAD系统使用非人类序列从而产生免疫原性风险,此外,需要反复刺激以维持CAR表达;基于光的系统的一个更基本的限制是光波的组织穿透性较差,即使对于显示最强组织穿透性的红色和近红外光源,光波也仅限于毫米,而通过使用声波可能会实现更有效的组织穿透,FUS波介导的发热已被证明可诱导体内Hsp启动子下的感兴趣基因的转录。
安全开关系统及其特性 图片来源:https://doi.org/10.1016/j.coi.2021.07.002
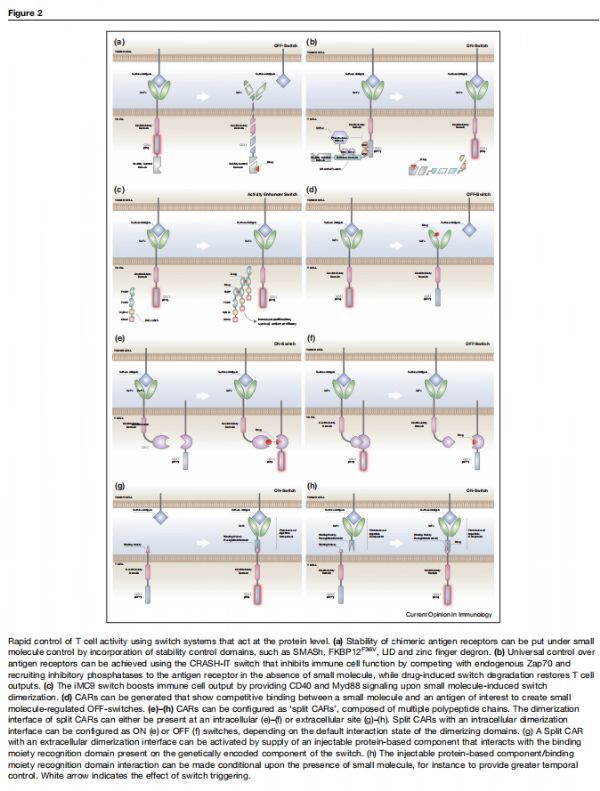
使用在蛋白质水平起作用的开关系统快速控制T细胞活性 图片来源:https://doi.org/10.1016/j.coi.2021.07.002
药物诱导的蛋白质稳定性控制系统起效快,因此被提议作为通过小分子给药控制CAR-T细胞的替代机制。此类中最常用的方法包括将蛋白质稳定性控制元件,如SMASh、FKBP12F36V、LID和基于锌指的degrons,直接融合到抗原受体的细胞内部分,从而创建关闭开关。为了控制T细胞功能,研究者设计了一种化学调节传递的SH2传递抑制尾(CRASH-IT)开关,不需要对抗原受体进行共价修饰,在CRASH-IT设计中,可以区分3个功能组件,共同允许将开关分子递送至抗原受体、抑制激活的抗原受体以及基于小分子的开关蛋白水平控制。通过这种设计,可以使用稳定性控制域来调节T和自然杀伤(NK)细胞的活性,此外,这种开关可以改装为具有经证实的临床活性的抗原受体,并且与不同的含有免疫受体酪氨酸激活基序(ITAM)的受体兼容。作为使用不需要抗原受体修饰的蛋白质水平开关调节免疫细胞活性的替代方法,已经开发出一种小分子诱导的MyD88/CD40二聚化策略(iMC)。在这种控制T细胞活性的策略中,嵌合抗原受体中使用的抗体结构域已被设计为在与小分子相互作用时发生构象变化,从而改变其对目标肿瘤抗原的亲和力。
一些研究小组报道了分离抗原受体设计,旨在实现对 CAR-T细胞功能的可逆控制。根据两条多肽链之间相互作用表面在细胞内或细胞外位点的定位,这些方法可以大致分为两类:具有细胞内二聚化接口的分裂CAR设计可以配置为ON或OFF开关,具体取决于二聚化域的默认交互状态,rapalog (AP21967)、赤霉素和来那度胺分别诱导FRB/FKBP12F36V、GID1/GAI和CRBN-锌指结构域的异二聚化,它们存在于这些开关系统,因此这些系统用作ON开关;“STOP-CAR”分子的两条链中存在的载脂蛋E4/Bcl-XL蛋白结构域之间默认的高亲和力相互作用可以通过提供小分子A1331852和A1155463来取消,从而使这种系统关闭开关。在使用细胞外二聚界面的分裂CAR设计中,肿瘤抗原结合抗体结构域已被一个独特的结合部分所取代,该结合部分可以与系统中基于蛋白质的可注射组件相互作用,已经报道了细胞外分裂CAR策略的一种变化,其中靶向部分和膜结合受体之间的结合依赖于小分子的添加。
一系列具有不同特性的可逆开关平台的设计体现了合成生物学在创建更先进的细胞疗法方面的前景,在未来几年,应该评估这些不同方法在提高过继细胞疗法安全性方面的临床价值。 除了它们在减少治疗相关毒性方面的价值之外,这种可逆的开关系统对于增加基于细胞的疗法的抗肿瘤活性也可能是有价值的。
可逆安全开关领域内的一个未充分研究的领域是它们作为AND或NOT门的潜力,以限制靶向肿瘤外的毒性,超越过继T/NK细胞疗法的领域,提供对细胞活动的时间和/或空间控制的非免疫原性开关系统的设计在基于干细胞的疗法中也应该具有吸引力,并且可能在未来被使用在体内基因修饰时控制定义的细胞区室。(生物谷 bioon)
参考文献
Ali Can Sahillioglu et al. Safety switches for adoptive cell therapy. CURRENT OPINION IN IMMUNOLOGY (2021 Aug 10) doi:https://doi.org/10.1016/j.coi.2021.07.002
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。