Science子刊:利用TCR-T细胞靶向COL6A3蛋白的一种泛癌表位有望治疗一系列实体瘤
来源:生物谷原创 2022-09-28 05:39
在一项新的研究中,研究人员确定了一种在多种肿瘤类型的癌细胞中高度表达但在人体健康组织中很少表达的泛癌抗原成分:一种由胶原蛋白VI α-3型基因的第6外显子编码的泛癌表位。
尽管过继性T细胞疗法被炒得沸沸扬扬,但要找到在不同肿瘤类型中一致性表达但在健康细胞中不表达的治疗靶标仍是一个挑战。如今,在一项新的研究中,来自美国宾夕法尼亚大学和德国Immatics生物技术公司(下称Immatics公司)的研究人员确定了一种泛癌抗原成分:COL6A3-FLNV,可以满足这两个条件。相关研究结果近期发表在Science Translational Medicine期刊上,论文标题为“Quantitative immunopeptidomics reveals a tumor stroma–specific target for T cell therapy”。

在这项新的研究中,这些作者指出利用T细胞受体(TCR)T细胞(TCR-T)疗法靶向他们发现的一种泛癌抗原成分时,可以减缓小鼠的癌症生长。这种泛癌抗原成分在11种不同类型的实体瘤患者的肿瘤样本中大量存在,但在健康细胞中却很少存在,这使它成为T细胞疗法的主要潜在靶标。如今,Immatics公司计划向美国食品药品管理局(FDA)申请试验性新药,希望能启动1期临床试验。
这些作者的研究目标是找到存在于不同肿瘤类型中的抗原,并在不伤害其他细胞的情况下安全地利用T细胞疗法加以靶向。他们首先用Immatics公司的XPRESIDENT发现平台分析了几组正常组织样本和肿瘤组织样本,该平台使用质谱来检查和比较免疫肽组(immunopeptidome)---与人类白细胞抗原相关的肽的集合---中的数百种肽。通过将XPRESIDENT分析与该公司的XCUBE生物信息学方法组合使用,就可利用人工智能来定量确定每个细胞中的肽拷贝数。
论文共同通讯作者、Immatics公司首席创新官Toni Weinschenk在一封电子邮件中解释道,“我们检测并定量确定那里存在的肽,以及癌症和正常组织之间的差别。”在其他研究中,免疫系统中的肽已通过结合预测进行了分析。但有了Immatics公司的发现平台和生物信息学工具的帮助,这些作者可以采取定量的方法。Weinschenk说,“我们无需进行预测。”
这些作者确定了一种在多种肿瘤类型的癌细胞中高度表达但在人体健康组织中很少表达的泛癌抗原成分:一种由胶原蛋白VI α-3型(collagen type VI α-3, COL6A3)基因的第6外显子编码的泛癌表位,它是由一种肿瘤特异性选择性剪接事件产生的,这种选择性剪接事件在健康细胞中很少发生。COL6A3蛋白是VI型胶原蛋白的一个组成部分,存在于整个身体的结缔组织中,但外显子6只在肿瘤微环境的基质细胞中表达。
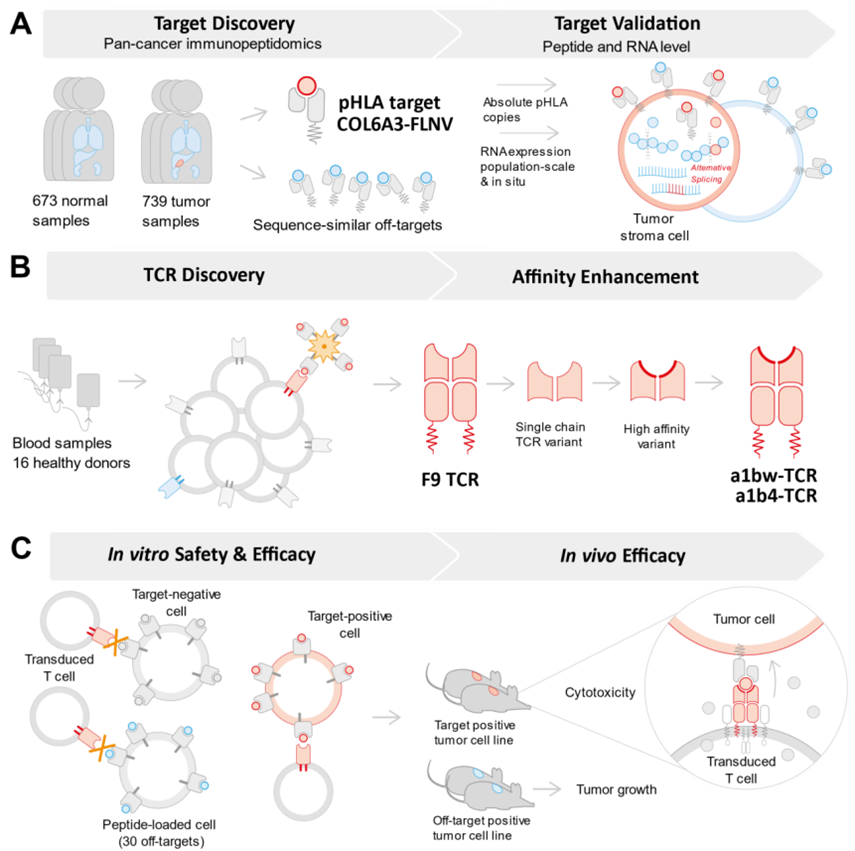
概述了适合过继T细胞治疗的HLA限制性肿瘤靶标和TCR的发现和验证。图片来自Science Translational Medicine, 2022, doi:10.1126/scitranslmed.abo6135。
Weinschenk说,“COL6A3蛋白大量表达,因此没有足够的选择性,无法成为过继性细胞疗法的靶标。这种肿瘤选择性是基于肿瘤相关的剪接事件,它保留了编码靶标的外显子6。”
有了他们的靶标,这些作者着手开发能够识别该表位而不攻击其他肽的TCR。他们再次利用Immatics发现平台的数据来比较肿瘤细胞和正常细胞之间的反应性,开发出高亲和力的TCR-T细胞,并将它们注射到接受人类白血病细胞移植的小鼠体内。癌症的生长速度减慢了,而且小鼠也没有出现严重的副作用。
对Weinschenk来说,这些结果表明Immatics公司的XPRESIDENT方法不仅可用于识别潜在的治疗靶标,还可用于开发具有强大安全性的TCR。接下来,这些作者计划针对这种COL6A3表位进行更多的研究,以便开展针对它的临床试验。(生物谷 Bioon.com)
参考资料:
1. Gloria B. Kim et al. Quantitative immunopeptidomics reveals a tumor stroma–specific target for T cell therapy. Science Translational Medicine, 2022, doi:10.1126/scitranslmed.abo6135.
2. One protein, many cancers: Immatics finds a multi-tumor target for adoptive T-cell therapies
https://www.fiercebiotech.com/research/one-protein-many-cancers-immatics-finds-multi-tumor-target-adoptive-t-cell-therapies
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


