Science:揭示细胞毒性T细胞如何重新装上武器,进行一次又一次的杀戮
来源:本站原创 2021-10-16 09:55
细胞毒性T细胞(CTL)是免疫系统中的重要细胞,能够识别并摧毁癌细胞和受到病毒感染的细胞。这种杀伤性是由专门的溶细胞蛋白---包括穿孔蛋白和颗粒酶B---的释放所介导的,这些溶细胞蛋白来自储存的分泌颗粒。使CTL成为特别有效的杀手的一个特点是它们能够进行持续的、连续的杀伤,单个CTL攻击多个目标,一个接一个地
2021年10月16日讯/生物谷BIOON/---细胞毒性T细胞(CTL)是免疫系统中的重要细胞,能够识别并摧毁癌细胞和受到病毒感染的细胞。这种杀伤性是由专门的溶细胞蛋白---包括穿孔蛋白和颗粒酶B---的释放所介导的,这些溶细胞蛋白来自储存的分泌颗粒。使CTL成为特别有效的杀手的一个特点是它们能够进行持续的、连续的杀伤,单个CTL攻击多个目标,一个接一个地攻击。尽管线粒体质量与CTL抗肿瘤活性相关,但CTL表现出对糖酵解的依赖性增加,这表明对线粒体呼吸的依赖性降低。在CTL寻找、识别和杀伤它们的目标时,线粒体是否、如何或为何做出贡献,目前还不是很清楚。
USP30(ubiquitin carboxyl-terminal hydrolase 30, 泛素羧基末端水解酶30)是一种已知可抑制线粒体自噬的去泛素酶,在对单基因缺失小鼠的大规模筛选中被确定为CTL杀伤性的调节因子。这些结果表明线粒体可能在CTL生物学特性中发挥了一种以前未被重视的作用。因此,在一项新的研究中,来自英国剑桥大学和邓迪大学的研究人员获得了来自USP30缺陷小鼠的CTL,以研究这种缺陷的性质,并了解它如何影响CTL的杀伤性。相关研究结果发表在2021年10月15日的Science期刊上,论文标题为“Mitochondrial translation is required for sustained killing by cytotoxic T cells”。

USP30缺陷小鼠的T细胞发育不受影响。然而,一旦遭受激活,CD8+T细胞产生的CTL具有急性线粒体损失和杀伤力受损。USP30缺陷的CTL的细胞毒性随着时间的推移而减弱,表明其持续杀伤力有缺陷。尽管Usp30-/- CTL失去了线粒体并降低了氧化磷酸化,但是它们的迁移能力、信号传递和分泌---这些都是CTL杀伤性所需的---都是完整的。然而,这些作者发现Usp30-/- CTL的分泌颗粒大小减少,新合成的关键溶细胞蛋白---穿孔蛋白和颗粒酶B---的中间产物也减少。这表明在蛋白从头合成过程中存在内在的缺陷,而这种蛋白从头合成正是持续杀伤所必需的。
监测蛋白翻译发现Usp30-/- CTL的蛋白合成明显减少。通过使用质谱法了解蛋白翻译缺陷是否同样影响所有的蛋白质,他们发现只有一部分细胞质蛋白受到影响,包括杀伤反应的关键介质:颗粒酶B、穿孔蛋白和肿瘤坏死因子-α(TNF-α)和干扰素-γ(IFN-γ)。CTL不需要有效的氧化磷酸化来维持它们的细胞毒性。然而,用多西环素或氯霉素选择性地抑制线粒体翻译,削弱了溶细胞蛋白的翻译,这表明线粒体翻译在持续的CTL杀伤中起着重要作用。
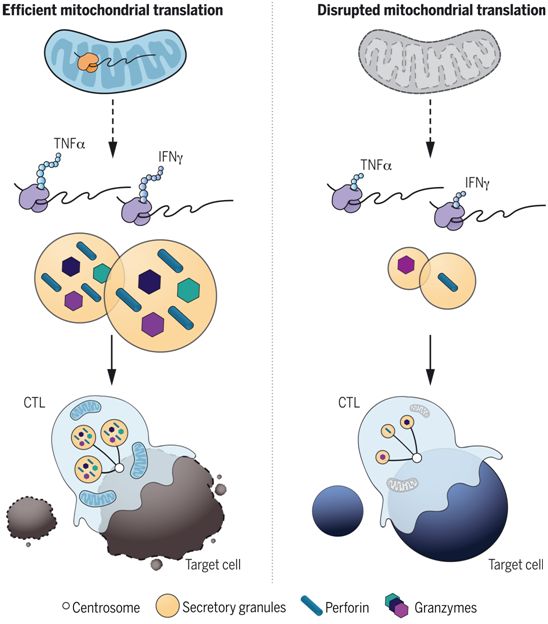
线粒体调节CTL的持续杀伤性,图片来自Science, 2021, doi:10.1126/science.abe9977。
线粒体翻译如何选择性地影响溶细胞蛋白的翻译并调节CTL的杀伤能力?mTOR信号和整合应激反应(integrated stress response)的激活都没有引起Usp30-/-CTL的细胞翻译和杀伤性丧失。然而,在USP30剔除的CTL和经过多西环素处理的CTL中,可以兼作RNA结合蛋白(RBP)的代谢酶的表达发生了改变。因此,这些研究结果表明RBP的转录后调节--一种在CTL中被充分描述的现象---可能调控USP30缺失后检测到的蛋白合成选择性下调。
综上所述,这项研究强调了线粒体作为CTL杀伤性的稳态调节者发挥作用,线粒体蛋白翻译与新的溶细胞蛋白产生保持同步。通过这种方式,蛋白合成的能量需求可以被微调,以满足免疫挑战期间的CTL连续性杀伤需求。(生物谷 Bioon.com)
参考资料:
Miriam Lisci et al. Mitochondrial translation is required for sustained killing by cytotoxic T cells. Science, 2021, doi:10.1126/science.abe9977.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


