重要研究成果聚焦科学家们在PD-1疗法研究中取得的新成果!
来源:本站原创 2020-06-20 17:15
本文中,小编整理了多篇重要研究成果,共同聚焦科学家们在PD-1疗法研究中取得的新成果,分享给大家!图片来源:Nature【1】Nature:揭示ILC2细胞可增强抗PD-1免疫疗法的功效doi:10.1038/s41586-020-2015-4先天淋巴细胞(innate lymphoid cells, ILC),也被称作固有免疫细胞,是一类不同于T细胞和B细
本文中,小编整理了多篇重要研究成果,共同聚焦科学家们在PD-1疗法研究中取得的新成果,分享给大家!
图片来源:Nature
【1】Nature:揭示ILC2细胞可增强抗PD-1免疫疗法的功效
doi:10.1038/s41586-020-2015-4
先天淋巴细胞(innate lymphoid cells, ILC),也被称作固有免疫细胞,是一类不同于T细胞和B细胞的淋巴细胞亚群,位于肠道粘膜表面中,增强免疫反应,维持粘膜完整性和促进淋巴器官形成。它们缺乏克隆性的抗原受体,在分化过程中也没有经历Rag基因的重排过程。在感染之后的数小时之内,ILC就能够活化产生保护性的效应。根据细胞因子表达谱的不同,ILC能够分为三大类群:ILC1、ILC2和ILC3,其中ILC1类似于Th1,主要表达IFN-g,这类细胞主要针对胞内细菌与寄生虫感染;ILC2和与Th2类似,表达IL-5、IL-13等细胞因子,它们对于寄生虫感染以及过敏反应产生有效的保护措施;ILC3表达IL-17A与IL-22,它们参与了肠道的细菌感染反应。一旦遭受有害的应激,它们就会产生大量的细胞因子效应物。这些ILC在调节I型、2型和3型(或者说Th17细胞)免疫反应中发挥着至关重要的作用,这些免疫反应控制着宿主保护性免疫反应和肠道稳态。
ILC2调节哺乳动物组织中的炎症和免疫力。尽管在这些组织的癌症中发现了ILC2,但是它们在抗癌免疫反应和免疫治疗中的作用尚不清楚。在一项新的研究中,来自美国纪念斯隆凯特琳癌症中心等研究机构的研究人员发现ILC2浸润到胰腺导管腺癌(PDAC)中以激活组织特异性的抗肿瘤免疫反应。白介素-33(IL33)激活小鼠原位胰腺肿瘤中的肿瘤ILC2和CD8+ T细胞,但不激活小鼠异位皮肤肿瘤中的肿瘤ILC2和CD8+ T细胞,从而抑制胰腺特异性的肿瘤生长,相关研究结果近期发表在Nature期刊上。
【2】Science子刊:阻断EGFR改善抗PD-1药物对EGFR突变肺腺癌的疗效
doi:10.1126/sciimmunol.aav3937
肺癌是全世界癌症相关死亡的主要原因之一。大约80%的肺癌病例被归类为非小细胞肺癌(NSCLC)。在NSCLC中已经报道了几种致癌驱动基因的改变,包括表皮生长因子受体(EGFR)编码基因和间变性淋巴瘤激酶(ALK)编码基因。在一项新的研究中,来自日本国家癌症中心和名古屋大学等研究机构的研究人员研究了EGFR突变肺腺癌的肿瘤微环境(TME)中的免疫表型,其中对EGFR突变肺腺癌(EGFR-mutated lung adenocarcinoma, 即发生EGFR突变的肺腺癌)而言,抗PD-1单抗药物治疗在很大程度上是无效的,相关研究结果发表在Science Immunology期刊上。
然而,EGFR突变肺腺癌具有未发炎的免疫抑制性肿瘤微环境,而通常存在于发炎的肿瘤微环境中的CD4+效应调节T细胞(CD4+ effector regulatory T cell)在那里显示出较高的浸润。 EGFR信号激活JNK(cJun N-terminal kinase, cJun N末端激酶)/cJUN并降低干扰素调节因子-1(IRF1):前者增加CCL22,从而招募CD4+调节性T细胞;后者下降CXCL10和CCL5,从而诱导CD8+T细胞浸润。
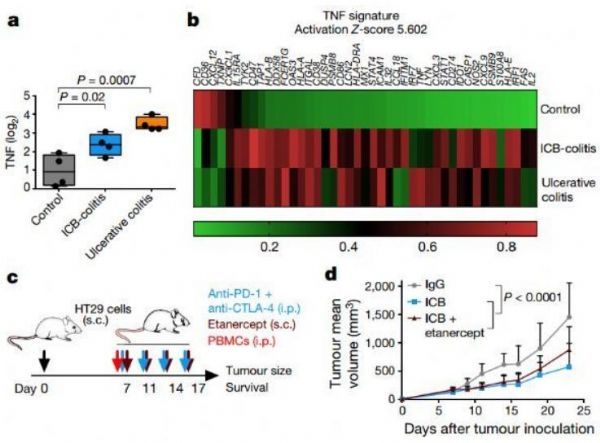
【3】Nature:预先抑制TNF显著增强PD-1和CTLA-4联合免疫疗法疗效并降低副作用
doi:10.1038/s41586-019-1162-y
由Cima和纳瓦拉临床大学的研究人员领导的一项合作实验研究提出了一种治疗癌症的新方法,即在动物模型中使用联合免疫疗法解决疗效和毒性的问题。这种临床策略包括阻断一种参与免疫系统调节的蛋白(称为肿瘤坏死因子,TNF),同时联合免疫治疗(抑制PD-1和CTLA-4等其他“减缓”免疫反应的蛋白)。相关研究成果于近日发表在Natrue上。
在这项研究中,我们发现肿瘤坏死因子的免疫调节功能是可有可无的,甚至在某种程度上对这种联合免疫疗法有害。我们已经在这些动物模型中证实,免疫治疗前预防性阻断TNF可以避免不良反应,提高治疗反应。这使我们能够更好地调整药物的剂量,从而达到更强的抗肿瘤效果。研究者表示,因为在预防方面,它意味着我们可以使用我们在日常实践中已经使用的方法来治疗自身免疫不良反应。”专家们指出,下一步的工作是把这项研究转移到临床。Melero博士说:“如果我们在病人身上取得这项研究的结果,它将改变治疗癌症的模式。然而,尽管在动物模型上有这些有希望的结果,我们必须对它们的解释非常谨慎,因为我们不确定它们是否会在正在进行的临床试验的患者身上得到复制,还是会在即将开始治疗的患者身上复制。
【4】Nat Med:一次抗PD-1治疗可以预测黑色素瘤病人预后!
doi:10.1038/s41591-019-0357-y
黑色素瘤病人对抗PD-1的疗法的免疫反应在治疗后很快就会发生,3周后就可以在血液中检测到反应性T淋巴细胞。但是研究人员并不清楚这种早期的基于血液的检测是否可以代表肿瘤微环境的变化。为此,来自宾夕法尼亚大学等单位的研究人员在III/IV期黑色素瘤病人身上进行了一项新辅助抗PD-1治疗的临床试验,发现在手术前进行一次辅助性抗PD-1治疗可以预测可手术切除的黑色素瘤病人的临床治疗效果,相关研究成果于近日发表在Nature Medicine上。
在实验开始之前研究人员猜想抗PD-1治疗后3周应该可以检测到肿瘤组织中的免疫系统的恢复,因此这种响应将与无疾病生存期相关。研究人员在手术前给27名病人进行了一次抗PD-1治疗,结果所有人体内都检测到了快速、强烈的抗肿瘤反应,其中8个病人甚至经历了完全有或者主要病理学响应,他们都处于无肿瘤的状态。
【5】Cancer Res:联合靶向miR-146a和PD-1可增强抗肿瘤免疫有效治疗黑色素瘤
doi:10.1158/0008-5472.CAN-18-1397
microRNA是细胞内表达的一些小的非编码RNA,能够在转录后水平调节基因表达,并在多种癌症类型中调控免疫应答反应。最近来自德国弗莱堡大学医学中心的研究人员在黑色素瘤微环境中发现了一种microRNA能够抑制抗肿瘤免疫应答,同时提出了治疗黑色素瘤的新策略。相关研究结果发表在国际学术期刊Cancer Research上。
在这项研究中,研究人员发现miR-146a能够作为免疫激活的负调控因子发挥类似免疫检查点分子的作用。研究表明miR-146a在黑色素瘤微环境组织中存在表达水平增加,miR-146a敲除小鼠存活更久并且相比野生型黑色素瘤荷瘤小鼠形成的转移灶更少。
图片来源:Wikipedia/CC BY-SA 3.0
【6】Science子刊:揭示免疫检查点阻断疗法副作用!抗PD-1治疗会破坏阿片类药物的镇痛作用
doi:10.1126/scitranslmed.aaw6471
使用PD-1靶向抗体的免疫检查点阻断疗法已显示出可治疗多种肿瘤的令人鼓舞的结果。阿片类药物治疗通常用于癌症患者,以控制与疾病相关的疼痛,比如吗啡通过μ阿片类药物受体(MOR)产生镇痛作用。但是,神经元中的PD-1信号很大程度上未知。近期已有人报道背根神经节(dorsal root ganglion, DRG)初级感觉神经元表达PD-1,PD-1的激活抑制神经元兴奋性和疼痛。在一项新的研究中,来自美国杜克大学医学中心等研究机构的研究人员报道吗啡镇痛作用和MOR信号转导需要神经元PD-1。相关研究结果发表在Science Translational Medicine期刊上。
在Pd1敲除小鼠中,全身或鞘内注射吗啡后,它引起的镇痛作用受到破坏。在静脉或鞘内注射纳武单抗(一种临床上使用的抗PD-1单克隆抗体)后,吗啡在野生型小鼠中的镇痛作用也有所减轻。在炎症性、神经性和癌症性疼痛的小鼠模型中,脊髓吗啡镇痛作用在敲除它们的PD-1后受到破坏。MOR和PD-1在小鼠和人类DRG组织中的感觉神经元及其轴突中共表达。
【7】Nat Commun:阻断Siah2可增强PD-1抑制剂的抗肿瘤免疫反应
doi:10.1038/s41467-019-13826-7
在一项新的研究中,来自美国桑福德-伯纳姆-普利贝斯医学发现研究所和纽约大学医学院的研究人员发现了一种新方法来提高免疫系统抵抗癌症的能力。他们利用小鼠模型鉴定出Siah2蛋白在控制一类称为调节性T细胞(Treg)的免疫细胞中起着重要作用,这限制了目前使用的免疫疗法的有效性,相关研究结果近期发表在Nature Communications期刊上。
研究者表示,尽管Siah2参与控制调节癌症产生的事件,但是这项研究提供了它在免疫系统的抗肿瘤免疫反应中发挥作用的首个直接证据。我们的研究表明,在缺乏Siah2基因的小鼠中,PD-1抑制剂可用于治疗目前对该疗法没有反应的肿瘤,从而为扩大免疫疗法的有效性提供了手段。这些发现也为我们努力寻找一种可阻断Siah2的药物提供了进一步的理由。
【8】Science子刊:挑战常规!陈列平教授发现激活PD-1H有望治疗狼疮
doi:10.1126/scitranslmed.aax1159
在过去的十年中,科学家们已发现阻断免疫系统的关键调节因子有助于激活身体对多种形式癌症的天然防御能力,从而开启了癌症免疫疗法的新时代。比如,免疫检查点阻断药物(也称为免疫检查点抑制剂)通过阻断T细胞表面上的免疫检查点PD-1或CTLA-4来对癌症发起免疫攻击,可有效地治疗很多癌症。
如今,在一项新的研究中,来自美国耶鲁大学的研究人员从本质上推翻了这一观点,他们通过基因敲除培育出缺乏免疫抑制性受体PD-1H(也称为VISTA或B7-H5)的BALB/c小鼠,并且发现这些PD-1H敲除小鼠会产生类似于人类两种狼疮形式---系统性狼疮和皮肤狼疮---的全身性自身免疫性疾病和皮肤自身免疫性疾病,并且更易受降植烷(pristane)诱导的自身免疫的影响。在系统性狼疮中,免疫系统攻击多种器官,而皮肤型狼疮的典型特征为明显的皮肤畸形,相关研究结果近期发表在Science Translational Medicine期刊上。
这些发现表明PD-1H功能受损会引起对皮肤和器官的破坏性免疫系统攻击,这正是自身免疫性疾病狼疮的典型特征。此外,这些PD-1H敲除小鼠的皮肤狼疮病灶聚集着浆细胞样树突细胞(pDC),这与人皮肤盘状红斑狼疮中的情形相类似。PD-1H分子明显地参与抑制狼疮,但是它似乎具有选择性,这是因为它在其他几种自身免疫性疾病中没有相同的作用。
【9】Nat Med:临床试验表明免疫诱导策略可提高转移性三阴性乳腺癌对PD-1阻断的敏感性
doi:10.1038/s41591-019-0432-4
PD-1阻断在治疗转移性三阴性乳腺癌(triple-negative breast cancer, TNBC)中的具有较低的疗效,这突出了需要开发让肿瘤微环境对PD-1阻断更敏感的策略。临床前研究已指出化疗和放疗的免疫调节特性。在一项适应性非对比的2期临床研究的第一阶段中,来自荷兰癌症研究院等研究机构的研究人员对67名转移性TNBC患者进行随机分配,让这些患者接受以下多种治疗方案中的一种:(1)纳武单抗,但未经化疗或放疗诱导,下称未诱导组;(2)纳武单抗,且接受2周低剂量放疗(3?×?8?Gy)诱导,下称放疗组;(3)纳武单抗,且接受2周低剂量环磷酰胺诱导,下称环磷酰胺组;(4)纳武单抗,且接受2周低剂量顺铂诱导,下称顺铂组;(5)纳武单抗,且接受2周低剂量阿霉素诱导,下称阿霉素组;所有患者均随后使用纳武单抗。相关研究结果近期发表在Nature Medicine期刊上。
在这整个队列中,客观反应率(ORR; iRECIST)为20%。大多数反应是在顺铂组(ORR 23%)和阿霉素组(ORR 35%)中观察到的。在阿霉素和顺铂诱导后,这些研究人员检测到PD-1/PD-L1和T细胞细胞毒性途径中的免疫相关基因上调。在阿霉素诱导后,与炎症、JAK–STAT和TNF-α信号转导相关的上调基因的富集进一步支持了这一点。
【10】Nat Med:肥胖竟可促进PD-1免疫检查点抑制剂治疗癌症
doi:10.1038/s41591-018-0221-5
在一项开创性的新研究中,来自美国加州大学戴维斯分校的研究人员揭示了为什么肥胖会促进癌症生长,并同时又允许新的重磅炸弹免疫治疗药物更好地对抗相同的癌症。这些充满矛盾的发现为癌症医生在给癌症患者选择药物和其他治疗方法时提供了重要的新信息,相关研究结果发表在Nature Medicine期刊上。
研究者表示,这是违反直觉的,这是因为到目前为止,我们所有的研究都已显示肥胖导致更多的与免疫治疗相关的毒性。这会引发观念变革,这是因为当我们开展个人化治疗和研究身体质量指数(BMI)时,它在某些情况下可能是不好的,在某些情况下可能是有益的。肥胖正达到大流行水平并成为多种癌症的主要风险因素。众所周知,它会加快癌症生长,促进癌症复发并恶化生存机会。肥胖也与免疫系统受损有关。之前利用免疫刺激性免疫治疗药物开展的研究已表明在肥胖动物模型和肥胖的人中,这些药物过度刺激免疫系统并引起严重的副作用。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。