研究揭示RYBP-/YAF2-PRC1复合物和组蛋白H1介导染色质压缩协同促进H2AK119ub蔓延和继承的分子机制
来源:生物物理所 2020-03-26 09:25
3月23日,中国科学院生物物理研究所生物大分子国家重点实验室李国红课题组在Nature Cell Biology上发表了题为RYBP/YAF2-PRC1 complexes and histone H1-dependent chromatin compaction mediate propagation of H2AK119ub1 during
3月23日,中国科学院生物物理研究所生物大分子国家重点实验室李国红课题组在Nature Cell Biology上发表了题为RYBP/YAF2-PRC1 complexes and histone H1-dependent chromatin compaction mediate propagation of H2AK119ub1 during cell division 的文章。该研究系统阐述了组蛋白修饰H2AK119ub1在染色质上蔓延以及跨细胞周期继承的具体机制。
真核细胞内,染色质是表观遗传信息的主要调控界面。诸多表观遗传因子通过调节染色质结构的开放与关闭,控制了基因的表达与沉默,从而维持了不同谱系细胞内基因的差异表达。其中,多梳抑制复合物1(PRC1)是一类重要的表观遗传调控因子,它主要通过压缩染色质结构和催化形成H2AK119ub1修饰这两种途径促进了兼性异染色质的形成,并以此维持了PRC1靶基因的沉默状态。H2AK119ub1在染色质局部往往连绵不断形成非常宽广的H2AK119ub1区域,但是其产生的机制一直未被解析。
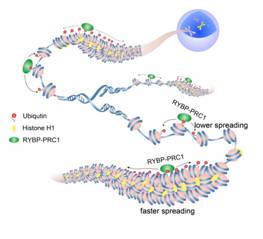
李国红课题组结合核小体pull-down、体外泛素化、TetR-TetO靶向和CHIP-seq等实验发现RYBP和YAF2蛋白能通过ZNF结构域特异识别并结合H2AK119ub1,借此使RYBP-PRC1和YAF2-PRC1复合物与其催化产物之间形成所谓的“酶-产物之间的正反馈机制”,从而促进了H2AK119ub1向周边的蔓延。有趣的是,通过基于组蛋白修饰和DNaseI高敏位点的染色质状态分析,作者发现H2AK119ub1主要分布在结构紧密的异染色质区域,因此提出非常规PRC1介导的H2AK119ub1蔓延也可能受到染色质高级结构的调控。之前,李国红和朱平课题组合作,利用冷冻电镜技术解析了组蛋白H1压缩30nm染色质纤维的高精度结构,揭示染色质纤维是以四核小体为结构单元的左手双螺旋结构,并发现相间核小体之间的相互作用在维系四核小体内部和四核小体之间的稳定性中发挥了重要作用。因此,30nm染色质纤维可能通过核小体-核小体配对(nucleosome-pairing)的方式促进了非常规PRC1介导的H2AK119ub1在染色质纤维上的蔓延。基于该假设,作者进行了进一步的实验并发现H1压缩的30nm染色质纤维的确促进了H2AK119ub1向邻近染色质区域的蔓延。在体外泛素化实验中,作者通过引入组蛋白相应位置的突变体,证明H1对H2AK119ub1蔓延的促进作用主要通过改变染色质高级结构来实现。并且,根据30nm染色质纤维的电镜结构,作者推测这种促进机制可能遵循相间核小体-核小体的配对原则。
众所周知,DNA复制过程中染色质会经历一次“破坏-重建”的过程。在DNA子链上新合成组蛋白的装配会导致组蛋白修饰至少稀释一倍,如果没有有效的组蛋白修饰恢复机制,细胞身份很难得以维持。那么以上机制是否也介导了H2AK119ub1在细胞周期的继承呢?利用TetR-TetO靶向系统,作者发现单纯靶向RING1B在8xTetO附近仅能形成很窄的H2AK119ub1修饰,当利用多西环素(Doxcycline,Dox)洗去RING1B-TetR-HA时,异位形成的H2AK119ub1修饰并不能在子代细胞内得到有效维持。然而过表达RYBP促进H2AK119ub1向两侧蔓延形成大约10kb的区域时,实验发现正反馈机制能介导H2AK119ub1在8xTetO附近维持至少6个细胞周期。同时,作者发现H1介导的染色质压缩对于H2AK119ub1的遗传也至关重要。另外在全基因组上,作者发现RYBP突变和H1c/H1d/H1e三敲除导致的H2AK119ub1降低以及基因表达变化有很大程度的重叠。并且利用神经分化模型,作者发现RYBP突变和H1c/H1d/H1e三敲除均导致神经前体细胞分化障碍。因此,说明RYBP-/YAF2-PRC1复合物和组蛋白H1通过协同促进细胞周期间H2AK119ub1的播散参与了细胞分化过程,提示该表观遗传通路具有重要的生物学功能。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


