高精度全脑血管图谱揭示阿尔茨海默症模型小鼠脑内血管损伤
来源:上海药物研究所 2019-12-12 21:48
阿尔茨海默症(Alzheimer’s disease,AD)是一种严重的中枢神经系统退行性疾病,临床上缺乏能够有效延缓或逆转疾病进程的药物及干预手段,严重危害老年人的身体健康和生活质量,给家庭和社会带来巨大负担。AD的发病机制一直存在胆碱能缺损、β-淀粉样蛋白级联反应、Tau蛋白过度磷酸化等多种假说,然而针对这些假说研发的单一作用机制的药物尚未取得理想的临床
阿尔茨海默症(Alzheimer’s disease,AD)是一种严重的中枢神经系统退行性疾病,临床上缺乏能够有效延缓或逆转疾病进程的药物及干预手段,严重危害老年人的身体健康和生活质量,给家庭和社会带来巨大负担。AD的发病机制一直存在胆碱能缺损、β-淀粉样蛋白级联反应、Tau蛋白过度磷酸化等多种假说,然而针对这些假说研发的单一作用机制的药物尚未取得理想的临床疗效,提示人类对AD发病机制的认识依然存在极大局限,亟需探索新的突破手段。
中国科学院上海药物研究所蒋华良、高召兵和章海燕三个课题组合作,开展AD发病机制和抗AD药物相关研究。近期,在《国家科学评论》(National Science Review)发表了题为High-resolution mapping of brain vasculature and its impairment in the hippocampus of Alzheimer’s disease mice 的研究论文,报道了首个转基因AD模型小鼠的高精度全脑血管网络图谱,结果显示AD模型小鼠脑内特别是海马区的血管系统显着受损,提示血管损伤在AD病理过程中的重要性之前远未充分认识,为发展高效AD治疗药物及干预手段指出了新的方向。
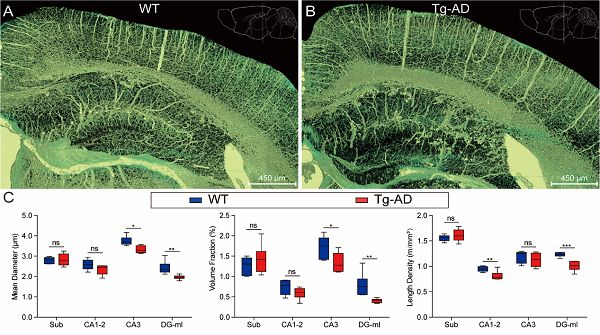
全脑血管网络的构筑尤其是微循环系统的高精度解析是获得这项研究成果的前提条件。在此之前,实现全脑尺度高分辨率成像、低信噪比影像数据增强、高空间复杂度三维图像数据的可视化和量化分析等方面依然面临诸多挑战。在该项工作中,研究团队应用华中科技大学教授骆清铭团队发展的原创MOST技术,首次在0.35 × 0.35 × 1.00微米分辨率水平上获取了app/PS1转基因AD模型小鼠(Tg-AD)的全脑数据集,再应用团队自己发展的算法对预处理后图像进行优化,构建了包含从直径几十微米的大血管到小于2微米的毛细血管的完整小鼠全脑跨尺度3D血管图谱(图1和视频1)。通过系统定量分析AD模型与野生型小鼠的脑血管网络,发现在AD模型小鼠中海马血管的平均血管直径、血管体积分数(单位体积组织内的血管容积)均显着降低。进一步对海马不同亚区的比较分析揭示了齿状回分子层(DG-ml)的平均血管直径、血管长度密度(单位体积组织内的血管长度)及血管体积分数的降低程度最为显着(图2)。此外,对单枝血管分支模式的量化分析结果说明,除了血管的变细、减少外,AD模型小鼠血管分支角度显着变小,导致单枝海马血管的血液灌注面积减少。采用研究团队首创的虚拟血管内窥技术,该研究还进一步揭示了AD模型与野生型小鼠在血管管腔内壁粗糙度、分支节点平滑度上均有显着差异(见图3和视频2)。上述研究结果证明了脑血管系统以及海马微循环在AD病理过程中的重要角色。
为开展此项研究,上海药物所组建了包括计算机图像处理、神经药理学、药物研发等多专业背景的交叉学科研究团队,聚焦微血管高精度图谱的构建与分析,发展了针对冠状面数据进行背景校正、噪声抑制、对比度增强的高效图像优化算法,搭建了快速高精度三维渲染、微结构形态学量化分析软硬件平台,实现了TB级别规模(万亿字节,20000×30000×12000Voxels)的三维图谱数据挖掘。
研究团队通过对2月龄的野生型小鼠的全脑血管网络量化分析后发现,在不超过0.2立方厘米的脑组织中竟然分布着总长超过300米的庞杂血管网络,并且不同脑区的血管分布规律及形态特征也存在明显的差异。此外,与皮层、丘脑等脑区相比,海马的平均血管直径、血管长度密度、血管体积分数均最低。通过对完整海马血管的高精度可视化,发现整个海马的横行血管垂直于海马纵轴呈耙式平行分布。此外,海马齿状回分子层的主要血管从上级主血管分出后直径急剧降低,在分支角度上也接近直角(图1)。这种呈现出来的独特的梳状血管分支模式,明显不同于其他海马亚区血管的逐步分级的分支模式。海马齿状回分子层血管特殊的分支模式可能导致其更容易受到损伤,这也与AD模型小鼠齿状回分子层平均血管直径、血管长度密度及血管体积分数的降低程度相吻合。
该研究中发展的高分辨率跨尺度的可视化及定量分析能力不仅适用于小鼠脑血管研究,还可用于其他具有更大空间尺度的大鼠、猴以及人类的脑血管研究,有助于跨尺度综合分析脑相关疾病和血管系统损伤的相关性。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


