RNAi药物,未来靶向药不可或缺的主力军 ---圣诺制药总裁兼CEO陆阳博士专访
来源:生物谷 2019-11-08 14:38
2019年10月31日至11月1日,第七届华兴资本医疗与生命科技领袖峰会在上海举行。本届峰会迎来了超过500位全球医疗与生命科技领域的顶尖科学家、企业CEO和投资人参与,超过100位重磅嘉宾上台分享,共同探讨创新药全球注册、生物科技企业治理和跨界合作、基因治疗及细胞治疗的新征程等议题。会后,生物谷对圣诺制药总裁兼CEO陆阳(Patrick Lu)博士进行了专访,就小干扰核酸药物的应用及未来发展进行
2019年10月31日至11月1日,第七届华兴资本医疗与生命科技领袖峰会在上海举行。本届峰会迎来了超过500位全球医疗与生命科技领域的顶尖科学家、企业CEO和投资人参与,超过100位重磅嘉宾上台分享,共同探讨创新药全球注册、生物科技企业治理和跨界合作、基因治疗及细胞治疗的新征程等议题。
会后,生物谷对圣诺制药总裁兼CEO陆阳(Patrick Lu)博士进行了专访,就小干扰核酸药物的应用及未来发展进行了深入探讨。
什么是小干扰核酸药物?
小核酸药物可以是所有寡核酸药物包括小干扰核酸、反义核酸、微核酸、核酸酶、适配体等不同结构类型。小干扰核酸(siRNA)药物是利用特定的递送技术将一段21-25个碱基对左右的双链小核酸分子导入靶细胞,激活名为“核酸干扰(RNA interference)”的生物学过程,通过酶解与小干扰核酸分子具有同源序列的mRNA达到靶基因沉默,从而实现对某些病人体内特定靶基因表达的抑制来治疗疾病。
核酸干扰药物与抗体、小分子药物及其他一些蛋白药物的功能和作用机理不同,它可以从mRNA层面直接抑制造成疾病的蛋白生成。如果从精准医疗角度来说,核酸干扰药物是最为精准的抑制剂。也正是因为作用机理不同,跟单抗和小分子药物相比,核酸干扰药物必须要进入细胞内才可以启动RNAi, 因此有一定难度。这就涉及到它的有效性、稳定性、成药性及安全性都与导入技术密切相关。
小干扰核酸药物,导入系统是关键
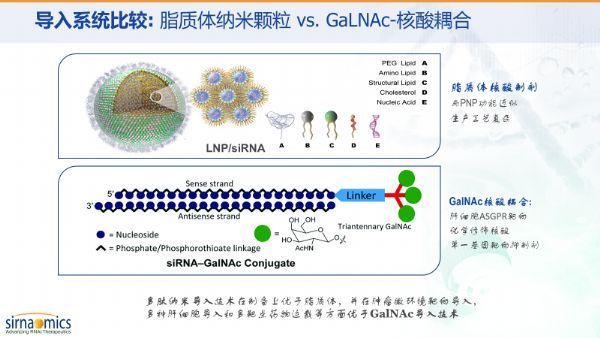
目前已经在临床研究阶段的核酸药物导入技术可分为三大类:第一类是现在比较成熟的脂质体纳米颗粒技术,如去年已经得到美国FDA批准上市的Onpattro就是使用这一技术;第二类是通过化学耦合,在小核酸序列上加入一个可以促进小核酸有效进入肝细胞的GalNAc技术,这类技术目前在国际上较为热门但仅限于肝细胞疾病的应用。
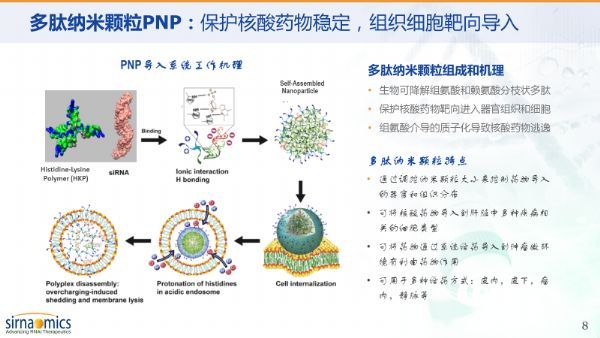
而第三类导入系统是圣诺制药的组氨酸-赖氨酸共聚多肽纳米颗粒(PNP)技术。这项由圣诺制药特有的多肽纳米导入系统使用化学合成的RNAi触发器(siRNA),通过多肽纳米颗粒(PNP)制剂递送至体内靶细胞。这是圣诺制药拥有全球独家知识产权的核心技术。
该类多肽纳米颗粒由易于合成的分支组氨酸赖氨酸多肽(HKP)组成,每个PNP可携带多个siRNA序列,能保证RNA不被肾脏过滤清除,在血液中可保护siRNAs免受周围环境影响,进入靶细胞后可有效释放负载,降解后的产物无毒副作用。这就同时克服了药物的靶向性和稳定性问题,是核酸干扰药物成功的关键。作为单一多肽,该药物在工业制备上的生产远优于脂质体,且生产纯度可以达到99%以上。
随着时间发展,PNP导入技术也不断实现更新迭代。第二代TT-PNP技术在纳米颗粒的基础上,加上肿瘤靶向的基团解决组织和细胞特异性的需求。在具备肿瘤微环境靶向的基础上,对肿瘤细胞和新生血管内皮细胞表面受体的亲和性进一步增强药物导入效率。
注:以下的两张图解释了PNP导入技术的特性,以及与其他核酸药物研发企业所使用的LNP导入系统(Lipidnanoparticles, 脂质纳米粒)和GalNac-核酸耦合导入系统的差异。
除此之外,PNP可以通过增强的渗透性和滞留(EPR)效应来提供siRNA对肿瘤微环境的影响以及抑制肿瘤生长。在肿瘤学(以及纤维化疾病)应用中,已经确定沉默多于一种靶标可以显着改善RNAi药物的功效。 而一个纳米颗粒可同时包两个或多个小核酸作为一个药物使用,即具有双靶点和多靶点的优势。在每种治疗适应症中,集中于鉴定2个沉默基因靶标,通过两者在同一细胞中沉默时产生相加或协同效应,达到更好的治疗效果。
聚焦双靶点,主攻肿瘤及纤维化
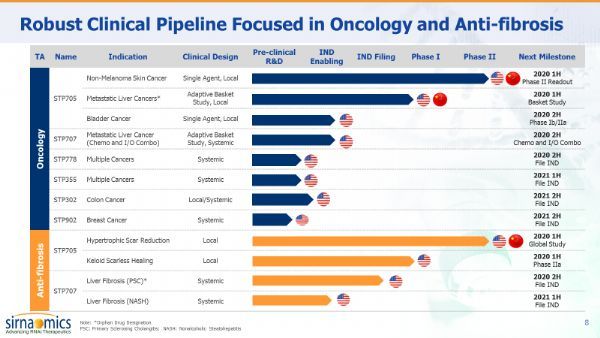
目前圣诺制药已构建了丰富的核酸干扰创新药物产品线,治疗领域覆盖肿瘤和抗纤维化治疗。下图为圣诺最新的研发管线(截止到2019年10月)以及预期的项目进度。
其中,进展最快的siRNA产品科特拉尼(STP705)目前已在美国进展到临床2期,用于治疗非黑色素瘤皮肤癌,该产品在中国处于临床1期阶段。
STP705由两个siRNA寡核苷酸组成,分别以TGF-β1和COX-2的mRNA为靶标,并通过与组氨酸赖氨酸多肽共聚物(HKP)形成纳米粒,促进更为有效的细胞导入。它通过同时抑制这两个靶点,可以诱导纤维细胞的凋亡,这个新的生物学功能也可以用于治疗纤维化疾病和肿瘤治疗。
2017,国内首例核酸干扰创新药STP705的临床申请获得NMPA批准,标志了中国自主创新的核酸干扰药物实现了临床试验“零的突破”。之后,该药在2017下半年获得美国FDA两种治疗原发性硬化性胆管炎(PSC)和胆管癌(CCA)的孤儿药认定。2018年,该核酸干扰药物用于晚期肝胆管细胞癌(CCA)治疗的临床研究申报获得美国FDA批准, 并在2019年中进入临床试验。
圣诺制药的主要研究方向聚焦在抗肿瘤及抗组织纤维化。 抗纤维化包括现有的疤痕纤维化和肝纤维化,其中,由非酒精引起的脂肪肝硬化市场广阔,是其未来主攻的临床方向。除此之外,圣诺也将尝试在肾纤维化领域进行研究。
而在肿瘤方面,小干扰核酸药物的研究涉及广泛,包括肝的胆管癌、非黑色素瘤的皮肤癌、肝癌、胰腺癌和膀胱癌。该公司研发的第二代具有肿瘤靶向性的多肽纳米导入系统已在动物模型上取得优异成果,现在正在推进安全评价和动物治疗效果。除此之外,其小干扰核酸药物STP707与免疫检查点抗体抑制剂联合用药在多个肝细胞癌动物模型实验中协同效应显着, 正在准备临床试验。希望未来可以充分利用TGF-β1核酸干扰抑制剂的优势,结合PD-L1抗体的使用同时抑制这两个靶点,开发出一种新的、具有突破性的肿瘤免疫药物。
生物谷记者与陆阳博士(中)
圣诺制药的公司总部位于美国马里兰州Gaithersburg市,在中国苏州和广州建有分公司,并在美国波士顿和中国香港设立办公室。跨越中美的圣诺制药集团的三家公司分工各异:美国圣诺作为总部负责国际合作、在美国的临床试验以及部分创新项目的开发;苏州圣诺则是中国研发中心和临床试验的协调基地;广州纳泰则是推动在中国的中试和规模化药物制剂生产的基地。
作为一家在核酸干扰(RNAi)药物创制领域领先并已进入多项临床试验阶段的生物制药企业,到目前为止,圣诺制药是全球唯一能够在中美同时推动核酸干扰创新药临床研究的企业和平台。该公司在不断完善技术平台的基础上,将未来商业化运作的重心聚焦于上市后1-3年内临床项目的推进。圣诺制药总裁兼CEO陆阳(Patrick Lu)博士指出: “核酸干扰(RNAi)药物的研发创制在重大疾病治疗领域前景广阔。最近PCSK9核酸干扰药物Inclisiran的临床三期结果表明,它不仅可成药,也必将是未来靶向药物的主力军之一。”如何在抓住核酸干扰治疗药物产业化机遇的同时, 实现在核酸干扰治疗领域创新药物研发中的突破与发展? 让我们拭目以待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->