Cell:解析出趋化因子受体CCR7的三维结构,并鉴定出有望治疗某些常见癌症的化合物
来源:本站原创 2019-08-28 10:18
2019年8月28日讯/生物谷BIOON/---在一项新的研究中,来自瑞士保罗谢勒研究所和制药巨头罗氏公司的研究人员在开发阻止某些癌症转移的药用试剂方面迈出了重要的一步。通过使用瑞士光源(Swiss Light Source),他们解析出一种在癌细胞迁移中起关键作用的受体的结构。这使得鉴定出可以通过身体的淋巴系统阻止某些癌细胞扩散的药用试剂成为可能。相关研究结果近期发表在Cell期刊上,论文标题为
2019年8月28日讯/生物谷BIOON/---在一项新的研究中,来自瑞士保罗谢勒研究所和制药巨头罗氏公司的研究人员在开发阻止某些癌症转移的药用试剂方面迈出了重要的一步。通过使用瑞士光源(Swiss Light Source),他们解析出一种在癌细胞迁移中起关键作用的受体的结构。这使得鉴定出可以通过身体的淋巴系统阻止某些癌细胞扩散的药用试剂成为可能。相关研究结果近期发表在Cell期刊上,论文标题为“Structural Basis for Allosteric Ligand Recognition in the Human CC Chemokine Receptor 7”。
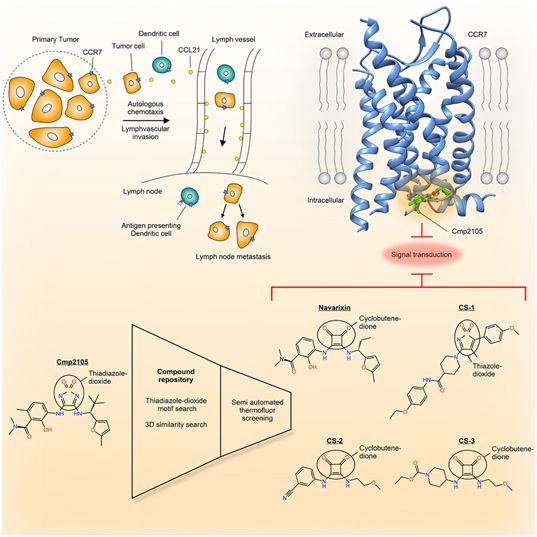
当癌细胞在体内扩散时,称为转移瘤的继发性肿瘤就可形成。这些继发性肿瘤导致大约90%的癌症患者死亡。传播癌细胞的一个重要途径是通过淋巴系统,淋巴系统像血管系统一样贯穿整个身体并将淋巴结彼此相互连接在一起。当白细胞通过淋巴系统迁移以便协调对抗病原体的防御时,作为一种特定的膜蛋白,趋化因子受体7(CCR7)起着重要作用。它位于细胞膜中,它可以接收外部信号并将这些信号传递到细胞内部。在与罗氏公司的合作中,保罗谢勒研究所的研究人员首次能够解析出CCR7的结构,这就为开发可以阻止某些常见的癌症转移的药物奠定基础。
在所有脊椎动物的细胞中,20种不同的趋化因子受体可与40多种称为趋化因子的信号蛋白相互作用。这些信号蛋白中的每一种仅适合于特定的受体。反过来,如果一种信号蛋白与受体结合,它会触发细胞内的过程,从而导致针对这种信号蛋白携带的信号的特定细胞反应。
CCR7是控制体内细胞迁移的受体之一。一旦细胞外的合适信号蛋白与它结合,细胞中的连锁反应就会使得细胞向这种信号蛋白的最高浓度方向移动。细胞遵循这种趋化因子的轨迹移动,就像追踪某种气味的猎犬。比如,作为身体免疫系统的重要细胞,白细胞源源不断地流向淋巴结。
癌细胞也可以利用CCR7并且为了自身的目的滥用这种细胞受体。合适的信号蛋白将它们引导出肿瘤并进入淋巴系统。此外,它们在体内扩散并最终在其他组织中形成转移瘤。这些转移性肿瘤极大地增加了患者的死亡风险。
为了提高癌症患者的存活率,抑制这种癌细胞转移过程具有重要的医学意义。这就是为什么保罗谢勒研究所研究人员在该研究所的瑞士光源(SLS)上使用X射线晶体衍射技术来解析CCR7受体的结构。
这种结构成为了与罗氏公司合作寻找相应活性试剂的基础。论文共同第一作者Steffen Brünle解释道,“合适的活性试剂分子可以阻止信号蛋白与这种受体结合并在细胞内引起反应。”解析这种受体的结构是一个真正的挑战。论文共同通讯作者、保罗谢勒研究所时间分辨晶体学研究小组联合负责人Jörg Standfuss说,“针对这一点的困难之处在于:首先,以我们能够利用X射线晶体学衍射技术研究它们的方式,培养出相应的晶体。”为了加快研究进程,罗氏公司开发了自己的新型蛋白修饰技术模块,即所谓的结晶伴侣蛋白(crystallization chaperone)。
利用关于这种受体精确结构的信息,他们能够鉴定出5种阻断这种受体的潜在药用分子,比如Navarixin,可阻止信号蛋白携带的信号传递到细胞中。Navarixin是一种多靶标拮抗剂。这5种化合物可作为潜在癌症治疗药物的候选药物。Brünle说,“我们的实验表明,细胞内的这种人工分子与这种受体结合。这阻止了导致细胞迁移的连锁反应的启动。” (生物谷 Bioon.com)
参考资料:
1.Kathrin Jaeger et al. Structural Basis for Allosteric Ligand Recognition in the Human CC Chemokine Receptor 7. Cell, 2019, doi:10.1016/j.cell.2019.07.028.
2.Preventing tumor metastasis
https://medicalxpress.com/news/2019-08-tumor-metastasis.html

图片来自Cell, 2019, doi:10.1016/j.cell.2019.07.028。
当癌细胞在体内扩散时,称为转移瘤的继发性肿瘤就可形成。这些继发性肿瘤导致大约90%的癌症患者死亡。传播癌细胞的一个重要途径是通过淋巴系统,淋巴系统像血管系统一样贯穿整个身体并将淋巴结彼此相互连接在一起。当白细胞通过淋巴系统迁移以便协调对抗病原体的防御时,作为一种特定的膜蛋白,趋化因子受体7(CCR7)起着重要作用。它位于细胞膜中,它可以接收外部信号并将这些信号传递到细胞内部。在与罗氏公司的合作中,保罗谢勒研究所的研究人员首次能够解析出CCR7的结构,这就为开发可以阻止某些常见的癌症转移的药物奠定基础。
在所有脊椎动物的细胞中,20种不同的趋化因子受体可与40多种称为趋化因子的信号蛋白相互作用。这些信号蛋白中的每一种仅适合于特定的受体。反过来,如果一种信号蛋白与受体结合,它会触发细胞内的过程,从而导致针对这种信号蛋白携带的信号的特定细胞反应。
CCR7是控制体内细胞迁移的受体之一。一旦细胞外的合适信号蛋白与它结合,细胞中的连锁反应就会使得细胞向这种信号蛋白的最高浓度方向移动。细胞遵循这种趋化因子的轨迹移动,就像追踪某种气味的猎犬。比如,作为身体免疫系统的重要细胞,白细胞源源不断地流向淋巴结。
癌细胞也可以利用CCR7并且为了自身的目的滥用这种细胞受体。合适的信号蛋白将它们引导出肿瘤并进入淋巴系统。此外,它们在体内扩散并最终在其他组织中形成转移瘤。这些转移性肿瘤极大地增加了患者的死亡风险。
为了提高癌症患者的存活率,抑制这种癌细胞转移过程具有重要的医学意义。这就是为什么保罗谢勒研究所研究人员在该研究所的瑞士光源(SLS)上使用X射线晶体衍射技术来解析CCR7受体的结构。
这种结构成为了与罗氏公司合作寻找相应活性试剂的基础。论文共同第一作者Steffen Brünle解释道,“合适的活性试剂分子可以阻止信号蛋白与这种受体结合并在细胞内引起反应。”解析这种受体的结构是一个真正的挑战。论文共同通讯作者、保罗谢勒研究所时间分辨晶体学研究小组联合负责人Jörg Standfuss说,“针对这一点的困难之处在于:首先,以我们能够利用X射线晶体学衍射技术研究它们的方式,培养出相应的晶体。”为了加快研究进程,罗氏公司开发了自己的新型蛋白修饰技术模块,即所谓的结晶伴侣蛋白(crystallization chaperone)。
利用关于这种受体精确结构的信息,他们能够鉴定出5种阻断这种受体的潜在药用分子,比如Navarixin,可阻止信号蛋白携带的信号传递到细胞中。Navarixin是一种多靶标拮抗剂。这5种化合物可作为潜在癌症治疗药物的候选药物。Brünle说,“我们的实验表明,细胞内的这种人工分子与这种受体结合。这阻止了导致细胞迁移的连锁反应的启动。” (生物谷 Bioon.com)
参考资料:
1.Kathrin Jaeger et al. Structural Basis for Allosteric Ligand Recognition in the Human CC Chemokine Receptor 7. Cell, 2019, doi:10.1016/j.cell.2019.07.028.
2.Preventing tumor metastasis
https://medicalxpress.com/news/2019-08-tumor-metastasis.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


