泛基因型丙肝新药!艾伯维Maviret(艾诺全)8周方案获欧盟批准,中国已上市,8周治愈率>99%
来源:本站原创 2019-08-03 14:03
2019年08月03日讯 /生物谷BIOON/ --美国生物技术巨头艾伯维(AbbVie)泛基因型丙肝鸡尾酒疗法Maviret(中文商品名:艾诺全,通用名:格卡瑞韦哌仑他韦,glecaprevir/pibrentasvir)近日在欧盟监管方面传来喜讯。欧盟委员会(EC)已批准Maviret短疗程方案(每日一次,8周),用于既往未接受治疗(初治)、伴有代偿性肝硬化的基因型(GT)1、2、4、5、6慢
2019年08月03日讯 /生物谷BIOON/ --美国生物技术巨头艾伯维(AbbVie)泛基因型丙肝鸡尾酒疗法Maviret(中文商品名:艾诺全,通用名:格卡瑞韦哌仑他韦,glecaprevir/pibrentasvir)近日在欧盟监管方面传来喜讯。欧盟委员会(EC)已批准Maviret短疗程方案(每日一次,8周),用于既往未接受治疗(初治)、伴有代偿性肝硬化的基因型(GT)1、2、4、5、6慢性丙型肝炎病毒(HCV)感染者的治疗。一项来自同一个临床试验的分析正在评估Maviret 8周方案用于初治、伴有代偿性肝硬化的GT3 HCV感染者。目前,Maviret也被批准作为一种8周的泛基因型(GT1-6)疗法,用于无肝硬化的初治患者。
此次批准,基于正在进行的IIIB期临床研究EXPEDITION-8的数据。该研究表明,接受8周Maviret治疗后,GT1、2、4、5、6患者的病毒学治愈率(SVR12)为97.9%。到目前为止,这些患者中没有报告病毒学失败,没有患者因不良事件停止治疗。研究中报告的不良事件(发生率>5%)包括瘙痒(9.6%)、疲劳(8.6%)、头痛(8.2%)和恶心(6.4%)。研究中发生6例严重不良事件(2%),均被认为与glecaprevir/pibrentasvir无关。本研究中未发现任何新的安全信号。这些数据已在美国肝病研究协会(AASLD)组织的2018年肝脏会议(Liver Meeting®2018)上公布。
正在进行的IIIB期临床研究EXPEDITION-8正在评估Maviret治疗所有主要基因型(GT1-6)、伴有代偿性肝硬化的初治慢性HCV患者。该研究已经报告了GT1、2、4、5、6患者(n=280)的数据。GT3患者的入组和治疗完成时间较晚,这一患者群体中的分析正在进行中。
德国法兰克福歌德大学医院医学部主任、医学博士Stefan Zeuzem表示:“目前仍有大量患者和病毒特征不同的HCV患者需要治疗选择。我们正在努力帮助实现世界卫生组织(WHO)的目标,即到2030年消除丙型肝炎病毒(HCV),让更多的患者群体有资格接受短期、8周的治疗选择,将有助于我们更接近这一目标。”
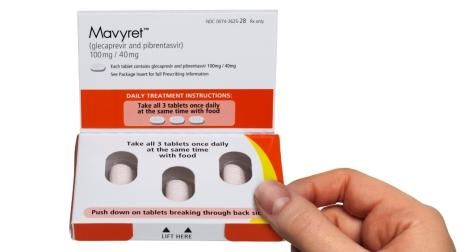
Maviret是一种泛基因型、每日一次、无利巴韦林的治疗药物,由固定剂量的2种独特抗病毒制剂组成,其中glecaprevir(G,100mg)是一种NS3/4A蛋白酶抑制剂,pibrentasvir(P,40mg)则是一种NS5A抑制剂。Maviret每日服药一次,每次3片药物。
Maviret被批准用于青少年(12岁至18岁)和成人治疗所有主要基因型(GT1-6)HCV的感染。Maviret是一种8周泛基因型(GT1-6)疗法,适用于初治、无肝硬化的患者,也适用于初治、伴有代偿性肝硬化的GT1、2、4、5、6患者。在初治、代偿性肝硬化GT3患者中,Maviret推荐的治疗方案为12周疗程。
Maviret也被批准用于治疗具有特殊挑战的患者,包括伴有代偿性肝硬化的所有主要基因型患者,以及以前治疗选择有限的患者,如伴有严重慢性肾脏病(CKD)的患者或GT3患者。Maviret被批准用于所有阶段CKD患者,该药禁止用于重度肝损伤(Child-Pugh C)患者,同时不推荐用于中度肝损伤(Child-Pugh B)患者。
在中国,Maviret(艾诺全)于2019年5月获批,用于治疗全部主要基因型(GT1、2、3、4、5、6)HCV感染的无肝硬化或代偿期肝硬化成人患者。8周治愈丙肝,Maviret凭借"较上市产品有治疗优势"纳入国家局发布的第二批临床急需境外新药名单中。
Maviret临床试验数据显示,对于初治、无肝硬化的所有主要基因型(GT1-6)丙肝患者,病毒学治愈率高达99%以上,疗程可短至8周。该治疗方案无需联合利巴韦林,日服一次。由于不通过肾脏代谢,Maviret适用于任何程度的肾功能损害患者(包括进行透析的患者)且无需调整给药剂量,病毒学治愈率近100%且安全性良好。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


