洪佳旭/蔡宇伽:复旦眼耳鼻喉科医院国内首个基因编辑治疗病毒性角膜炎临床结果出炉
来源:生物世界 2023-09-05 09:39
这些初步临床结果表明,HELP可能是限制人类角膜中HSV-1复制的有效策略,且无明显的CRISPR相关副作用,具有可接受的安全性。
洪佳旭主任医师、蔡宇伽研究员作为共同通讯作者,在 Molecular Therapy 期刊上发表了题为:In Vivo CRISPR Gene Editing in Patients with Herpes Stromal Keratitis 的研究论文。
该研究对3名伴有急性角膜穿孔的严重难治性单纯疱疹病毒性角膜炎(HSK)患者进行了HELP治疗联合角膜移植,并进行了平均18个月的随访。结果显示,3名患者的未发生HSV-1复发,且没有检测到CRISPR诱导的脱靶效应,也未出现全身性不良事件。
这些初步临床结果表明,HELP有望成为一种全新的体内抗病毒疗法,助力体内基因编辑治疗时代的真正到来,为无药可治、有药难治的遗传性、获得性及感染性疾病的患者带来新的希望。

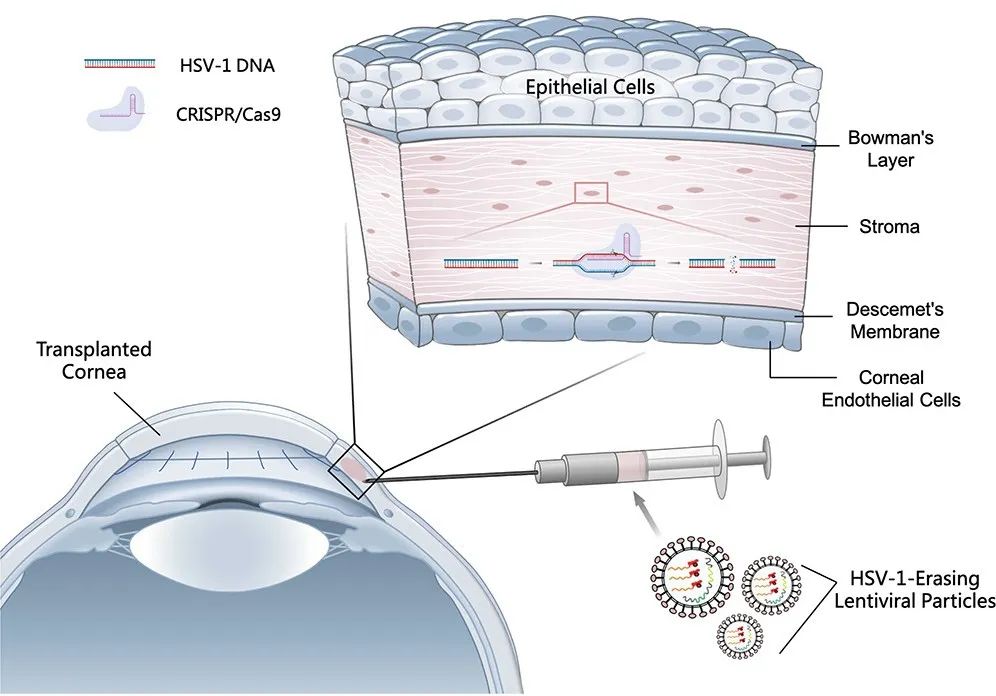
在此前的研究中,蔡宇伽和洪佳旭研究团队使用HELP技术进行了治疗病毒性角膜炎的临床前研究,在急性和复发感染的小鼠模型中实现了从角膜到三叉神经节的逆行运输,将潜藏在神经节的HSV-1病毒库清除。
体内CRISPR基因编辑治疗具有巨大的临床潜力,但其安全性和疗效仍在很大程度上是未知的。在这项研究中,研究团队在角膜移植术中对3例伴有急性角膜穿孔的严重难治性单纯疱疹病毒性角膜炎(HSK)患者的角膜注射了HELP疗法。这是一项在单中心开展的调查性、开放标签、单组、非随机干预性试验(NCT04560790)。
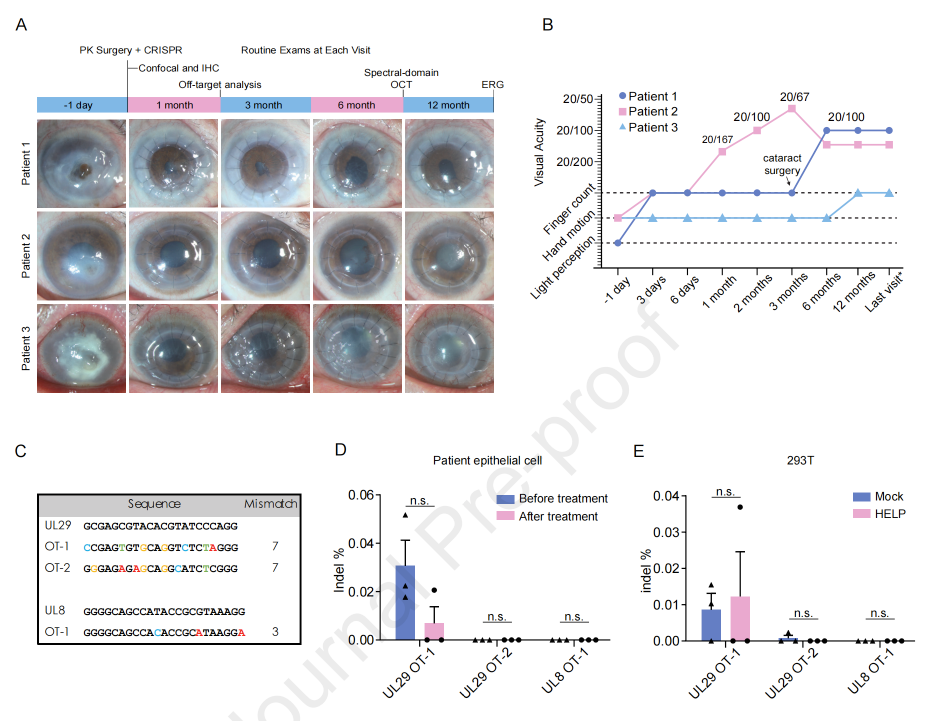
3名患者在HELP治疗后停止了抗病毒治疗,并进行了平均18个月的随访,在末次随访时,他们的角膜移植物和泪液拭子均未见HSV-1病毒复发。
此外,研究团队使用全基因组无偏双链断裂点测序(GUIDE-seq)检测了全基因水平的CRISPR-Cas9系统脱靶情况,结果未发现由CRISPR-Cas9诱导的脱靶DNA断裂。进一步检测未发现注射HELP诱导的载体特异性免疫应答,也未发现其他全身性不良事件。
这些初步临床结果表明,HELP可能是限制人类角膜中HSV-1复制的有效策略,且无明显的CRISPR相关副作用,具有可接受的安全性。该疗法在未来还有望将治疗范围扩大到较轻的单纯疱疹病毒性角膜炎(HSK)患者,以防止他们发展为难治性HSK以及发生角膜穿孔并发症。总的来说,这项研究为体内CRISPR基因编辑作为潜在的抗病毒策略提供了临床概念验证。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


