Biomaterials: 谷氨酸延伸肽抗原和咪唑喹啉TLR7/8激动剂经可电离脂质纳米颗粒共递送可诱导保护性抗肿瘤免疫
来源:网络 2024-07-27 10:16
该研究揭示了谷氨酸延伸肽抗原和咪唑喹啉TLR7/8激动剂经可电离脂质纳米颗粒共递送可诱导保护性抗肿瘤免疫。
当体细胞发生突变,产生新的抗原时,这些新抗原可以通过与MHC-I(主要组织相容性复合体I类)分子结合的肽片段来帮助免疫系统识别并摧毁癌细胞。为了使这些抗原发挥作用,它们首先必须被递送到抗原呈递细胞(APCs)那里。在APCs内部,抗原会被分解成更小的氨基酸序列,也就是所谓的表位,然后这些表位会与MHC-I分子结合,并被运送到细胞表面展示出来,以便被免疫系统的CD8+ T细胞识别。
然而,直接以可溶性形式给予的抗原并不擅长激发强大的CD8+ T细胞反应。这主要是因为两个原因:第一,抗原在淋巴组织中的APCs摄取效率较低;第二,从外部来源来的肽难以有效地通过MHC-I途径呈递给免疫系统。为了解决这个问题,科学家们开发了一种方法,即将抗原包裹在纳米颗粒中,这样可以更有效地将抗原递送到淋巴结(通过皮下或肌肉注射)或脾脏(通过静脉注射),这些地方是免疫系统的关键部位。
纳米颗粒的结构设计(如大小和物理化学特性)对其能否被免疫细胞吞噬至关重要,但通常来说,它们比单纯的可溶性肽更容易被吞噬。此外,纳米颗粒还可以携带额外的分子,称为佐剂,比如Toll样受体(TLR)激动剂,这些分子可以激活APCs的先天免疫反应。有研究表明,激活TLR可以增强MHC-I的抗原呈递能力,同时也能促使APCs分泌更多的共刺激分子和细胞因子,营造一个更加活跃的免疫环境,这能显著提升T细胞对抗原的反应强度和质量。
因此,为了实现更好的治疗效果,研究人员已经研发出了多种纳米颗粒配方技术,包括脂质纳米颗粒、脂质体以及聚合物纳米颗粒,这些技术都在努力提高免疫疗法的效能。

图片来源:https://doi.org/10.1016/j.biomaterials.2024.122693
近日,来自根特大学的研究者们在Biomaterials杂志上发表了题为“CO-DELIVERY of glutamic acid-extended peptide antigen and imidazoquinoline TLR7/8 agonist via ionizable lipid nanoparticles induces protective anti-tumor immunity”的文章,该研究揭示了谷氨酸延伸肽抗原和咪唑喹啉TLR7/8激动剂经可电离脂质纳米颗粒共递送可诱导保护性抗肿瘤免疫。
癌症疫苗旨在产生细胞毒性CD8+ T细胞,杀死癌细胞并使肿瘤持久消退。因此,CD8+肽表位应由抗原呈递细胞呈递到淋巴组织的CD8+ T细胞。不幸的是,在未配制的可溶性形式下,肽抗原很难被抗原呈递细胞吸收,不能有效地到达淋巴结。因此,缺乏有效的递送仍然是使用肽抗原的癌症疫苗成功临床翻译的主要限制。
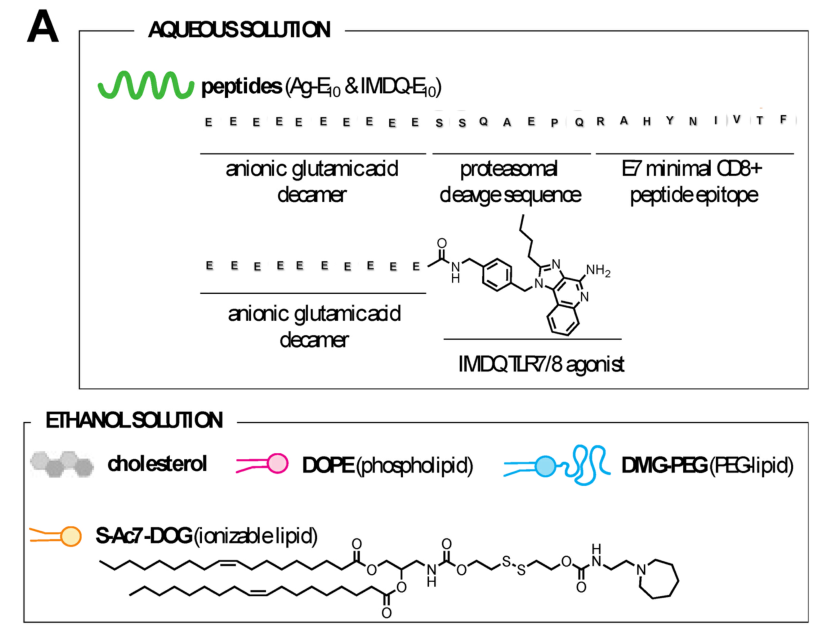
Peptide-LNP设计
图片来源:https://doi.org/10.1016/j.biomaterials.2024.122693
在本研究中,研究者提出了一种通用的肽纳米配方策略,通过延长肽抗原表位的氨基酸序列与10个谷氨酸残基。由此产生的肽的整体阴离子电荷允许通过与可电离的阳离子脂质静电相互作用封装成脂质纳米颗粒(肽- lnp)。
研究者证明静脉注射肽- lnp有效地将肽递送到脾脏的免疫细胞。共包被一种咪唑喹啉TLR7/8激动剂(IMDQ)的肽- lnp可在脾脏广泛的免疫细胞亚群中诱导强大的先天免疫激活。Peptide-LNP含有hpv16型E7癌蛋白和IMDQ的最小CD8+ T细胞表位,可诱导血液中高水平的抗原特异性CD8+ T细胞,并可在预防和治疗环境中赋予对表达E7的肿瘤的保护性免疫。
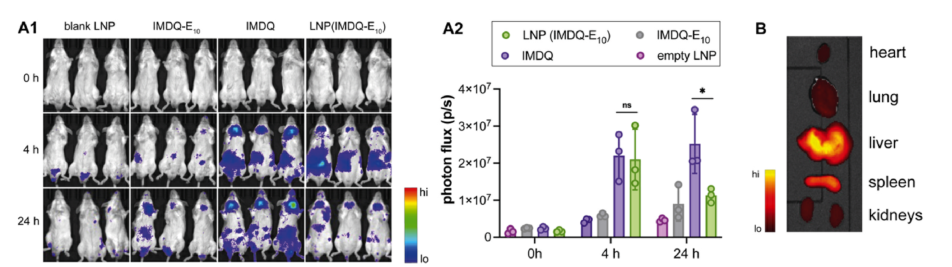
LNP(IMDQ-E10)在体内诱导细胞因子的产生
图片来源:https://doi.org/10.1016/j.biomaterials.2024.122693
总之,研究者提出了一种简单而有效的方法,将肽抗原和咪唑喹啉TLR7/8激动剂制备成LNPs。研究者的策略是基于用10个谷氨酸残基扩展肽表位。后者使肽具有整体阴离子电荷,允许在乙醇-水溶剂交换过程中与可电离的阳离子脂质静电相互作用形成LNPs。
静脉注射LNPs被脾脏的抗原呈递细胞吸收,TLR7/8激动剂在脾细胞中诱导广泛激活。抗原和TLR7/8激动剂的共同递送在初始增强免疫后产生强大的抗原特异性CD8+ T细胞反应,并在预防和治疗环境中提供针对表达抗原的肿瘤攻击的保护性免疫。
本研究的LNP方法对不同货物的包封具有灵活性,这些货物塑造了免疫反应的幅度和质量,并对靶向特定免疫细胞亚群的表面修饰具有灵活性。(生物谷 Bioon.com)
参考文献
Tingting Ye et al. CO-DELIVERY of glutamic acid-extended peptide antigen and imidazoquinoline TLR7/8 agonist via ionizable lipid nanoparticles induces protective anti-tumor immunity. Biomaterials. 2024 Jun 27:311:122693. doi: 10.1016/j.biomaterials.2024.122693.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


