Mol Cancer:肿瘤抑制因子LKB1/STK11的缺失可用于靶向癌症治疗
来源:生物谷原创 2024-09-28 14:17
该研究揭示了lkb1缺陷肿瘤的关键代谢脆弱性,可用于靶向癌症治疗。
肺腺癌(LUAD)是最常见的人类肺癌类型,属于非小细胞肺癌(nsclc)的范围。LUAD是全球癌症相关死亡的主要原因,约占肺癌病例的40%。目前LUAD的治疗方法包括手术切除、化疗、放疗和靶向治疗,其中靶向治疗在治疗具有可识别的驱动性致癌事件的患者方面具有显著优势。然而,尽管肺癌治疗在过去几十年取得了进展,但预后仍然特别差,5年生存率仅为15-20%,而远处转移患者的生存率约为8%。
在分子水平上,在几种恶性肿瘤中观察到LKB1肿瘤抑制因子(也称为STK11)的缺失,值得注意的是,包括超过30%的人类luad。事实上,LKB1是luad中第三常见的突变基因,经常与致癌基因TP53和KRAS共存。LKB1是一种丝氨酸苏氨酸激酶,包括主要细胞能量传感器amp活化激酶(AMPK)的主调节因子,它通过磷酸化激活AMPK,以及其他12种AMPK相关激酶。
在低能量条件下,如饥饿,活性AMPK使哺乳动物雷帕霉素(mTOR)靶蛋白处于封闭状态,阻止细胞进一步增殖和生长。考虑到AMPK在几乎所有肿瘤发生病例(约99%的人类肿瘤,图S1A)中保持遗传完整,mTOR激活需要丢失AMPK阳性调节因子(如LKB1)是合理的。
然而,LKB1肿瘤表现出一种高代谢表型,通过诱导丝氨酸-甘氨酸碳途径偶联s -腺苷蛋氨酸生成。在斑马鱼中,lkb1突变体对代谢应激和能量储备过早耗尽表现出缺陷反应。治疗利用肿瘤抑制突变是间接可能的,当他们赋予特定的依赖于癌细胞。T肿瘤细胞经常在营养不良和缺氧的环境下进行基本的代谢变化以满足其增加的能量需求。事实上,癌细胞的重组代谢被认为是癌症的致命弱点。然而,伴随LKB1丢失的代谢特征改变是否可以作为治疗LKB1肿瘤的机制迄今尚未得到解决。

图片来源:https://doi.org/10.1186/s12943-024-02061-4
近日,来自雅典国立和卡波迪斯特里安大学的研究者们在Mol Cancer杂志上发表了题为“Loss of the tumour suppressor LKB1/STK11 uncovers a leptin-mediated sensitivity mechanism to mitochondrial uncouplers for targeted cancer therapy”的文章,该研究揭示了lkb1缺陷肿瘤的关键代谢脆弱性,可用于靶向癌症治疗。
非小细胞肺癌是最致命和最常见的恶性肿瘤之一。LKB1/ STK11肿瘤抑制因子在约30%的非小细胞肺癌(典型的肺腺癌(LUAD))中发生突变。研究者将斑马鱼和人类肺类器官作为协同平台,对选择性靶向lkb1缺陷肿瘤的代谢化合物进行临床前筛选。有趣的是,两种激酶抑制剂piceatanol和Tyrphostin 23似乎对LKB1突变具有合成致死性。虽然LKB1的损失加速了能量消耗,但研究者意外地发现,它还改变了关键能量稳态维持参与者LEP的调节,进一步增加了能量负担,暴露了一个脆弱点;获得对已鉴定化合物的敏感性。
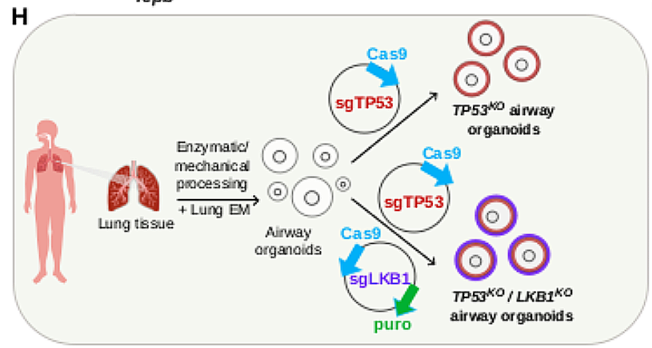
通过CRISPR/ cas9介导的基因组编辑获得克隆TP53KO或TP53KO/LKB1KO ao的实验策略示意图
图片来源:https://doi.org/10.1186/s12943-024-02061-4
研究者发现,复合治疗通过拮抗Von Hippel-Lindau (VHL)介导的HIF1A泛素化来稳定缺氧诱导因子1- α (HIF1A),从而驱动LEP过度激活。重要的是,研究者证明了在已经受到lkb1缺陷的细胞中,对皮杉醇/tyrphostin 23的敏感性在上位性上依赖于hif1a - lep解偶联蛋白2 (UCP2)信号轴,该信号轴降低了细胞能量,使其无法存活。因此,研究者发现了lkb1缺陷肿瘤的关键代谢脆弱性,可以使用本研究鉴定的化合物作为线粒体解偶联剂进行治疗。
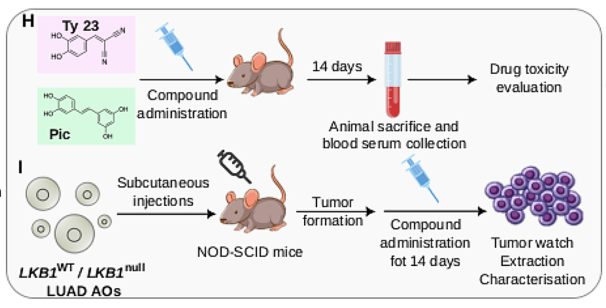
小鼠给药示意图,以确定潜在的毒性作用
图片来源:https://doi.org/10.1186/s12943-024-02061-4
综上所述,本研究阐明了LKB1缺陷细胞的关键代谢脆弱性的分子机制,这可以很容易地利用来对抗LKB1肿瘤的发生。通过使用精准医学模型系统,研究者揭示了一种新的信号通路,该通路赋予了对已鉴定的线粒体解偶联剂的易感性,并在没有实质性毒性的情况下消除了LKB1肿瘤负担。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


