“复必泰”临床试验再度被延!“争相竞技”的国产mRNA疫苗谁能突出重围?
来源:生物探索 2022-05-18 18:03
根据全球权威的临床试验登记网站ClinicalTrials.gov网站显示,“复必泰”中国Ⅱ期临床试验的预计结束日期延期至10月30日。
根据全球权威的临床试验登记网站ClinicalTrials.gov网站显示,“复必泰”中国Ⅱ期临床试验的预计结束日期延期至10月30日。这项由BioNTech公司登记的Ⅱ期临床试验于2020年12月启动,试验共入组950人,主要研究疫苗在中国大陆健康人群中的安全性,原计划于2021年12月结束,后延期至今年4月30日,如今却再度被延期半年!
去年7月,复星医药董事长吴以芳曾表示,疫苗的“审定工作基本完成,正在加紧进行行政审批”,这一度被业内视为复必泰即将上市的信号。今年3月,吴以芳再度回应复必泰的上市进展时,态度则略显保守,回应称“还在审批,没有更多的消息。”然而,此次再度传出的临床延期消息,让“复必泰”在大陆地区上市蒙上阴影(图1)。
图1 复必泰的国产化之路(图源:生物探索编辑团队原创)
一直以来,这款mRNA疫苗的商业价值是有目共睹的。正是凭借此款疫苗产品,辉瑞公司在2021年度实现了高达367.8亿美元的总营收,重新夺回全球制药Top1的宝座;此外,根据最近的Q1财报,辉瑞在2022年第一季度也实现了132.3亿美元的高营收,远远高于上年度同期水平(相关阅读:重夺全球制药Top1?从年度财报看这家公司的实力)。在辉瑞赚得盆满钵满之际,然而复必泰仅在我国港、澳、台三地投入使用。在2021年报中,虽然复星医药并未披露复必泰在港澳台地区的具体营收,但在制药板块销售规模超10亿的3种产品当中,复必泰占据首位,使其一举成为复星医药三大超10亿营收的龙头产品。
此前任何一点风吹草动都能引发市场对于复必泰获批的期盼,而复星医药也多次表示早已为复必泰上市做好随时待命的准备。尽管市场翘首以盼,复星医药也已随时待命,复必泰上市的消息至今仍未能等到。如今Ⅱ期临床试验再度延期,似乎上市更是前路漫漫。
mRNA疫苗作为一种通过体外转录构建的核酸疫苗,可将病毒无害的小片段呈现给免疫细胞“学习”并“演练”如何识别和攻击病毒,在下次“真枪实战”时可快速产生特异性免疫反应,从而防止病毒在人体复制和传播(图2)。mRNA疫苗具备无病毒感染风险、研发周期短和拥有双重免疫机制等突出优势。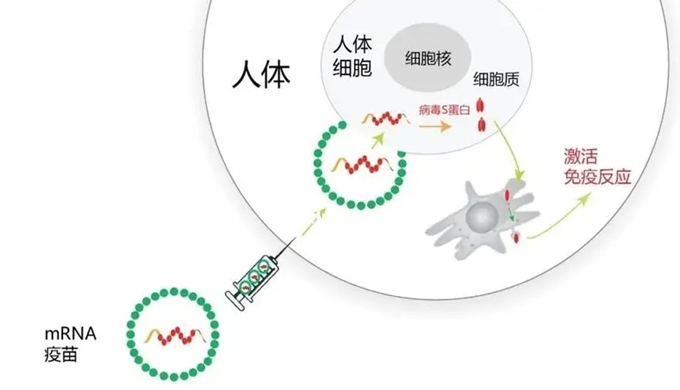
图2 mRNA疫苗的作用机制(图源:健康界)
近年来,国内企业对布局mRNA技术路线保持如此高的热情,不单单是因为辉瑞、莫德纳两家巨头的mRNA产品获得全球市场的优异反馈,更是考虑到mRNA新冠疫苗基础免疫的保护效力临床数据表现优异,三针加强针后对变异株的保护力也有明显提升,超越其他技术路线的新冠疫苗。对此,张文宏教授和钟南山院士都曾公开表达过此观点。
3月24日,华山医院感染科主任张文宏教授发微博称,“根据香港疫苗有效性数据,灭活疫苗和mRNA疫苗都可以预防严重疾病和死亡。在年龄≥60岁的成人中,灭活冠状病毒两针接种对重症新冠与死亡的保护率为74.1%,但仍不如BNT162b2(有效率88.2%)。”
4月,在钟南山院士为南开学子公开授课《科学指导抗疫,勇攀医学高峰》时,分享了在巴西开展的异源性疫苗接种的真实世界数据。数据显示,两针科兴疫苗,再用mRNA疫苗加强免疫14-30天后,预防感染率可高达92.7%,预防重症达97.3%(图3)。
图3 钟南山院士公开授课(图源:[2])
据统计,国内聚焦mRNA药物研发的创新企业有十余家,主要有艾博生物、丽凡达生物、蓝鹊生物、斯微生物等(表1)。值得一提的是,在这其中斯微生物是国内最早致力于mRNA技术的制药公司,其他聚焦mRNA领域的公司多成立于2018年以后。
表1 国内聚焦mRNA药物研发的创新企业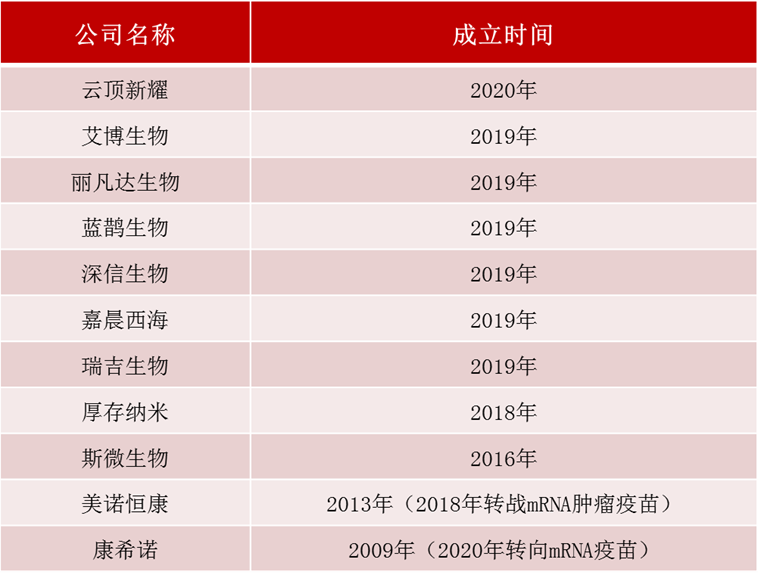
数据来源:[1]丨制表:生物探索编辑团队
注:美诺恒康虽成立于2013年,但该公司最初创立时主营外包服务,于2018年开始转战研发mRNA肿瘤疫苗。成立于2009年的康希诺,自2020年开始转向mRNA疫苗研发。
目前,国内暂无mRNA疫苗获批上市。据不完全统计,截至目前,国内已有7家企业的mRNA疫苗候选药物进入临床阶段,其中5款已处于I和II期临床试验阶段,2款获得国家药监局的IND审批,即将进入临床阶段,具体进展可见表2。
表2 国内新冠mRNA疫苗研发临床进展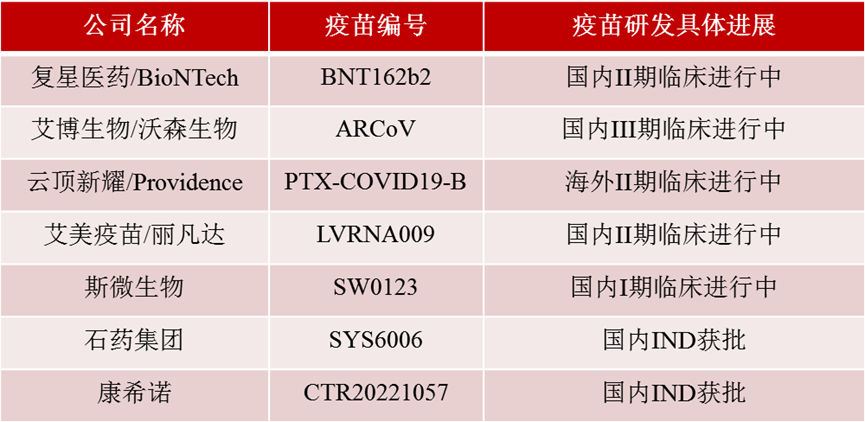
数据来源:[1]丨制表:生物探索编辑团队
艾博生物&沃森生物(ARCoV)
2019年,艾博生物在苏州成立,致力于基于核酸(siRNA,mRNA,DNA)的新药研发。2020年6月,艾博生物联合军事科学院军事医学研究院、云南沃森生物共同研制的新型冠状病毒mRNA疫苗(ARCoV),正式获得IND批准,进入临床I期研究阶段。
2022年1月24日,《柳叶刀-微生物》刊登了浙江大学医学院附属第一医院李兰娟院士团队对mRNA疫苗ARCoV的安全性、耐受性和免疫原性研究,正式公布这款新冠mRNA疫苗ARCoVaX(ARCoV)的I期临床试验数据。该项题为“Safety and immunogenicity of the SARS-CoV-2 ARCoV mRNA vaccine in Chinese adults: a randomised, double-blind, placebo-controlled, phase 1 trial”的研究数据显示,ARCoV在所有五组剂量下安全性耐受性良好,并可诱导强烈的免疫反应(图4)。
图4 研究成果(图源:[3])
云顶新耀&Providence(PTX-COVID19-B)
2021年9月,云顶新耀宣布与Providence Therapeutics公司达成合作,获得Providence公司的mRNA新冠候选疫苗在大中华区、东南亚、巴基斯坦等亚洲新型市场的授权许可,同时也引进Providence的mRNA技术平台,在全球进一步合作开发mRNA产品。公司获得mRNA疫苗整个制造过程的全部技术转让。
2021年5月,Providence宣布了I期临床的中期数据。I期临床数据显示,接受过PTX-COVID9-B治疗的受试者的血清在第28天显示出中和活性,而接受安慰剂治疗的受试者均未产生中和抗体。在第二次注射两周后,中和抗体滴度随着剂量的增加和时间的推移而增加。第42天的中和效价比新冠康复患者的中和水平高出10倍以上。
2021年12月,云顶新耀与Providence Therapeutics共同宣布,PTX-COVID19-B已加入世界卫生组织的新冠疫苗团结试验(Solidarity Trial Vaccines)(图5)。目前,PTX-COVID19-B正处于全球II期临床试验阶段。此外,云顶新耀和Providence还合作开发针对Omicron的下一代mRNA疫苗。
图5 WHO组织的新冠疫苗团结试验(图源:[4])
艾美疫苗&丽凡达(LVRNA009)
成立于2019年,艾美疫苗控股子公司丽凡达生物公司自主开发的mRNA基因制药平台多线推进传染病疫苗、癌症疫苗、蛋白补充治疗等一系列创新型生物药的研发、生产和上市,拥有自主mRNA生产和药物递送技术平台,在药物设计、生产和制剂递送方面已拥有多项发明专利。
2021年3月,艾美疫苗控股子公司丽凡达开发的新冠mRNA疫苗(LVRNA009)获得IND批准。2022年1月8日,LVRNA009的I期临床试验数据显示,总的不良事件发生级别都为1-2级,没有发生3级以上的不良事件,因此LVRNA009具备良好的安全性和耐受性。3月,丽凡达启动新冠mRNA疫苗的II期临床试验,旨在评估该疫苗在中国18-59岁人群中接种的免疫原性和安全性。
斯微生物(SW0123)
2016年,斯微生物由海归科学家创立,其致力于打造中国领先的mRNA药物平台和产品管线。2017年7月,休斯顿卫理会医院授予斯微生物在LPP(lipopolyplex)递送平台的全球独家商业化权益。
目前,斯微生物针对野生株的第一代mRNA疫苗I期临床试验已经结束,数据显示安全性良好。针对变异株的二代新冠mRNA疫苗在老挝正开展I/II期临床试验;此外,斯微生物已经获得巴西的临床I期、II期、III期的批件。根据初步动物实验,这款疫苗对于Delta、Beta等变异株都具有非常好的保护效果。
注:LPP纳米递送平台是一种以聚合物包载mRNA为内核、磷脂包裹为外壳的双层结构。LPP的双层纳米粒和传统的LNP相比具有更好的包载、保护mRNA的效果,并能够随聚合物的降解逐步释放mRNA分子。
石药集团(SYS6006)
SYS6006为石药集团自主研发的、针对新冠病毒变异毒株的mRNA疫苗。通过针对性的抗原突变设计,临床前研究表明其对包含Omicron和Delta在内的主流突变毒株都具有良好的免疫保护效力,通过体液免疫和细胞免疫对机体提供免疫保护,并可产生记忆B细胞,提供长效保护力。此外,安全性方面也得到临床前安全性评价数据证明。2022年4月4日,石药集团生产的mRNA疫苗SYS6006获得国家药监局IND批准。
此外,SYS6006使用先进的生产技术,产业化能力强,稳定性好,可在2-8°C长期储藏。此外,在供应链上,公司对mRNA技术的关键生产原料和辅料实现了内化生产和国产化替代,可满足大规模产能供应需求。基于综合优势,SYS6006被NMPA列入特别审批程序,被快速批准进入临床。后续公司将全力推进该产品的国内及国际多中心临床研究工作,力争尽快上市。
康希诺(CTR20221057)
2009年,康希诺成立于天津,致力于为中国及全球公共卫生研发、生产和商业化创新疫苗。公司现有四个创新疫苗平台技术,包括腺病毒载体疫苗技术、结合技术、蛋白设计与重组技术、制剂技术。公司在mRNA合成和递送技术上布局多年,已申请多项关于mRNA疫苗设计和新型递送系统设计的专利。
根据临床前结果显示,该款疫苗可以诱导出针对多种WHO认定的重要变异株(包括当前流行株)的高滴度的中和抗体,与以原型株为基础开发的现有新冠疫苗相比广谱性更强,可以更为有效保护机体免受现有变异株的感染。
2021年年底,康希诺生物与上海医药合作建设的mRNA疫苗生产厂房完成交付,并获得上海首张新冠疫苗生产许可证,预计今年年底前将具备大规模商业化生产条件。2022年4月4日,公司生产的mRNA疫苗获得国家药监局IND批准。5月5日,康希诺登记启动了新冠mRNA疫苗的I期临床试验,针对18岁及以上成年人,试验登记号为:CTR20221057。
综上,由于mRNA疫苗所具有的独特技术优势,以及它在免疫保护方面的优越性,我国民众一直对mRNA翘首以盼。目前,我国多家企业也正纷纷布局mRNA技术平台,投入到mRNA疫苗的研发中。小编相信在此种争相竞技的氛围下,我们将接连见证新的突破,早日见证国产mRNA疫苗实现“零”的那一天!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


