Gut | 海军军医大学廖专/邹文斌开发改善慢性胰腺炎的新方法
来源:生物探索 2024-04-08 10:26
该研究首次证明AAV8-hSPINK1介导的基因治疗胰腺炎具有较高的转导效率和安全性。使用衣壳优化的AAV8载体有效准确地将hSPINK1基因传递到胰腺细胞中,对其他关键器官表现出低趋向性。
海军军医大学廖专及邹文斌共同通讯在Gut(IF 25)在线发表题为“Pancreas-directed AAV8-hSPINK1 gene therapy safely and effectively protects against pancreatitis in mice”的研究论文,该研究表明胰腺导向的AAV8-hSPINK1基因治疗安全有效地改善小鼠胰腺炎。结果表明,构建的AAV8-hSPINK1载体特异性安全靶向胰腺,对心、肺、脾、肝、肾的器官趋向性低,转导效率高(最佳表达剂量为2×1011 vg/只)。
hSPINK1的表达和疗效在注射后4周达到峰值,并保持显著水平至少8周。在所有三种小鼠模型中,发病前单剂量AAV8-hSPINK1显著减轻了胰腺炎的严重程度,减缓了纤维化的进展,降低了胰腺细胞凋亡和自噬水平,加速了胰腺炎的恢复过程。总之,一次性注射AAV8-hSPINK1安全靶向胰腺,转导效率高,可有效改善小鼠胰腺炎表型。该方法在预防和治疗CP方面具有广阔的前景。

慢性胰腺炎(CP)是一种由遗传和环境因素引起的终身进行性纤维炎性疾病。其特征是腹痛,急性胰腺炎(AP)反复发作,胰腺功能随着时间的推移而恶化,导致患者生活质量显著下降CP患病率为每10万人13.5至52.4例,在过去二十年中稳步上升,造成了很高的疾病负担CP也会显著增加患胰腺癌的风险。遗憾的是,目前还没有根治CP的方法迫切需要有效的治疗和疾病预防策略。
丝氨酸蛋白酶抑制剂Kazal 1型(SPINK1)编码胰腺分泌性胰蛋白酶抑制剂(PSTI),是与胰腺炎相关的主要基因之一。SPINK1/PSTI在胰腺腺泡细胞中合成,被认为是通过抑制过早激活的胰蛋白酶来抵抗胰腺炎的第一道防线SPINK1基因的失功能突变破坏了胰蛋白酶激活和抑制之间的平衡,促进了胰腺炎的发生和发展。在西方国家,携带SPINK1 c.101A>G (p.Asn34Ser)变异的最常见单倍型mRNA表达量低于野生型,CP风险增加10倍。
在亚洲,SPINK1的功能丧失变异(以C .194+2T > C为代表)在CP患者中占主导地位,约占中国CP队列的30%,并且与东亚(OR=73.16)和非东亚(OR=10.21)人群中罹患CP的风险增加显著相关。动物实验也支持这些发现。例如,在Spink1(也称为Spink3)纯合缺陷小鼠中,胰腺细胞发生自噬变性,导致出生后2周内死亡。与此一致的是,纯合子SPINK1缺乏的个体在大约5个月大时表现出严重的外分泌胰腺功能不全。此外,之前的研究发现杂合Spink1 C .194+2T>C突变小鼠发生自发性胰腺损伤。
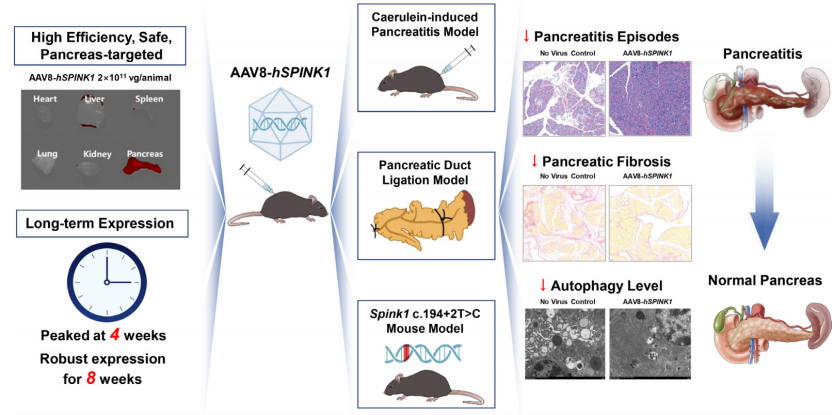
AAV8-hSPINK1介导的三种小鼠胰腺炎基因治疗模式(Credit: Gut)
鉴于上述证据,外源性胰蛋白酶抑制剂可能有利于胰腺炎的预防和治疗。事实上,胰蛋白酶抑制剂如抑酶蛋白、卡莫司他、那莫司他和加贝酸酯已经在各种胰腺炎动物模型中进行了研究。此外,甲磺酸那莫他酯和甲磺酸加贝酸酯已在临床上用于预防内镜逆行胆管造影引起的胰腺损伤,或治疗儿童AP另一种策略是发展表达大鼠或人胰蛋白酶抑制剂基因的转基因小鼠。基因过表达的人SPINK1 (hSPINK1)能够持续抑制活性胰蛋白酶,为治疗CP提供了一种新的方法。然而,要承认,为这一目的修改人类基因目前面临着伦理障碍。因此,迫切需要一种安全有效的基因替代治疗载体。
综上所述,该研究首次证明AAV8-hSPINK1介导的基因治疗胰腺炎具有较高的转导效率和安全性。使用衣壳优化的AAV8载体有效准确地将hSPINK1基因传递到胰腺细胞中,对其他关键器官表现出低趋向性。该研究明确地证明了AAV8-hSPINK1载体在胰腺中的高特异性和安全性。在三种模型(即小粒蛋白诱导的胰腺炎模型、胰管结扎模型和Spink1 C .194+2T>C突变模型)中,单剂量AAV8-hSPINK1治疗小鼠一致表现出AP和CP进展的显著缓解。该疗法的有效性已在多种胰腺炎小鼠模型中得到证实,为基因治疗策略成功治疗临床胰腺炎提供了临床前实验证据。需要进一步探索AAV8-hSPINK1在大型动物和非人灵长类动物模型中的可行性和有效性。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


