Dev Cell | 陈海洋团队揭示极长链脂肪酸作为信号分子调控肠道干细胞中的过氧化物酶体稳态和肠道损伤修复过程
来源:生物探索 2024-08-01 09:28
这项研究深入探讨了肠道损伤后调节干细胞内过氧化物酶体数量动态变化的详细机制,揭示了VLCFAs作为信号分子在此过程中的关键角色。
肠道是人体与外界环境直接接触的关键器官,时刻抵御着有害物质和病原体的侵袭。得益于其内在的干细胞系统,肠道具备了非凡的自我修复能力。尽管如此,肠道干细胞(intestinal stem cell,ISC)是如何感应到损伤信号,并从静息状态迅速激活,进而通过增殖和分化来修复受损肠上皮组织,目前科学界对此尚缺乏全面的理解。四川大学华西医院陈海洋团队的研究发现,在肠道受损时,肠道干细胞中的过氧化物酶体(Peroxisome)数量显著上升,并通过调节JAK-STAT-SOX21信号通路,促进干细胞分化,对肠道的修复过程起到调控作用【1】。然而,ISCs中的过氧化物酶体如何响应肠上皮损伤信号,以及其数量如何在损伤修复过程中发生动态变化,这些机制仍有待进一步阐明。
四川大学华西医院陈海洋团队再次在Developmental Cell杂志上发表了题为Very long-chain fatty acids control peroxisome dynamics via a feedback loop in intestinal stem cells during gut regeneration 的研究。该研究揭示了肠道损伤后,肠道内的极长链脂肪酸(Very long-chain fatty acids,VLCFAs)含量上升,并作为关键信号分子,通过激活过氧化物酶体增殖体激活受体(peroxisome proliferator-activated receptors,PPARs)与SOX21转录因子之间的负反馈机制,精确调控ISC内过氧化物酶体的动态平衡。这一发现为理解ISC在肠道损伤后的修复机制提供了新的视角。

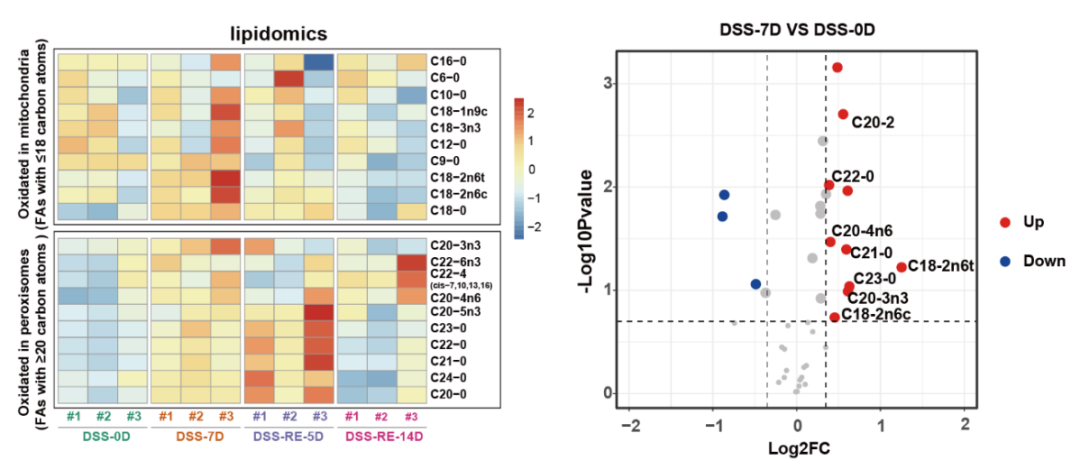
图1.损伤早期(DSS-7D)和修复早期(DSS-RE-5D)肠道中VLCFAs增多(Credit: Developmental Cell)
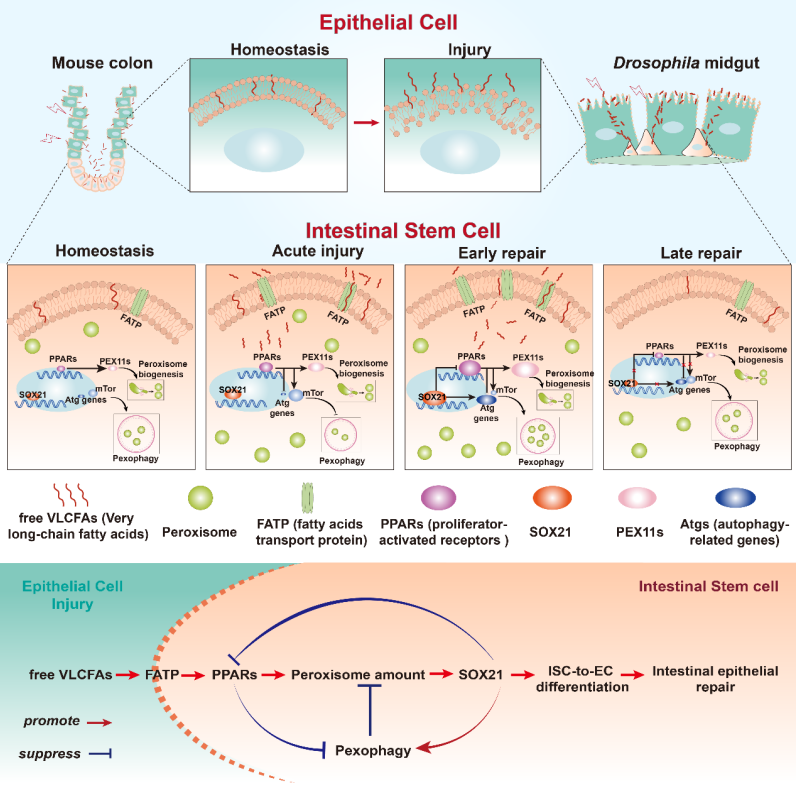
图2.模式图(Credit: Developmental Cell)
参考文献:
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


