Sci Adv:科学家发现帕金森疾病中缺失的关键调节子,有望帮助开发新型靶向性疗法
来源:生物谷原创 2025-02-16 12:23
本文研究取得了重大发现,因为研究人员花费了数年时间在寻找缺失的调节子,重要的是,他们发现了这一关键的调节子,其能开启或关闭LRRK2 GTPase的功能。
LRRK2的突变是帕金森疾病发生最常见的遗传原因,LRRK2蛋白包括两种酶类结构域:一种是GTPase (Roc-COR),另一种则是激酶结构域;致病突变在这两种结构域中都存在。近日,一篇发表在国际杂志Science Advances上题为“CalDAG-GEFI acts as a guanine nucleotide exchange factor for LRRK2 to regulate LRRK2 function and neurodegeneration”的研究报告中,来自康涅狄格大学医学院等机构的科学家们通过研究发现了帕金森疾病遗传原因的又一个新的谜题,这就为开发新型疗法策略提供了新的机遇。
如今,帕金森疾病影响着近100万美国人的健康,尽管多年来科学家们已经知道LRRK2突变对于理解帕金森疾病的发病原因非常重要,但突变是如何导致疾病发生的,以及其背后存在的分子机制,研究人员知之甚少。此前研究者Xiong及其团队发现,在DNA转录成RNA随后表达蛋白的过程中,一种称之为ATIC的酶类及其底物(AICAR)能在mRNA的水平上调节LRRK2的表达,ATIC在帕金森疾病患者中会表现地过度活跃,并能指示LRRK2制造过多称之为震颤素(dardarin)的蛋白。
基于此前研究工作,这项研究中,研究者Xiong等人发现了一种关键的调节子,其或能被用来抑制LRRK2的过度活性。LRRK2拥有两种酶类结构域,即激酶和GTPase结构域,激酶主要负责催化磷酸基团的转移,而GTPase则能在蛋白调节过程中与核苷酸鸟苷三磷酸(GTP)和鸟苷二磷酸(GDP)相结合;文章中,研究人员识别出了维持GTPase功能的关键调节子CalDAG-GEFI (CDGI),其能控制LRRK2 GTPase结合GTP或GDP的开关。
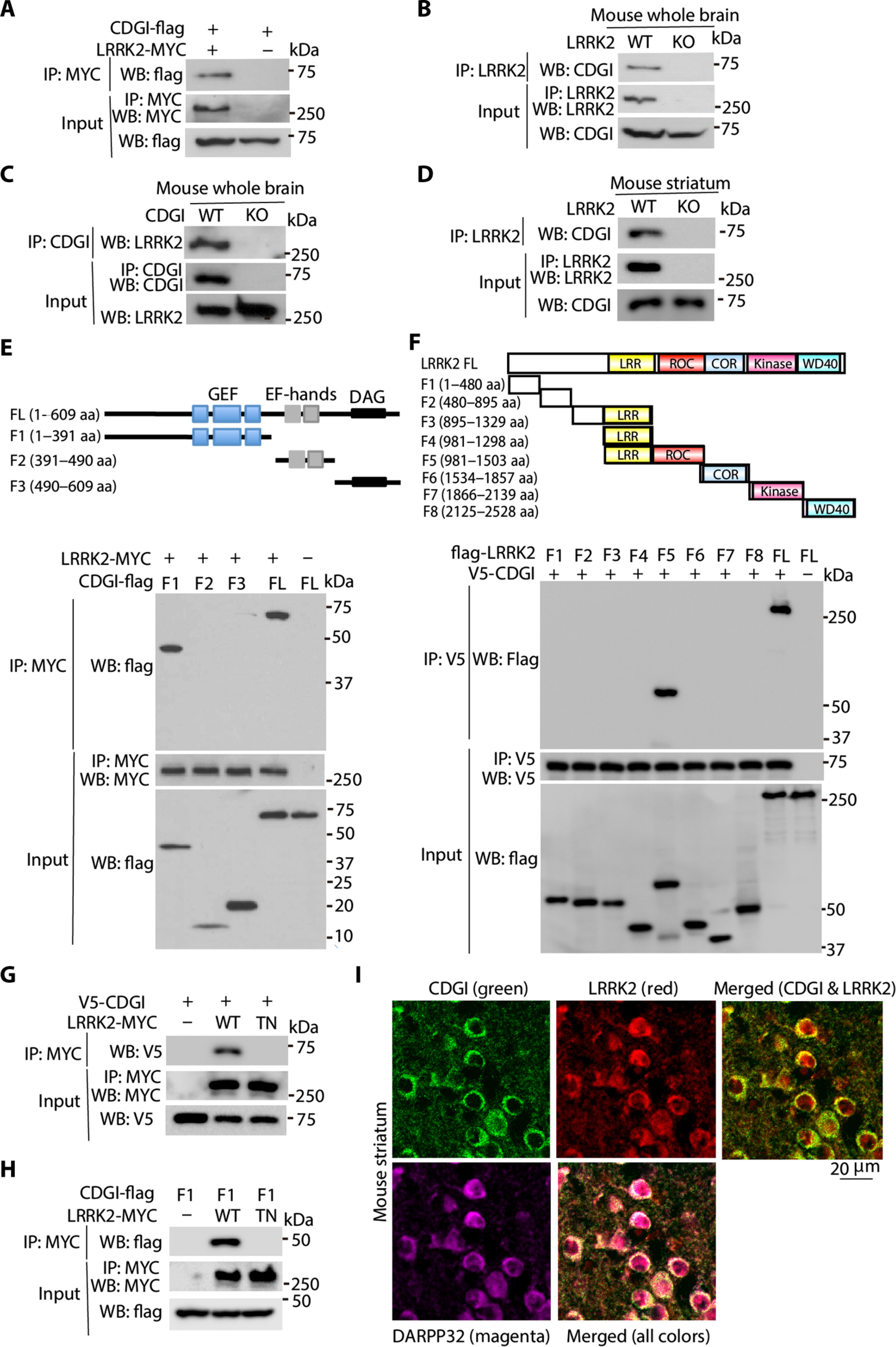
CDGI与LRRK2之间的相互作用
目前大多数研究都集中在理解和靶向作用激酶结构域,因为其要比GTPase更容易成为一种新型的药物靶点,尽管LRRK2 GTPase是帕金森疾病研究的关键靶点,但研究人员很难利用药物来选择性地调节GTPases,此外,作为GTPases结构域的一部分,COR结构域并没有已知的药物能够附着的小分子结合位点。研究者Xiong说道,这或许是一个研究不足的领域,而这一方面的研究工作并不多,本文研究取得了重大发现,因为研究人员花费了数年时间在寻找缺失的调节子,重要的是,他们发现了这一关键的调节子,其能开启或关闭LRRK2 GTPase的功能。如果能抑制这种调节子,科学家们就能阻止震颤素的过度活性从而减缓帕金森疾病的进展。
随后研究人员利用细胞和小鼠模型完成了这项研究,下一步他们将会利用人类样本来继续深入研究;如今研究者Xiong还与一家公司合作基于本文研究结果,共同开发能够穿过血脑屏障从而运输潜在药物的特殊小分子,他们还在深入研究促使这种抑制剂更能靶向作用并调节LRRK2的活性,而研究人员此前发现的抑制剂也能靶向作用LRRK2蛋白的表达。
综上,本文研究中,研究人员识别出了LRRK2的生理性鸟苷酸交换因子(GEFs),并提供了有力的证据表明,LRRK2 GTPase能被GAPs和GEFs所调节,LRRK2 GTPase、GAP或GEF的活性或许能潜在作为治疗性靶点,而这与直接抑制LRRK2激酶不同。(生物谷Bioon.com)
参考文献:
QINFANG LIU,BINGXU HUANG,NOAH GUY LEWIS GUIBERSON, et al. CalDAG-GEFI acts as a guanine nucleotide exchange factor for LRRK2 to regulate LRRK2 function and neurodegeneration, Science Advances (2024). DOI: 10.1126/sciadv.adn5417
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


