CRISPR+类器官,林德晨团队揭示胃食管癌发生发展机制,并发现潜在药物
来源:生物世界 2022-12-05 13:37
这项研究建立了一个研究早期GEJ肿瘤的类器官疾病模型,揭示了早期GEJ肿瘤TP53/CDKN2A失活相关的促癌机制,确定了在GEJ肿瘤发生过程中的关键代谢和表观基因组变化,有助于GEJ肿瘤的早期诊断和


论文通讯作者林德晨研究员(左),论文第一作者Zhao Hua(右)
研究团队从接受上消化道内窥镜检查的患者身上提取正常的人体活检组织,进而创建了GEJ类器官疾病模型。这些类器官由来自干细胞的3D细胞集合组成,这些干细胞可以复制器官的特征或功能。
TP53和CDKN2A是两种重要的抑癌基因,这两种基因的失活会在GEJ肿瘤发生的早期会出现,但由于缺少GEJ特异性疾病模型,TP53和CDKN2A失活在GEJ中的促癌后果尚未被表征。
接下来,研究团队使用CRISPR-Cas9基因编辑技术在GEJ类器官中敲出了这两个关键抑癌基因——TP53和CDKN2A。这两个抑癌基因的双重敲除,会使细胞癌变,让它们生长更快,显微特征也更接近恶性肿瘤。这些基因编辑后的类器官能够在免疫缺陷小鼠中形成肿瘤。
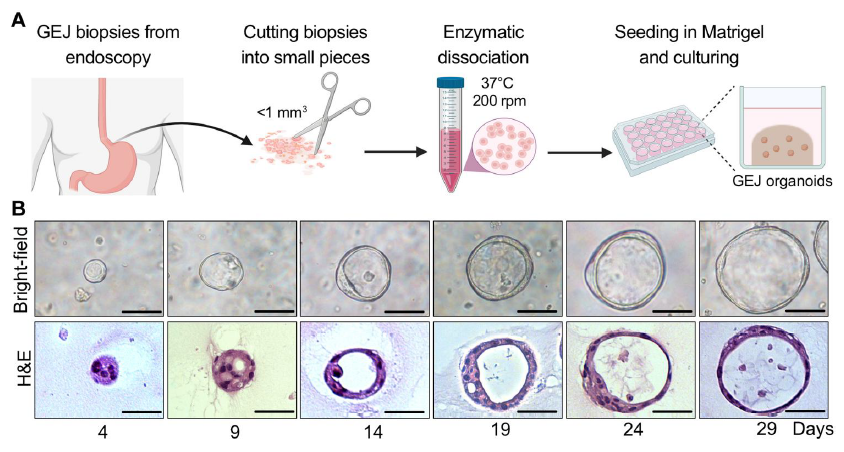
人胃食管结源类器官,利用CRISPR-Cas9基因编辑技术敲除关键抑癌基因TP53和CDKN2A后的人胃食管交界部腺癌类器官
研究团队对基因敲除的GEJ类器官进行的脂质组学分析发现,几种血小板激活因子(PTAF)是上调最多的脂质。血小板随血液循环,当它们识别出受损血管时就会凝结在一起发挥止血作用。
从机制上来说,TP53/CDKN2A双失活,破坏了细胞的转录组和DNA甲基化,这可能是由关键转录因子FOXM1介导。FOXM1通过与血小板激活因子受体(PTFAR)的启动子结合,从而激活PTAFR转录,进一步放大PTAF-PTAFR通路。
接下来,研究团队使用siRNA阻断PTAF-PTAFR,能够在体外抑制TP53/CDKN2A基因敲除的GEJ类器官的细胞增殖以及其他肿瘤学特征。使用WEB2086(这是一种FDA批准的PTAF拮抗剂,用于治疗血小板疾病),能够抑制TP53/CDKN2A基因敲除的GEJ类器官在体内的肿瘤形成。
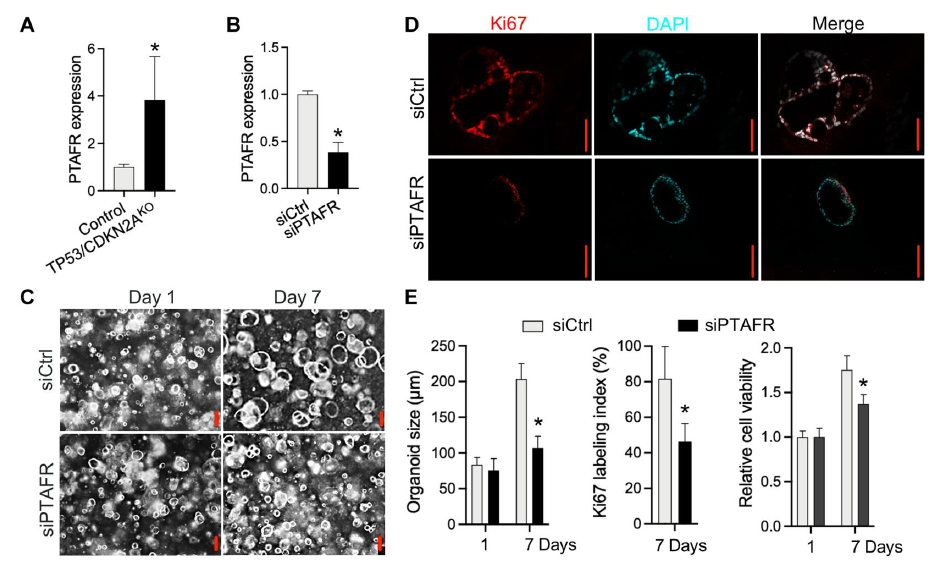
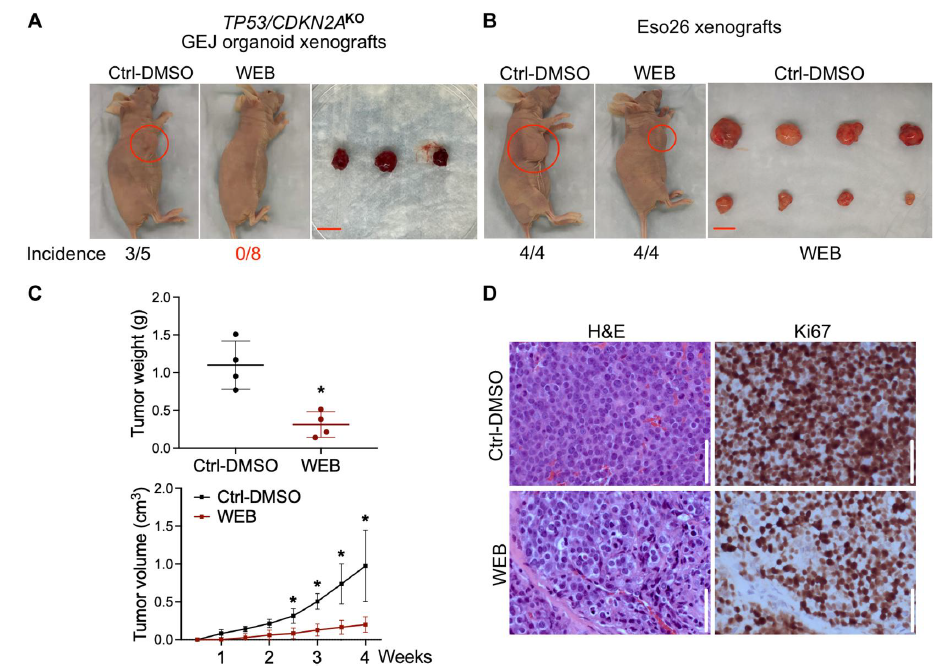
总的来说,这项研究建立了一个研究早期GEJ肿瘤的类器官疾病模型,揭示了早期GEJ肿瘤TP53/CDKN2A失活相关的促癌机制,确定了在GEJ肿瘤发生过程中的关键代谢和表观基因组变化,有助于GEJ肿瘤的早期诊断和预防,并发现了一种潜在的GEJ癌症治疗策略。
研究团队表示,将血小板激活因子(PTAF)抑制剂应用于人类GEJ癌症患者之前,还需要更多研究,但类器官确实有助于加速这些研究。将类器官与CRISPR-Cas9基因编辑技术结合,是研究人类癌症的有效方法。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


