筑起抗癌“鹊桥”!独特2:1抗体结构,让T细胞与癌变B细胞“亲密无间”,治疗B细胞淋巴瘤迎来又一利器丨奇点深度
来源:代丝雨 2022-07-08 18:01
目前,Glofitamab还在进行更多的尝试
笔者小时候,对血液肿瘤的印象≈绝症(都怪电视剧)。严格来说,这种对癌症常规的认知倒也不算特别离谱,从二战浴火而生的化疗,确实在淋巴瘤上遭遇了一些滑铁卢。但是在二十世纪八九十年代之后,淋巴瘤治疗已悄悄发生巨变,其影响之巨,我们今天还在深受荫泽。
那就是CD20的发现。
简单来说,CD20是B细胞的标志表面抗原,几乎表达于B细胞的全生命周期——当然也包括“化身为恶”的各种B细胞性血液肿瘤细胞。更令人欣喜的是,处于B细胞发育最早阶段的未成熟B细胞并不表达CD20,这就意味着,即使抗CD20单抗把正常B细胞和癌细胞一起干掉,B细胞的数量和功能也可通过自身造血功能自然恢复。
简直是太理想不过的抗癌靶点了!
这种设想中的理想药物,其实20多年前就面世了。1997年,全球首个单克隆抗体药物、开启癌症靶向治疗时代的原研利妥昔单抗正式获得FDA批准上市,从实验室走向临床只用了短短7年,这段跌宕起伏充满戏剧性的故事我们早已讲过,就不再赘述了。
利妥昔单抗的出现让淋巴瘤治疗来到了新的时代,与化疗联合的R-CHOP方案至今仍是弥漫性大B细胞淋巴瘤(DLBCL)、滤泡性淋巴瘤(FL)和慢性淋巴细胞性白血病(CLL)的一线治疗选择,而最近十数年中层出不穷的后来者挑战利妥昔单抗的经典地位屡屡受挫。
然而利妥昔单抗并非100%完美,对一线治疗后复发或难治性(R/R)的患者,治疗方案仍有改进的空间,多年来以CD20为靶点的治疗性抗体并未有太大的进展,即使科学家们已经尝试了新的表面抗原、抗体修饰等多种方案,但拿到满意临床效果的屈指可数。
那么我们是不是可以考虑考虑,从另一个角度下手呢?
比如,T细胞?
给T细胞和癌细胞牵红线,大家可能更眼熟的是给T细胞装上瞄准器的CAR-T疗法,其作为一种技术革新性的治疗方法,给疾病领域带来了新的武器和希望。不过这种疗法仍存在不少大规模应用的限制,众所周知,CAR-T细胞需要较长时间的定制化生产,这是病情快速进展的患者难以接受的。而且,当前的CAR-T疗法对临床工作者平衡疗效和不良事件管理的要求也比较高。
除CAR-T外,我们还有一招可以在体内就完成这个过程,那就是使用具有两个不同靶点、可以同时结合T细胞和癌细胞的双特异性抗体,让它们“手牵手”。
这类疗法的先行者是双特异性T细胞衔接器(BiTE)类药物,然而其取消了抗体的可结晶Fc段导致血液循环半衰期较短,同时仍有较明显的细胞因子释放综合征(CRS)相关严重的副作用,即使采取了剂量递增(SUD)使用方式,输注相关反应和中枢神经系统毒性仍然是难以克服的问题[1]。
那么真正全长抗体结构的双特异性抗体(TCB)又如何?不得不说,1:1的经典TCB并不是最优解,半衰期和副反应仍旧是问题。而具有创新性2:1结构的Glofitmab则交出了比较好的答卷。更长的半衰期、更好的疗效、更安全便捷的使用,这都要归功于它独特的“长短手”结构。接下来就让我们看看“长短手”的Glofitamb到底拥有了哪些神奇技能吧。
从图上可以看到,Glofitamab的特别之处在于,作为一个抗体,它的两条臂并不一样,一侧的Fab段是中规中矩的CD20结合位点,而另一侧则是将一个抗CD20 Fab和一个抗CD3 Fab柔性头尾相接,即具有2:1比例的CD20和CD3结合位点[2]。
不用多说,抗CD20 Fab抓牢癌细胞,抗CD3 Fab找T细胞,独特的抗体结构设计使Glofitamab相比1:1结构的TCB具有更强的B细胞抓取能力,可诱导更紧密和稳定的T细胞-癌细胞免疫突触[3]。
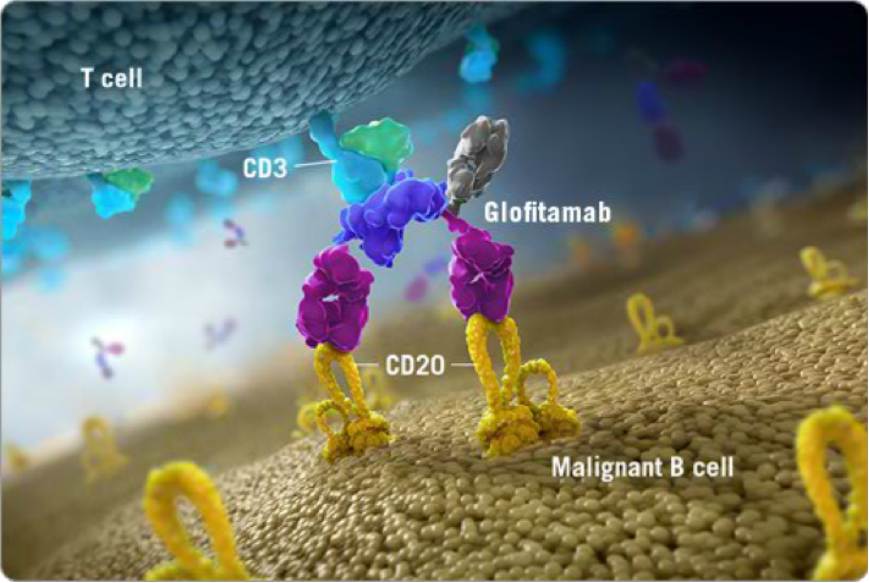
图源[4]
Glofitamab的高超结构不止这一处,Fc段也有巧思。Glofitamab的Fc段选择了一种含有PG LALA突变的人源化IgG1 Fc段[5],这个突变能使Fc段不与人体内的自然杀伤细胞Fcγ受体及补体蛋白C1q结合,同时维持与FcRn(新生儿Fc受体)的结合能力。
Fcγ受体参与抗体依赖性细胞介导的细胞毒性(ADCC)和抗体介导的细胞吞噬反应(ADCP),C1q则参与补体依赖的细胞毒性作用(CDC),也就是说突变的Fc段可以避免这些作用,防止召唤来的T细胞被误杀。FcRn则可以阻止抗体被溶酶体裂解,能够有效延长抗体的半衰期,避免短半衰期带来的必须持续输注给药的困境。
从实验结果来看,Glofitamab的效价是1:1的TCB的40倍,能够以更低的药物浓度达到更好的癌细胞杀伤效果[6]。
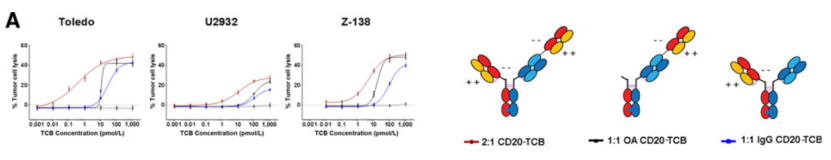
在不同癌细胞系中,2:1都表现出比1:1更佳的效果
值得一提的是,研究者们还提出了一种新的预处理思路,在首次Glofitamab治疗之前使用奥妥珠单抗预处理(Gpt),能够有效地清除B细胞,减少细胞因子释放。
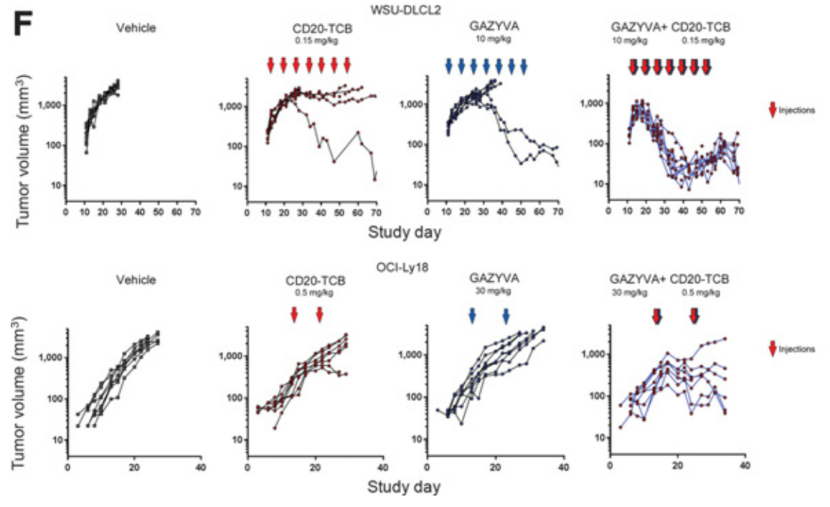
奥妥珠单抗与Glofitamab联用能够取得更好的抗癌效果
Glofitamab的优秀特性在临床研究中也得到了验证。在针对复发或难治B细胞非霍奇金淋巴瘤(R/R B-NHL)的1/2期临床研究NP30179中,Gpt+Glofitamab在不同剂量的组别中均取得了良好的治疗效果,总缓解率达到53.8%,实现完全缓解(CR)的有36.8%,在达到推荐2期剂量的组别中,总缓解率更是达到了65.7%[7]。
63例实现CR的患者中,有53例(84.1%)效果持久,最长达到27.4个月。
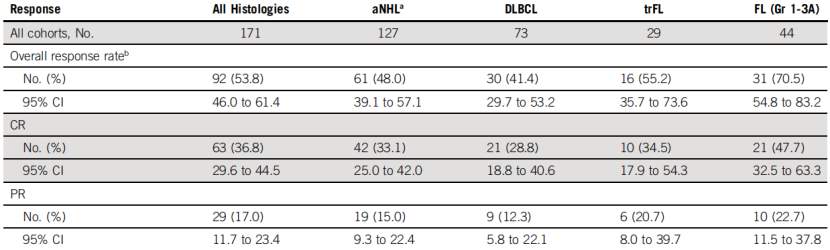
在不同亚型中均取得了一定的治疗效果
特别值得一说的是,Gpt+Glofitamab的方案耐受性良好,大多数不良反应为1-2级, CRS发生率50.3%,仅有3.5%为3-4级。
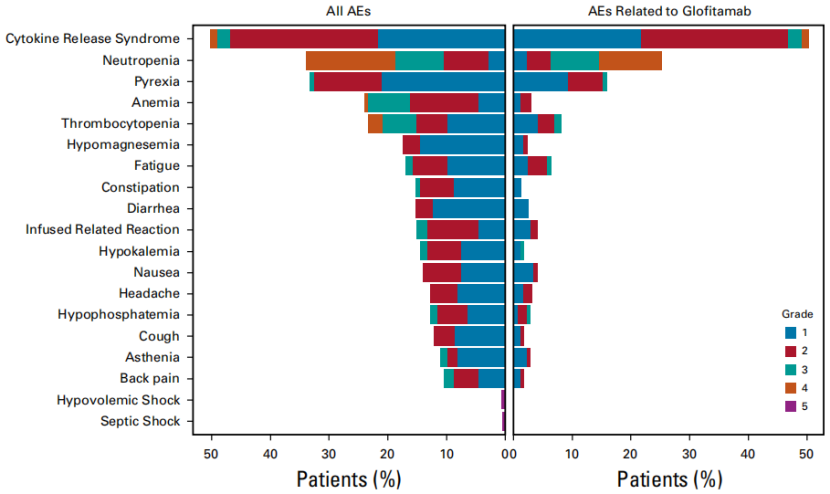
不良反应主要为低级别
EHA2021上则公布了NP30179试验中Gpt+Glofitamab SUD组的数据,随着剂量的增加可明显观察到反应改善的趋势,通过SUD达到了更高的目标治疗剂量(30mg),以期最大化抗肿瘤疗效[8]。
在近期召开的ASCO 2022和EHA2022上,首次公布了Glofitamab治疗既往接受≥2线治疗的R/R DLBCL患者的关键性扩展队列数据,在中位随访12.6个月后,ORR和CR分别达到了51.6%和39.4%,大部分患者(77.6%)在12个月时持续CR,CR中位持续时间未达到[9]。EHA2022上的另一项来自台湾的回顾性分析结果显示,中位9个月随访,患者OR和CR分别达到50%和23%[10]。
目前,Glofitamab还在进行更多的尝试,包括联合R-CHOP的NP40126、联合免疫治疗和ADC的NP39488、在中国开展的YO42610等等,相信严谨科学的临床探索能够让血液肿瘤的治疗不断向前,延续和再创抗CD20靶点的经典传奇。
参考资料:
[1] Viardot A, Goebeler ME, Hess G, Neumann S, Pfreundschuh M, Adrian N, et al. Phase 2 study of the bispecific T-cell engager (BiTE) antibody blinatumomab in relapsed/refractory diffuse large B-cell lymphoma. Blood 2016;127:1410–6.
[2] Bacac M, Fauti T, Sam J, Colombetti S, Weinzierl T, Ouaret D, et al. A novel carcinoembryonic antigen T-cell bispecific antibody (CEA TCB) for the treatment of solid tumors. Clin Cancer Res 2016;22:3286–97.
[3] Klein C, Neumann C, Fauti T, Weinzierl T, Freimoser-Grundschober A, Waldhauer I, et al. Engineering a novel asymmetric head-to-tail 2þ1 T cell bispecific IgG antibody platform (2þ1 TCB) with superior T cell killing compared to 1þ1 asymmetric T cell bispecific IgG antibodies (1þ1 TCB). Can Res 2017;77:Abstr 3629.
[4]https://www.genentechoncology.com/pipeline-molecules/glofitamab.html?msclkid=ca89c0b6b0bd11eca758478c781c0280
[5] Schlothauer T, Herter S, Koller CF, Grau-Richards S, Steinhart V, Spick C, et al. Novel human IgG1 and IgG4 Fc-engineered antibodies with completely abolished immune effector functions. Protein Eng Des Sel 2016;29:457–66.
[6] Bacac M, Colombetti S, Herter S, et al. CD20-TCB with obinutuzumab pretreatment as next-generation treatment of hematologic malignancies[J]. Clinical Cancer Research, 2018, 24(19): 4785-4797.
[7] Hutchins M, Morschhauser F, Ikoboni G, Carlo Stella C, Offner FC, Suradar A, Salles G, Martinez-Lopez J, Cramp M, Thomas DN, Morcos PN, Fellini C, Brosque AE, Belousov A, Bacachi M, Demir N, Carlisle DJ, Lundberg L, Perez-Callejo D, Umnia P, Moore T, Weisel M, Dickinson MJ.Glofitamab is a novel bivalent CD20-targeted T cell participation bi-specific antibody. Induction of durable complete remission in relapsed or refractory B-cell lymphoma: Phase I trial. J. Colin Unker. June 20, 2021; 39 (18) : 1959-1970.
[8] Carlo‐Stella C, Hutchings M, Offner F C, et al. GLOFITAMAB STEP‐UP DOSING: UPDATED EFFICACY DATA SHOW HIGH COMPLETE RESPONSE RATES IN HEAVILY PRETREATED RELAPSED/REFRACTORY (R/R) NON‐HODGKIN LYMPHOMA (NHL) PATIENTS[J]. Hematological Oncology, 2021, 39.
[9] Michael Dickinson. ASCO 2022 7500.
[10] Shang-Ju Wu. EHA 2022 P1234.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


