Cell子刊:闫靖等人开发有希望的渐冻症治疗药物,可阻止运动神经元的损失并减轻疾病进展
来源:生物世界 2024-02-11 11:16
研究证实了eNMDAR毒性是渐冻症发病机制的关键因素,而TwinF界面抑制剂可能为渐冻症患者提供一种有效的治疗选择。
闫靖博士、Hilmar Bading教授等在 Cell 子刊 Cell Reports Medicine 上发表了题为:TwinF interface inhibitor FP802 stops loss of motor neurons and mitigates disease progression in a mouse model of ALS 的研究论文。
该团队在之前研究的基础上开发了一种TwinF界面抑制剂——FP802,其通过破坏 NMDAR/TRPM4死亡信号复合物来发挥神经保护作用,并在渐冻症小鼠模型和渐冻症患者来源的脑类器官中证实了其保护作用。
该研究证实了eNMDAR毒性是渐冻症发病机制的关键因素,而TwinF界面抑制剂可能为渐冻症患者提供一种有效的治疗选择。这型研究具有深远的临床意义,有望显著减轻渐冻症患者的痛苦并延长他们的预期寿命。

大约10%的渐冻症患者是由一个或多个基因突变引起,其余的大多数渐冻症患者的病因仍然未知。遗传性家族性渐冻症以及更常见的散发性渐冻症患者都存在兴奋性氨基酸转运蛋白(EAAT)的表达或功能缺陷,这会导致突触间隙中谷氨酸(Glu)泄漏,进而导致细胞外谷氨酸浓度增加至神经毒性水平。
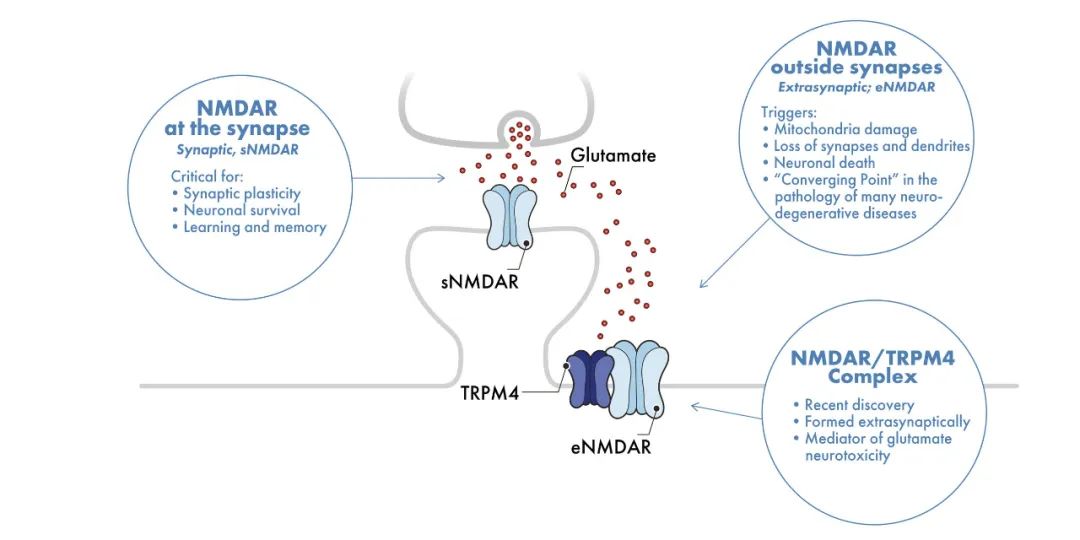
NMDA受体(NMDAR),那些位于突触外启动毒性信号的NMDAR,已被认为是渐冻症及其他神经退行性疾病死亡信号的启动者。然而,突触外NMDAR(eNMDAR)在渐冻症中的确切作用仍在很大程度上未被探索。尽管有有效的NMDAR阻断剂可供使用,但由于NMDAR在大脑中的双重功能,药理学研究在解释其作用方面面临困难。突触外NMDAR(eNMDAR)是谷氨酸诱导的神经元细胞死亡的主要介质,而突触NMDAR(sNMDAR)控制突触可塑性相关事件和认知功能。经典的NMDAR阻断剂无法区分位于突触内外的NMDAR,因此其不仅消除了毒性作用,还消除了生理功能。这限制了它们在神经退行性疾病的动物研究中的价值,以及在临床试验中作为治疗药物的适用性。
2020年10月,闫靖博士等在 Science 期刊发表了一篇题为:Coupling of NMDA receptors and TRPM4 guides discovery of unconventional neuroprotectants 的研究论文。
该研究发现,突触外NMDAR(eNMDAR)与瞬时受体电位阳离子通道亚家族M成员4(TRPM4)的物理相互作用是其毒性信号传导的罪魁祸首,而使用互作界面抑制剂破坏二者的结合,可缓解毒性作用并维持eNMDAR的正常生理功能。

上述发现为开发靶向TRPM4中的TwinF结构域的小分子抑制剂来发挥神经保护作用奠定了基础。TwinF界面抑制剂通过结合TRPM4相互作用界面的TwinF结构域,破坏NMDAR/TRPM4死亡信号复合物,可选择性地消除eNMDAR的毒性信号,同时保留sNMDAR的生理功能。
在这项研究中,研究团队首先探索了化合物8的的化学空间,这是一种TwinF界面抑制剂原型药物,进而改造出了一种安全和有效的神经保护剂——FP802,随后用于研究eNMDAR在渐冻症中的作用。
研究团队在SOD1G93A渐冻症小鼠模型发病后使用FP802进行治疗,其可以阻止脊髓中运动神经元的进行性丧失,导致渐冻症的血清生物标志物神经丝轻链蛋白(NfL)的减少,改善运动表现并延长寿命。此外,研究团队还构建了渐冻症患者来源的前脑类器官,FP802可有效地阻止其中神经元的死亡。
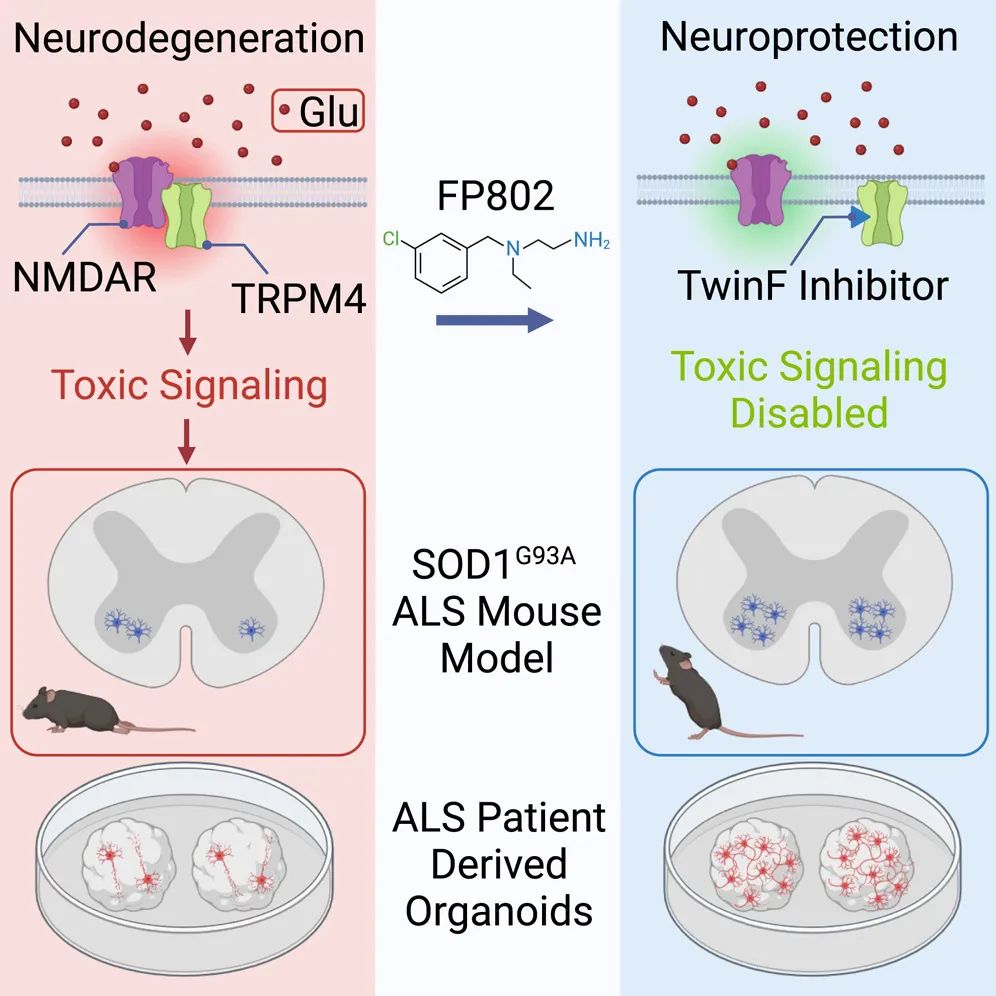
这些结果证实了突触外NMDAR(eNMDAR)毒性是渐冻症发病机制中的关键角色,而TwinF界面抑制剂可能为渐冻症患者提供一种有效的治疗选择。

Hilmar Bading教授、闫靖博士等创立了一家名为FundaMental Pharma的公司,开发NMDAR/TRPM4界面抑制剂,以治疗渐冻症、阿尔茨海默病、中风等疾病。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


