治疗早期阿尔兹海默病!卫材/渤健「仑卡奈单抗」新适应症获FDA受理
来源:医药魔方 2024-06-12 09:21
仑卡奈单抗是一种用于治疗AD的人源化单克隆抗体,可以选择性中和并清除导致AD神经病变的可溶且有毒性的Aβ聚集体。
6月9日,卫材和渤健共同宣布仑卡奈单抗(Lecanemab,商品名:Leqembi)静脉注射(IV)剂型的补充生物制品许可申请(sBLA)获FDA受理,用于维持治疗早期阿尔茨海默病(AD)患者,即存在轻度认知障碍或处于轻度痴呆阶段的AD患者。PDUFA日期为2025年1月25日。

早期AD患者需在起始阶段先接受每两周1次(Q2W)的仑卡奈单抗治疗,然后再接受每月1次的仑卡奈单抗治疗,以此维持有效的药物浓度从而清除有毒的原纤维(即使在淀粉样蛋白β(Aβ)斑块从大脑中清除后,这些原纤维仍会继续存在导致神经元损伤)。
此次sBLA主要是基于II期Study 201研究及其开放标签扩展(OLE)研究和Clarity AD(Study 301)研究及其OLE研究的数据。
Clarity AD研究纳入了1795例早期AD患者。研究结果表明,在第18个月时,与安慰剂组相比,仑卡奈单抗组患者的临床痴呆症评分总表(CDR-SB)分数下降了27%。此外,由AD看护者评估的次要终点阿尔茨海默病协作研究组-轻度认知障碍-日常生活能力量表评分(ADCSMCI-ADL,衡量患者独立运作的能力,包括能够穿衣、喂食和参与社区活动)也下降了37%。
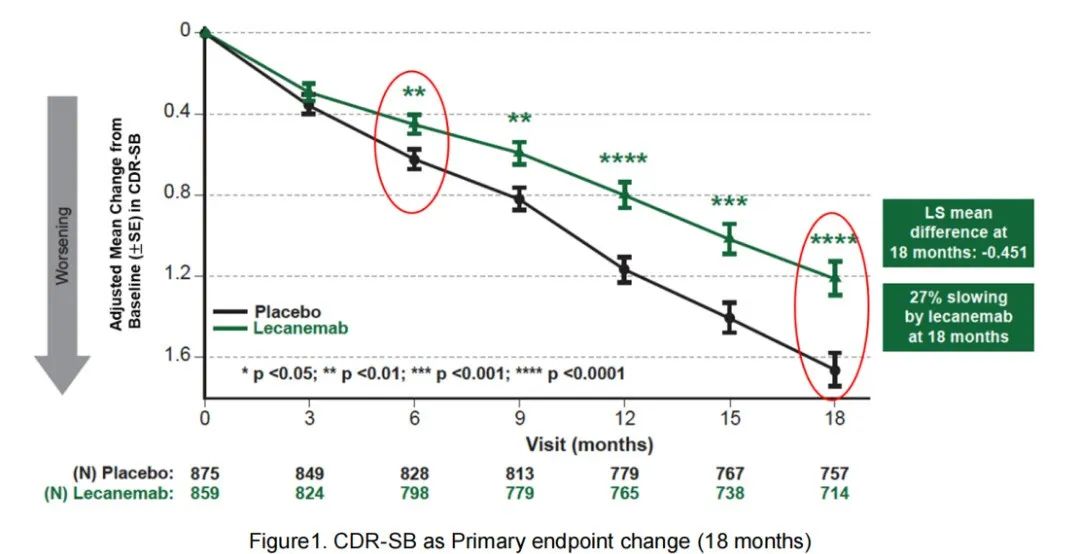
主要终点结果(来源:NEJM)
安全性方面,仑卡奈单抗组出现了6例死亡,安慰剂组出现了7例死亡。调查人员认为死亡事件与仑卡奈单抗及ARIA现象(淀粉样蛋白相关成像异常,可能是大脑水肿(ARIA-E)或微出血(ARIA-H)的迹象)均无关。仑卡奈单抗治疗组严重不良事件(SAE)发生率为14%,安慰剂组为11.3%。最常见的SAE是输注相关反应、ARIA-E、房颤、晕厥及心绞痛。
此外,卫材正在向FDA滚动提交仑卡奈单抗皮下注射(SC)剂型每周1次)用于维持治疗AD的BLA(见:卫材在美递交阿尔兹海默症新药Leqembi皮下注射剂上市申请)。
AD是一种持续的神经毒性过程,在Aβ斑块沉积之前开始并在Aβ斑块沉积之后持续进展。治疗早期AD是当务之急,因为在早期进行持续治疗可以减缓AD的进展。AD引起的轻度认知障碍和轻度痴呆越早得到诊断和治疗,患者获益的机会就越大。
仑卡奈单抗是一种用于治疗AD的人源化单克隆抗体,可以选择性中和并清除导致AD神经病变的可溶且有毒性的Aβ聚集体。因此,仑卡奈单抗可能对AD病理过程产生积极影响并减缓疾病发展进程。
仑卡奈单抗IV剂型现已在美国、日本和中国获批上市。2014年3月,渤健与卫材达成协议,获得了该药物的共同开发和商业化权益。据渤健财报,2023年仑卡奈单抗销售额为1000万美元。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


