“主动预防”破解CMV感染挑战,来特莫韦为移植手术保驾护航
来源:生物谷 2022-08-03 17:38
新型管理模式,不仅给造血干细胞移植成功提供了强有力的支持,还将这种病毒的防控端口从被动治疗前移到前端主动预防治疗。
巨细胞病毒(CMV)是一种常见的人类疱疹病毒,在全球绝大多数人群体内均存在巨细胞病毒终身潜伏。在健康成人中,CMV通常被视为一种无症状且致病性温和的病毒,但对于免疫抑制或缺陷患者,如异基因造血干细胞移植(allo-HSCT)术后患者,是其高发病率和死亡率的原因之一。如何守护患者平安度过感染的窗口期,这是摆在临床医生面前亟待解决的关键问题。
作为全球首个且目前唯一用于CMV血清阳性的异基因造血干细胞移植受者CMV感染的预防药物,来特莫韦开启了“预防为先”的CMV管理新格局。国家药品监督管理局(NMPA)于2021年12月和2022年5月正式批准来特莫韦片及来特莫韦注射液用于接受异基因造血干细胞移植的CMV血清学阳性的成人受者(R+)CMV感染和CMV病的预防,填补了移植后预防领域的空白。
预防为先,CMV防控亟需创新应对手段
CMV感染是异基因造血干细胞移植后常见的、影响患者预后的、甚至危及生命的并发症,被称为“移植巨魔”。在我国,成人造血干细胞移植患者移植前CMV血清学阳性率高达92%[1],病毒复燃比例高达30~80%[2],如不采去预防措施,80%的患者可能会在异基因造血干细胞移植后100天内出现CMV再激活[3],而CMV再激活与移植后结局较差相关[4]。近年来,中国的造血干细胞移植水平已经达到国际领先水准,但在巨细胞病毒的防控领域,仍然存在较大的未被满足的需求。
当前应对CMV感染的主要方法为抢先治疗,即通过定量聚合酶链反应 (PCR) 对患者CMV-DNA水平进行早期监测,在CMV-DNA达到阈值时立即启动抢先治疗策略进行抗病毒治疗[5]。虽然抢先治疗是控制巨细胞病毒的有效方法,但仍有诸多不足,如病毒阈值不统一,抢先治疗药物存在骨髓抑制、肾毒性等不良反应问题,增加了患者的死亡风险和医疗负担[6,7,8]。临床亟需安全且高效的CMV感染预防应对手段。

刘开彦教授
北京大学血液病研究所主任医师刘开彦教授表示,CMV感染是造血干细胞移植患者生命健康的一大威胁。作为全球首个且目前唯一获批用于异基因造血干细胞移植巨细胞血清学阳性成人受者预防CMV感染及CMV病的药物,来特莫韦弥补了CMV预防领域的空白,为临床应对CMV感染提供了全新解决方案。临床试验及多国真实世界研究均已证实来特莫韦能够有效预防异基因造血干细胞移植患者的CMV感染并改善患者预后,同时无明显骨髓抑制、肾毒性等不良反应及交叉耐药,为造血干细胞移植成功提供了有力支持,同时也能够减少医疗资源的消耗与浪费。期待这一医学创新成果能够在临床实践中得到广泛应用,为更多血液病患者点亮治疗希望。
首款预防性药物打破CMV管理困局
与传统抗CMV药物不同,来特莫韦是一种新型非核苷CMV抑制剂,通过结合和抑制UL56和UL89处的病毒末端酶复合物,作用于病毒复制的晚期,阻止病毒的剪切和包装[3]。
早在2017年《新英格兰医学杂志》就发布了来特莫韦的一项关键III期临床研究[9]。该研究将入组的CMV血清阳性移植受者按2:1随机分为来特莫韦组和安慰剂组,来特莫韦给药剂量为480mg/天(服用环孢素的患者240mg/天),持续给药至第14周(大约100天)。主要终点和次要终点分别为在随机化时未检测到CMV DNA的患者中,移植后24周内和14周内发生有临床意义的CMV感染(CMV病或导致优先治疗的CMV病毒血症)的患者比例。患者随访至移植后第48周。
结果显示,至移植后24周,来特莫韦组有临床意义的CMV感染率较安慰剂组显著降低(18.9% vs 44.3%,P<0.001)。
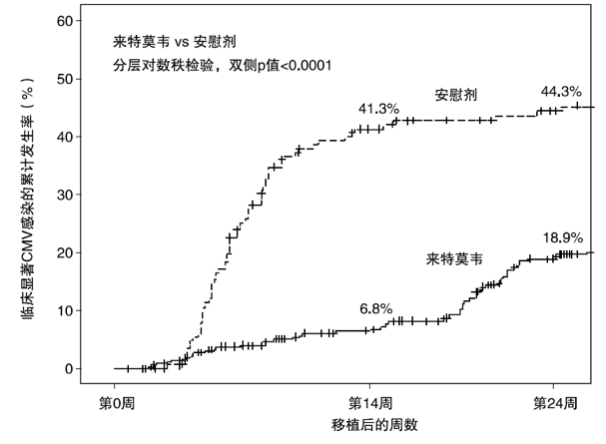
图1 有临床意义的CMV感染率随时间变化趋势
在主要有效性人群中,来特莫韦组移植受者移植后24周的全因死亡率低于安慰剂组(10.2% vs 15.9%,P=0.03)。
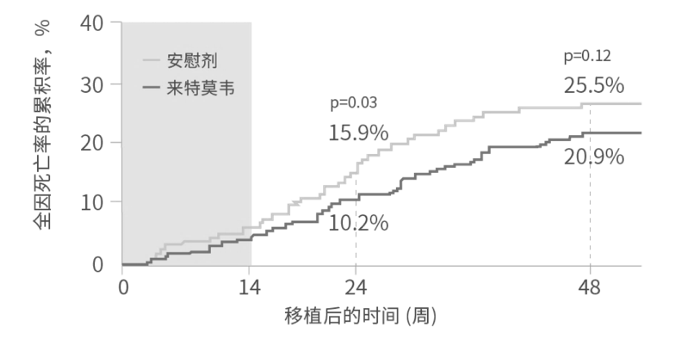
图2 全因死亡率随时间的变化趋势
同时,在安全性方面,其不良反应及严重程度与安慰剂相似。与安慰剂相比,来特莫韦无骨髓抑制、肾毒性事件增加。
此外,意大利真实世界研究也显示,移植后0天启动来特莫韦,持续预防100天,CMV复燃和CMV病发生率分别降低82%和83%,180天内移植受者再住院率显著降低39.4%,且无交叉耐药的限制[10]。
除上述口服剂型外,来特莫韦注射剂也于今年5月获批,这为临床应对造血干细胞移植过程中的巨细胞病毒感染问题提供了更丰富的预防性治疗选择,特别是对部分口服药不耐受的患者,注射剂型能够帮助该类患者提高药物吸收效率,继而提升临床预防的效果。两种剂型相互配合,将更好地满足患者个性化治疗需求。
让创新医学成果惠及更多血液疾病患者
来特莫韦预防给药的管理模式,不仅给造血干细胞移植成功提供了强有力的支持,还将这种病毒的防控端口从被动治疗前移到前端主动预防治疗,降低了患者终末器官疾病、难治性或耐药性CMV感染以及移植再住院率,延迟了开始抢先治疗的中位时间,同时亦无明显骨髓抑制、肾毒性等不良反应,降低了CMV相关医疗风险、以及CMV相关治疗和管理成本。在一定程度上为我国异基因造血干细胞移植后受者提供了经济有效的保护,减轻了患者的疾病和经济负担。期待相关部门能持续关注移CMV感染防控问题,让更多具有临床实践和药物经济学优势的创新药加速进入医保,减轻患者的用药负担,让血液疾病患者享受到前沿的医学创新成果。
参考文献
1,丁昊炜等. 造血干细胞移植患者巨细胞病毒感染危险因素和疗效分析.北京大学学报(医学版).2003;35(6):596-599
2,Styczynski J. Infect Dis Ther. 2018;7(1):1-16
3,Ljungman P, et al. Hematol Oncol Clin North Am. 2011 Feb;25(1):151-69
4,Camargo JF, et al. Hematol Oncol Stem Cell Ther. 2017 Dec;10(4):233-238.
5,Hakki M, et al. Transplant Cell Ther. 2021 Sep;27(9);707-719
6,Hakki M, et al. Transplant Cell Ther. 2021 Sep;27(9);707-719
7,Britt W J, Prichard M N. Antiviral research, 2018, 159: 153-174.
8,El Haddad L, et al. J Med Virol. 2020 Jan;92(1):86-95.
9,Marty FM, et al. N Engl J Med. 2017;377(25):2433-2444.
10,Malagola M, et al. Front Cell Dev Biol. 2020;8:534268.
11,中国淋巴瘤治疗指南(2021年版)[J]. 中华肿瘤杂志, 2021, 43(7):29.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


