Cell:重磅!下一代更智能的细胞疗法出炉!表达模块化SNIPR受体的CAR-T细胞可高效杀死实体瘤,同时减少毒副作用
来源:生物谷原创 2022-04-21 19:45
格拉德斯通研究所和加州大学旧金山分校的研究人员在一项新的研究中对用于设计治疗性细胞的分子构件进行了系统分析。
基于工程化免疫细胞(即经过基因改造的免疫细胞)的疗法最近成为治疗癌症的一种有希望的方法。与传统药物相比,工程化免疫细胞在检测和消除癌细胞的能力方面更加精确和精密。然而,尽管前景广阔,基于细胞的疗法仍然面临重要的限制,包括毒性和它们可能攻击健康细胞的可能性。此外,科学家们并没有很好地掌握如何对现有的治疗性细胞(therapeutic cell)进行基因修饰,以扩它们的应用范围或更好地控制它们的活性。
为了克服这些限制,格拉德斯通研究所和加州大学旧金山分校的研究人员在一项新的研究中对用于设计治疗性细胞的分子构件进行了系统分析。他们的研究为设计具有更高特异性和安全性的治疗性细胞,以及最终定制基于细胞的治疗方法制定了全面的规则手册。相关研究结果发表在2022年4月14日的Cell期刊上,论文标题为“Modular design of synthetic receptors for programmed gene regulation in cell therapies”。

论文通讯作者、加州大学旧金山分校微生物学与免疫学系副教授Kole Roybal博士说,“我们确定了一些应当极大地促进治疗性细胞工程化使其具有比以前更高的敏感性、准确性和安全性的原则。我们的研究将为生物医学科学家们提供一个工具包,用于将一系列基于细胞的疗法引导到它们的预定靶标,并对它们的治疗活性进行编程。”
构建更好的受体
大多数治疗性细胞的关键是一种叫做受体的分子。受体是跨越细胞外膜的大型蛋白。它们的胞外部分能识别特定的靶标(例如癌细胞表面上的蛋白),而它们的胞内部分则告诉细胞在识别这个靶标后要做什么。设计治疗性细胞的一种方法是在细胞---通常是称为T细胞的免疫细胞---中插入由已知受体的片段拼凑而成的合成受体。
这种方法被用来构建CAR-T细胞,它已被证明对消除某些类型的血癌非常有效。CAR-T细胞携带“嵌合抗原受体(CAR)”,而CAR是基于通常在T细胞中发现的受体而产生的。
从不同的骨架开始,Roybal之前开发了一种名为synNotch的受体,可以引导T细胞更好地识别和杀死实体瘤(Cell, 2016, doi:10.1016/j.cell.2016.09.011)。自从这项早期研究以来,Roybal的实验室已经展示了synNotch如何与CAR结合使用,以开发针对卵巢癌和间皮瘤的下一代细胞疗法(Science Translational Medicine, 2021, doi:10.1126/scitranslmed.abd8836)。synNotch受体使得科学家们能够精确控制治疗性T细胞在何时和何处是有活性的。
Roybal说,“这些智能细胞疗法可以精确地在疾病部位释放强大的治疗活性,提高疗效,减少患者出现威胁生命的毒性的机会。”
然而,原始的synNotch受体很难在人类中部署用于基于细胞的治疗。首先,它体积较大,这使得它很难插入到人类细胞中。另外,它的一些部分来自小鼠、酵母和病毒,而不是人类受体,这可能导致工程化细胞一旦进入患者体内就会产生免疫排斥反应。
为了了解他们能从synNotch受体中保留和剔除什么而不失去其理想的功能,Roybal团队系统地交换了该受体的各个部分。在将修改后的synNotch受体插入人类T细胞中后,他们测试了它们识别预定靶标和激活预期反应的能力。
论文共同第一作者、Roybal实验室博士后Raymond Liu博士说,“一项具有挑战性但有趣的壮举是弄清楚已知受体的不同部分是如何发挥作用的,这样我们就可以把这些部分拆开,然后以新的方式把它们重新组合起来,以满足我们的设计要求。”
最后,Roybal团队构建出一个他们称之为SNIPR(synthetic intramembrane proteolysis receptor,合成膜内蛋白分解受体)的受体的目录,这些受体足够小,可以在人类细胞中进行低成本的工程化。它们也完全由人类受体片段制成,可以检测和响应少量的靶标。此外,SNIPR的活性可以被调整,以便携带它们的细胞不只是杀死靶细胞,而且还可以将特定的分子递送到精确的疾病位置。
论文共同第一作者、Roybal实验室研究生Iowis Zhu说,“了解受体设计的规则使我们能够构建更有效、也更适合临床转化的受体。”
下一代细胞治疗的平台
这些作者接下来评估了这些优化的受体在白血病、间皮瘤和卵巢癌的小鼠模型中清除肿瘤的能力。为了减少杀死非靶细胞的机会,他们将经设计后用于识别肿瘤表面上的一种分子的SNIPR与经基因改后识别另一种肿瘤分子的CAR受体相结合。此外,他们使CAR受体的产生依赖于SNIPR受体的激活。这样,只有携带synNotch和CAR受体的作用靶标的细胞才会被杀死,而只携带其中的一种作用靶标的细胞则不会被杀死。
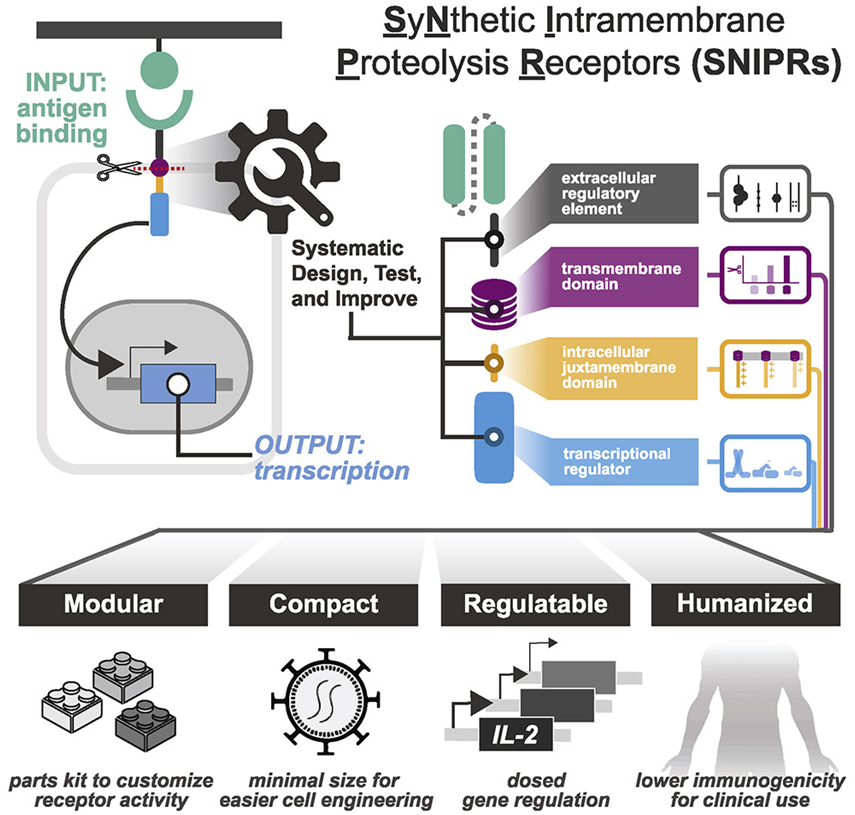
图片来自Cell, 2022, doi:10.1016/j.cell.2022.03.023。
在他们测试的三种癌症类型中的每一种中,这种两步靶向策略导致了比单独使用任何一种受体都更有选择性地消除癌细胞,从而突出了这种方法有望减少细胞疗法的脱靶毒性。
在科研机构和一家由Roybal联合创立的名为Arsenal Bio的公司中,基于SNIPR的细胞疗法如今正被优化,用于治疗卵巢癌、肾癌、前列腺癌和胶质母细胞瘤。
癌症可能不是唯一可以用基于SNIPR的细胞疗法治疗的疾病。这种受体系统也适用于增强免疫细胞的抗炎活性,以治疗自身免疫疾病。此外,SNIPR可可能能够用于靶向干细胞或其他细胞类型,以检测组织损伤并诱导组织修复或逆转纤维化。
Roybal说,“工程化细胞有可能作为比传统的小分子和生物制剂更聪明的治疗方法发挥作用。我们希望我们的新受体系统将作为一个技术平台,使科学家和临床医生能够设计出更安全、更有针对性、更有效的细胞疗法来对抗癌症和许多其他疾病。”(生物谷 Bioon.com)
参考资料:
1. Iowis Zhu et al. Modular design of synthetic receptors for programmed gene regulation in cell therapies. Cell, 2022, doi:10.1016/j.cell.2022.03.023.
2. A New Toolkit To Engineer Safe and Efficient Therapeutic Cells
https://gladstone.org/news/new-toolkit-engineer-safe-and-efficient-therapeutic-cells
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


