Cell Stem Cell:揭示TET2基因缺陷诱发人类急性髓性白血病发生的分子机制
来源:生物谷原创 2023-08-22 10:41
来自希望之城Beckman研究所等机构的科学家们通过研究揭示了低水平的TET2基因促进动物模型机体中急性髓性白血病快速生长的分子机制。
TET2在急性髓性白血病(AML)中会反复突变,TET2的缺乏会促进白血病的发生(由侵袭性致癌突变所驱动)并增强白血病干细胞(LSC, leukemia stem cell)的自我更新,然而潜在的细胞/分子机制,目前研究人员并不清楚。近日,一篇发表在国际杂志Cell Stem Cell上题为“TET2-mediated mRNA demethylation regulates leukemia stem cell homing and self-renewal”的研究报告中,来自希望之城Beckman研究所等机构的科学家们通过研究揭示了低水平的TET2基因促进动物模型机体中急性髓性白血病快速生长的分子机制。
文章中,研究者发现,TET2的缺乏会引发一系列生化改变,从而就会增强骨髓癌的扩散能力,这些变化包括:1)驱动恶性干细胞从血液中移动到其起源的骨髓区域,称之为生境(niche)的微环境能保护细胞的生存以及分裂和自我复制的能力;2)增加一种名为TSPAN13的蛋白质的表达,其能向白血病干细胞发送信号让其回归到骨髓生境中;3)导致甲基化形式的RNA基胞嘧啶的积累,从而就能增强TSPAN13信使RNA的稳定性,并导致TSPAN13蛋白表达水平的增加;4)激活称之为TSPAN13/CXCR4轴的信号通路,从而就能增加恶性干细胞归巢到骨髓生境并进行自我复制,从而导致白血病的快速发展。
通过扩大对TET2影响急性髓性白血病发生的多个通路的理解,本文研究发现或能提供治疗该疾病的新型潜在治疗性靶点;研究者Chen说道,本文研究为急性髓性白血病发生背后的细胞和分子机制提供了新的见解,同时该研究强调了在携带TET2突变或转录抑制的患者中重新激活TET2信号的治疗潜力,同样兴奋的是,这种策略或许还能应用于其它以TET2缺乏为特征的癌症类型。
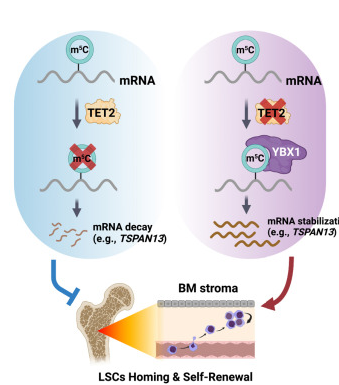
揭示TET2基因缺陷诱发人类急性髓性白血病发生的分子机制。
图片来源:Cell Stem Cell (2023). DOI:10.1016/j.stem.2023.07.001
急性髓性白血病往往以不成熟的白血病细胞的快速分裂和扩散为特点,有超过一半的患者会发生疾病的复发,而且患者5年的生存率仅为30%,阐明如何摧毁这些细胞对于有效治疗急性髓性白血病至关重要。TET2的缺乏常常会与源于染色体异常或基因突变的白血病相关癌蛋白协同作用,从而驱动白血病的的发生并增强恶性干细胞分裂和扩散的能力,然而截止到目前为止,研究人员仍然并不清楚这些过程背后的细胞和分子机制。
通过对来自癌症基因组图谱的数据进行分析后,研究者Chen及同事发现,TET2的低表达或突变常常与患者较差的预后以及较短的总体生存率相关,相比健康对照受试者而言,TET2的表达在急性髓性白血病患者机体中会明显受到抑制,这就会促使研究人员开始调查TET2在疾病发生过程中的临床相关性。综上,本文研究结果揭示了TET2作为mRNA m5C去甲基化酶在白血病发生、白血病母细胞迁移/归巢和LSC的自我更新中的功能重要性。(生物谷Bioon.com)
原始出处:
Yangchan Li,Meilin Xue,Xiaolan Deng, et al. TET2-mediated mRNA demethylation regulates leukemia stem cell homing and self-renewal, Cell Stem Cell (2023). DOI:10.1016/j.stem.2023.07.001
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


