解决胰岛素百年困境!David Baker团队从头设计出更安全有效的“AI胰岛素”,开启糖尿病治疗新时代
来源:生物世界 2025-10-16 12:09
这项研究不仅展示了如何设计更安全有效的胰岛素受体激动剂,还揭示了受体激活与信号转导之间的基本关系,为开发更安全、更有效的下一代糖尿病治疗药物奠定了基础。
自一个世纪前,班廷发现胰岛素(Insulin)以来,它一直是治疗糖尿病的基石,然而,基于胰岛素及其类似物的治疗存在着诸多局限性,例如,需要复杂的生产过程、严格的储存条件,可能促进癌细胞增殖,对部分遗传性胰岛素抵抗的患者无效。
胰岛素(Insulin)通过激活细胞表面的胰岛素受体(Insulin Receptor,IR)发挥作用。该受体如同一个复杂的“锁”,胰岛素则是开启它的“钥匙”。胰岛素激活胰岛素受体后,会启动两条主要信号通路:一条调控代谢(AKT 通路),负责降低血糖;另一条调控细胞生长(MAPK 通路),可能促进癌细胞增殖。因此,胰岛素受体的信号转导失调会导致糖尿病和癌症等疾病。
而通过基于 AI 的蛋白质从头设计,生成一种超稳定的、易于生产的蛋白质,作为胰岛素受体激动剂,发挥胰岛素功能,有望解决当前的胰岛素及其类似物的局限性。
2025 年 10 月 13 日,华盛顿大学蛋白质设计中心 David Baker 教授、Wang Xinru 博士,德克萨斯大学西南医学中心白晓晨研究员等,在 Cell 子刊 Molecular Cell 上发表了题为:Tuning insulin receptor signaling using de novo-designed agonists 的研究论文。
该研究利用基于 AI 的蛋白质从头设计,生成了胰岛素受体激动剂(AI 胰岛素),其不仅降血糖效果优于胰岛素,更能精准调控体内信号通路,避免胰岛素促进癌细胞生长,为开发更有效、更安全的糖尿病治疗方法奠定了基础。

在这项最新研究中,华盛顿大学、德克萨斯大学西南医学中心和哥伦比亚大学的研究人员组成的科研团队采用了一种全新策略,他们不再局限于天然胰岛素的结构,而是通过基于 AI 的蛋白质从头设计方法,从头设计生成新的胰岛素受体激动剂。
研究团队首先设计了两种结合蛋白:一种专门结合胰岛素受体的 L1 结构域(site-1,胰岛素与胰岛素受体的主要结合位点),另一种结合 F1 结构域(site-2,胰岛素与胰岛素受体的次要结合位点)。然后,通过不同长度的连接链将这两种结合蛋白连接起来,形成全新的胰岛素受体激动剂分子。
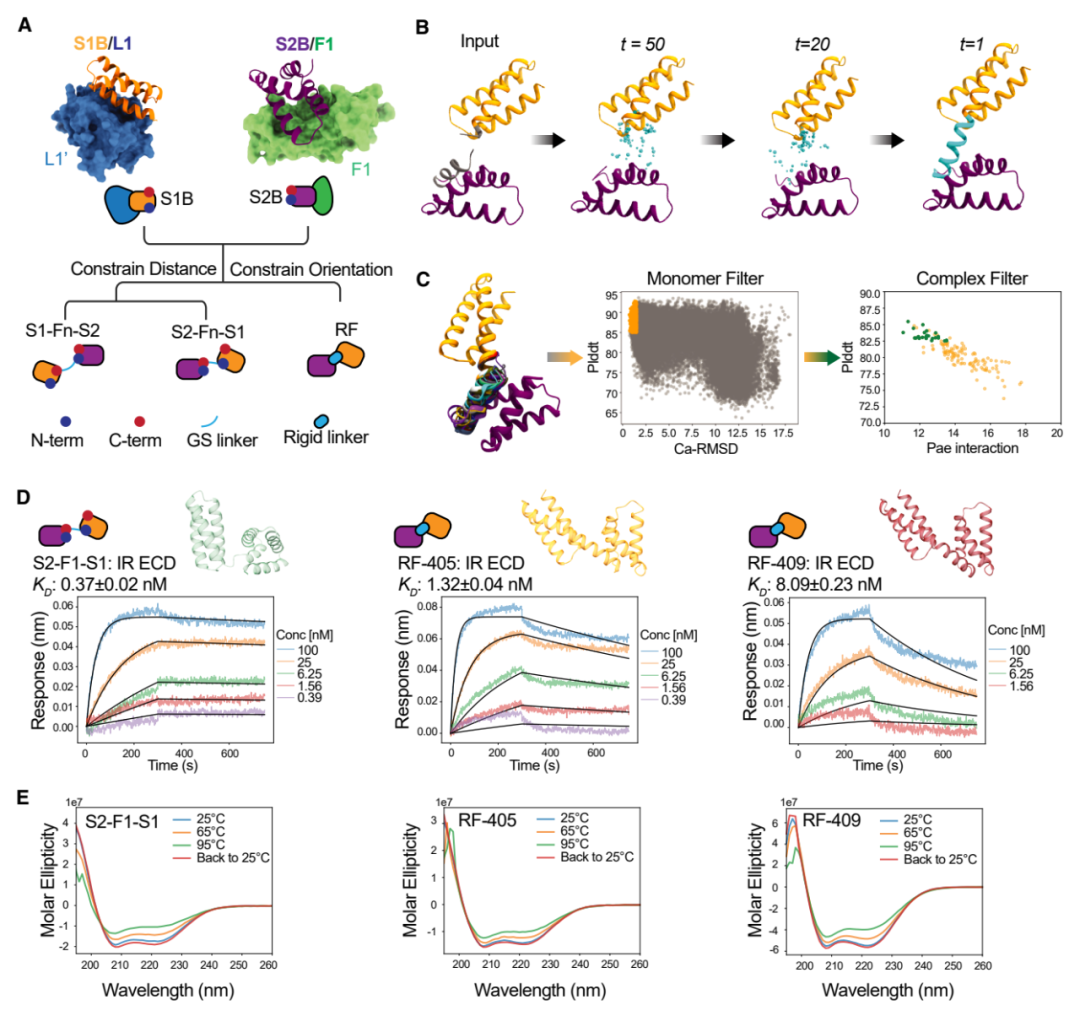
这些设计的胰岛素受体激动剂展现出令人瞩目的特性:
更强的热稳定性:与天然胰岛素不同,新设计的蛋白质在 95°C 的高温下仍能保持稳定,大大简化了储存和运输要求。
更精准的信号调控:通过调整连接链的刚性,研究团队实现了对信号通路的精确控制。刚性连接的设计(例如 RF-405)能同时激活代谢(AKT 通路)和细胞生长(MAPK 通路),而柔性连接的设计(例如 S2-F1-S1)则主要激活代谢,大幅减少了对细胞生长的刺激。
在小鼠实验中,这些设计的胰岛素受体激动剂分子展现出显著优势,其中,RF-409 在降低血糖方面比胰岛素更有效,仅需一半剂量就能达到相同效果,且作用时间更长。在肥胖糖尿病小鼠模型中,单次注射 RF-409 可使血糖水平维持低位达 6 小时,而胰岛素治疗后在 2 小时内血糖即开始回升。
特别值得注意的是,这些设计的胰岛素受体激动剂分子能够激活某些胰岛素抵抗患者体内的基因突变的胰岛素受体,为罕见遗传性糖尿病带来了新的治疗希望。
最令人振奋的是,这些设计的胰岛素受体激动剂分子在正常细胞中能有效激活胰岛素受体,但在乳腺癌细胞中却无法发挥作用。进一步研究发现,这是因为癌细胞表面同时表达胰岛素受体和 IGF-1 受体,容易形成杂交受体,而设计胰岛素受体激动剂分子只特异性结合胰岛素受体。
这种特异性结合能力意味着,这些设计的胰岛素受体激动剂可能大幅降低传统胰岛素治疗的潜在癌症风险,对于那些需要长期使用胰岛素治疗且担心癌症风险的患者而言,这无疑是个重大利好。
总结来说,胰岛素能够激活正常细胞的胰岛素受体,但无法激活突变的胰岛素受体,还会激活癌细胞的胰岛素受体;而基于 AI 的蛋白质从头设计的胰岛素受体激动剂,不仅能够激活正常细胞的胰岛素受体,还能激活突变的胰岛素受体,且不激活癌细胞的胰岛素受体。此外,设计的胰岛素受体激动剂降血糖效果更持久、稳定。
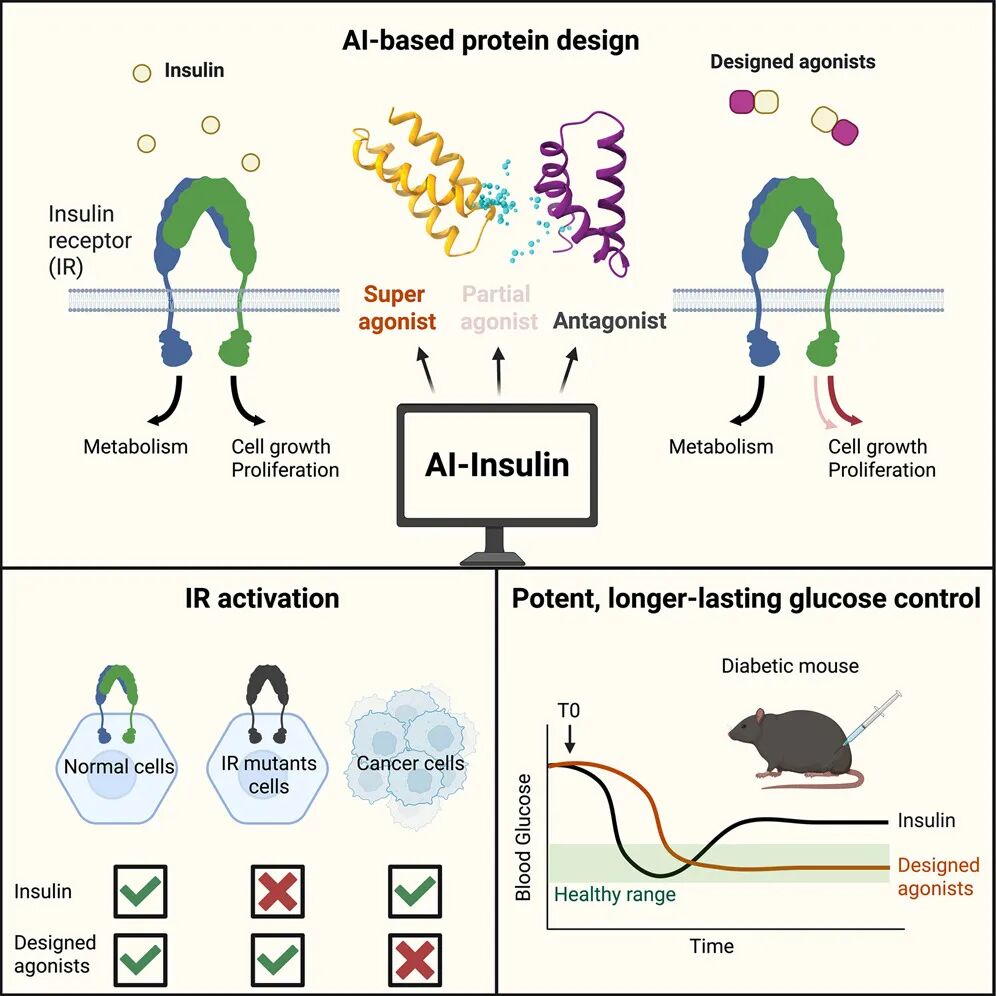
这项研究不仅展示了如何设计更安全有效的胰岛素受体激动剂,还揭示了受体激活与信号转导之间的基本关系,为开发更安全、更有效的下一代糖尿病治疗药物奠定了基础。
值得一提的是,David Baker 教授、Wang Xinru 博士等人创立了一家名为 Lila Biologics 的公司,该公司致力于利用 AI 蛋白质设计解锁突破性疗法,该公司目前有两大研究方向——AI 设计的放射性配体疗法,用于癌症治疗;AI 设计的长效注射剂,用于非癌症疾病治疗。
2025 年 9 月,Lila 宣布与国际制药巨头礼来达成合作,旨在发现、开发和商业化用于实体瘤成像和治疗的新型放射性配体疗法(RLT)。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


