扬州大学包文斌教授团队取得仔猪细菌性腹泻抗性遗传基础和调控机制研究新进展
来源:扬州大学 2022-06-29 15:12
该论文首次系统解析了仔猪细菌性腹泻抗性的遗传基础和调控机制,确定了仔猪腹泻抗性相关功能分子标记物及靶标基因。
2022年6月13日,江苏省现代农业(生猪)技术体系良种繁育岗位专家、扬州大学动物科学与技术学院包文斌教授团队在国际病原学权威期刊《PLoS Pathogens》在线发表了题为“Insight into mechanisms of pig lncRNA FUT3-AS1 regulating E. coli F18-bacterial diarrhea”的研究论文,该论文首次系统解析了仔猪细菌性腹泻抗性的遗传基础和调控机制,确定了仔猪腹泻抗性相关功能分子标记物及靶标基因。

腹泻引起的仔猪成活率低是长期以来我国母猪年生产力远远低于发达国家水平的主要限制因素,危害居猪病之首。对于以F18大肠杆菌为主要病原的细菌性腹泻,多年以来依赖抗生素及疫苗防控效果不尽如人意,反而给人类健康带来了威胁。随着耐药菌株的不断出现以及对抗生素使用的日益限制,开展抗病育种愈发成为迫切需求,但是由于遗传基础和调控机制不清楚、有效抗性分子标记缺乏等制约因素和瓶颈问题,导致抗病育种一度进展缓慢。研究发现,长链非编码RNAs (lncRNAs)参与基因转录调控、蛋白互作、表观修饰等多种生物学过程,可作为动物机体疾病及多种生理过程的分子标记物及药物靶点。
在该研究中,该团队以中国地方猪品种梅山猪和培育品种苏太猪(杜洛克×梅山猪)为研究素材,通过F18菌株攻毒试验并结合仔猪表型观察、菌落计数、肠道组织病理检测以及细菌体外黏附试验等一系列进行验证,严格筛选与获得了断奶仔猪F18大肠杆菌抗性型与易感型个体,在此基础上基于组学测序及数据分析筛选出1个与大肠杆菌抗性相关的重要lncRNA分子:FUT3-AS1,通过Northern blot、FISH定位、核质分离、RNA敲降以及细菌黏附能力测定等系统验证表明,FUT3-AS1作为F18大肠杆菌易感性调控的关键非编码RNA分子。
为了深入探究FUT3-AS1对大肠杆菌抗性的调控机制,该团队利用RNA/DNA pull down、RIP、ChIP-qPCR、双荧光素酶活性以及表达验证等系统探究发现FUT3-AS1一方面在细胞核内可以介导组蛋白H4K16ac乙酰化修饰影响FUT3启动子区转录因子Sp1结合,另一方面在细胞质内充当miR-212海绵体作用来竞争性地调控FUT3表达。此外,对靶基因FUT3开展了系统的功能验证,在细胞和组织水平上发现FUT3表达与F18大肠杆菌易感性密切相关,同时构建了FUT3基因敲除小鼠,通过F18大肠杆菌灌胃试验以及表型鉴定发现FUT3敲除小鼠明显提高了其对细菌性腹泻的抵抗能力。最后,利用iTRAQ蛋白组学、CoIP-MS和Pull down-MS蛋白互作探究了FUT3下游调控机制,发现FUT3可以通过激活/抑制鞘糖脂生物合成通路(调控大肠杆菌受体形成)和Toll样信号通路(调控细胞免疫应答能力),最终影响仔猪对F18大肠杆菌的易感性。
该研究从非编码RNA层面解析了对断奶仔猪F18大肠杆菌抗性的分子调控机制,确定了F18大肠杆菌病抗性的重要分子标记物及功能基因,不仅为今后制订抗仔猪细菌性腹泻病分子选育策略奠定基础和提供依据,同时为其他畜禽重要性状相关的lncRNA的功能验证以及调控作用机制分析提供了系统的科研思路。
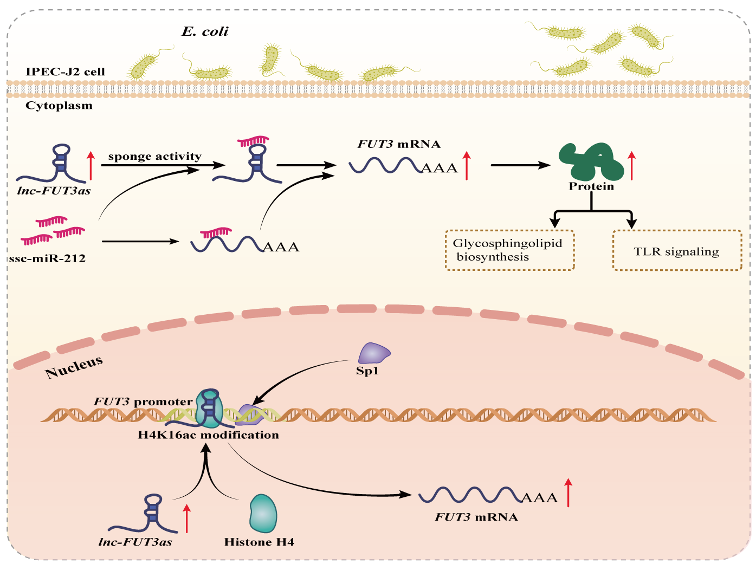
LncRNA-FUT3as调控F18大肠杆菌易感性的分子机制示意图
*扬州大学动物科学与技术学院青年教师吴正常为论文第一作者,博士研究生范海瑞为论文共同第一作者,包文斌教授为论文通讯作者,扬州大学动科学院吴圣龙研究员、江苏省现代农业(生猪)技术体系首席专家南京农业大学黄瑞华教授、扬州大学兽医学院高崧教授也参与论文的研究工作。该研究得到了国家自然科学基金、江苏省重点研发计划(现代农业)、中国博士后基金等项目的资助。
全文链接:https://doi.org/10.1371/journal.ppat.1010584
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


