Cancer Cell | 复旦大学江一舟/邵志敏/胡欣通过遗传相互作用揭示了乳腺癌独特的生物学和治疗意义
来源:生物探索 2024-04-13 12:23
该研究通过基因组学的整合分析及治疗队列和功能实验的验证,系统性功能解析了乳腺癌基因组变异互作对疗效的影响。
复旦大学江一舟、邵志敏及胡欣共同通讯在Cancer Cell 在线发表题为“Genetic interactions reveal distinct biological and therapeutic implications in breast cancer”的研究论文,该研究系统性绘制了全面的乳腺癌基因组变异互作网络,结合临床治疗队列及体内外模型功能性解析了基因组变异互作对乳腺癌治疗结局的影响,提出了基于基因组变异互作的精准治疗新策略。
该研究探究了一个大规模的多组学队列(n = 873)和一个现实世界的临床测序队列(n = 4405),包括几个具有详细治疗结果的临床试验,并在患者来源的类器官、肿瘤片段和体内模型中进行了功能验证。通过这种综合的方法,构建了一个由共变和互斥事件组成的网络,并表征了它们的治疗潜力和潜在的生物学基础。值得注意的是,研究发现TP53mut-AURKAamp与内分泌治疗耐药、种系BRCA1mut-MYCamp与PARP抑制剂敏感性提高、TP53mut-AURKAamp与免疫治疗耐药之间存在关联。此外,该研究揭示了由共同改变告知的精确治疗策略有望改善患者的预后,并强调了基因相互作用在指导基因组知情的治疗决策方面的重要性,而不是单一驱动因素的改变。

精准肿瘤学通过对癌症基因组的持续研究和下一代测序的常规应用,引入了新的治疗选择,彻底改变了乳腺癌的治疗前景。基因组靶向治疗或基因组知情治疗,如抗erbb2靶向治疗或PARP抑制剂(PARPi),可改善特定基因组改变患者的预后虽然临床成功推动了精准治疗的努力,但由于普遍关注临床决策中的单一驱动改变,忽视了共同发生的基因组改变对临床结果的影响,因此疗效仍然有限。此外,诸如免疫疗法等有前景的药物的出现使治疗反应的准确预测复杂化,需要识别超越单一驱动改变的新型生物标志物。鉴于这些挑战,迫切需要将注意力转向基因相互作用,以有效地指导精确治疗。
癌症的发生是由多个基因中连续发生的基因改变的聚合精心策划的,表现出非随机和受调节的模式。观察到的这些遗传改变的共发生或相互排他性可能反映了遗传相互作用的存在,从而描绘了不同的功能关系。具体来说,互排他性表明要么是功能冗余,要么是拮抗作用,这表明在缺乏靶向改变的患者中,合成的致命相互作用具有治疗潜力相反,共发生反应了功能合作,表明合成的拯救相互作用和针对其中一种共改变的治疗可能产生耐药性。
最近的研究已经深入了解了特定驱动因素变化的非随机模式。相互排他性已经在各种肿瘤类型中进行了研究,而某些共同发生的改变与临床结果和微环境组成有关。CRISPR和化合物筛选也提供了特异性致癌改变之间相互作用的证据。尽管人们越来越关注共同发生和相互排他性,但这些事件背后的临床后果尚未得到充分阐明。
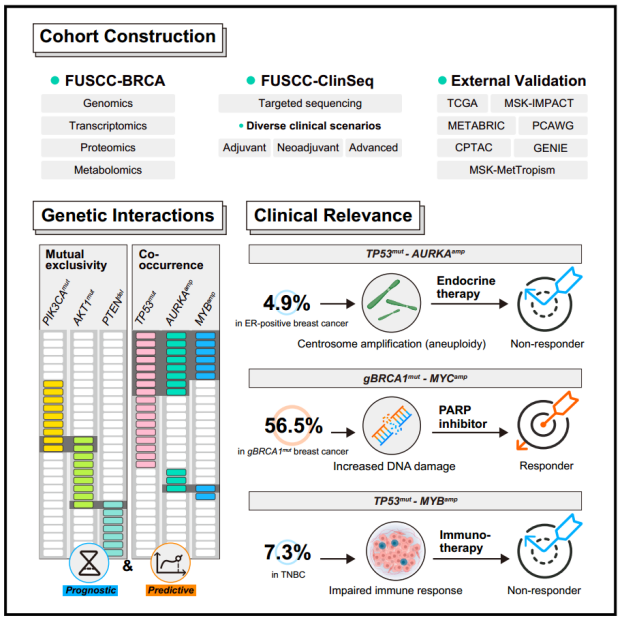
模式图(Credit: Cancer Cell)
总的来说,对癌症基因组的新见解需要关注基因组改变的共发生和相互排他性。为了研究它们的生物学特性并辨别对治疗结果的影响,该研究提供了一个大规模的多组学队列(FUSCC-BRCA)和一个注释良好的前瞻性靶向测序队列(FUSCC-ClinSeq)。该研究通过基因组学的整合分析及治疗队列和功能实验的验证,系统性功能解析了乳腺癌基因组变异互作对疗效的影响。因此,这些发现可能提高人们解释治疗反应变化的能力,并补充正在进行的精确肿瘤学研究。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


