Nature:揭示膜固醇激活七跨膜蛋白SMO的机制
来源:本站原创 2019-07-08 12:57
2019年7月8日讯/生物谷BIOON/---Hedgehog信号转导是胚胎发育和出生后组织再生的基础。异常的出生后Hedgehog信号转导导致几种恶性肿瘤,包括基底细胞癌和儿童成神经管细胞瘤。Hedgehog蛋白结合并抑制跨膜胆固醇转运蛋白Patched-1(PTCH1),从而允许七跨膜转导蛋白Smoothened(SMO)激活,但是人们对这种激活机制知之甚少。在一项新的研究中,来自美国加州大学
2019年7月8日讯/生物谷BIOON/---Hedgehog信号转导是胚胎发育和出生后组织再生的基础。异常的出生后Hedgehog信号转导导致几种恶性肿瘤,包括基底细胞癌和儿童成神经管细胞瘤。Hedgehog蛋白结合并抑制跨膜胆固醇转运蛋白Patched-1(PTCH1),从而允许七跨膜转导蛋白Smoothened(SMO)激活,但是人们对这种激活机制知之甚少。
在一项新的研究中,来自美国加州大学旧金山分校、犹他大学和斯坦福大学的研究人员报道了活性小鼠SMO与激动剂SAG21k和一种细胞内结合的纳米抗体(nanobody)结合在一起时的晶体结构图,其中这种纳米抗体让SMO的生理相关活性状态保持稳定。相关研究结果于2019年7月1日在线发表在Nature期刊上,论文标题为“Smoothened stimulation by membrane sterols drives Hedgehog pathway activity”。
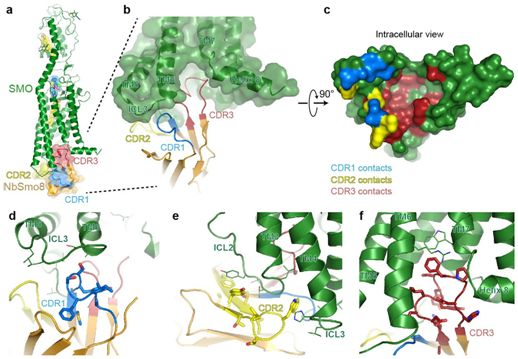
与其他的G蛋白偶联受体相类似的是,SMO的激活与细胞外结构域中的细微运动和更大的细胞内变化相关。
与近期提出的模型不同的是,对SMO激活至关重要的胆固醇分子在它的七跨膜口袋内的深处结合。
这些研究人员提出Hedgehog让PTCH1失活允许跨膜固醇进入这个七跨膜位点(可能通过疏水隧道),从而促进SMO激活。
这些研究结果与信号转导研究和分子动力学模拟相结合确定了 PTCH1-SMO调节的结构基础,并提出了克服SMO抑制剂临床耐药性的策略。(生物谷 Bioon.com)
参考资料:
Ishan Deshpande et al. Smoothened stimulation by membrane sterols drives Hedgehog pathway activity. Nature, 2019, doi:10.1038/s41586-019-1355-4.
在一项新的研究中,来自美国加州大学旧金山分校、犹他大学和斯坦福大学的研究人员报道了活性小鼠SMO与激动剂SAG21k和一种细胞内结合的纳米抗体(nanobody)结合在一起时的晶体结构图,其中这种纳米抗体让SMO的生理相关活性状态保持稳定。相关研究结果于2019年7月1日在线发表在Nature期刊上,论文标题为“Smoothened stimulation by membrane sterols drives Hedgehog pathway activity”。

图片来自Nature, 2019, doi:10.1038/s41586-019-1355-4。
与其他的G蛋白偶联受体相类似的是,SMO的激活与细胞外结构域中的细微运动和更大的细胞内变化相关。
与近期提出的模型不同的是,对SMO激活至关重要的胆固醇分子在它的七跨膜口袋内的深处结合。
这些研究人员提出Hedgehog让PTCH1失活允许跨膜固醇进入这个七跨膜位点(可能通过疏水隧道),从而促进SMO激活。
这些研究结果与信号转导研究和分子动力学模拟相结合确定了 PTCH1-SMO调节的结构基础,并提出了克服SMO抑制剂临床耐药性的策略。(生物谷 Bioon.com)
参考资料:
Ishan Deshpande et al. Smoothened stimulation by membrane sterols drives Hedgehog pathway activity. Nature, 2019, doi:10.1038/s41586-019-1355-4.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


