北京协和医学院:GOLM1抑制自噬介导的肝癌抗肿瘤免疫
来源:本站原创 2021-09-26 16:22
免疫介导的肿瘤消除依赖于细胞因子的产生和肿瘤微环境中免疫细胞的募集。细胞死亡相关信号,对下游免疫反应的激活至关重要。
免疫介导的肿瘤消除依赖于细胞因子的产生和肿瘤微环境中免疫细胞的募集。细胞死亡相关信号,对下游免疫反应的激活至关重要。GOLM1,又称GOLPH2和GP73,是一种高尔基跨膜蛋白,参与蛋白质货物通过高尔基体运输,在各种癌症中被广泛研究,其通过AKT/ mTOR途径促进癌症增殖和转移的多功能作用。它的分泌形式已被用作肝细胞癌(HCC)肿瘤发生和进展患者的血清生物标志物。但其在抗癌免疫中的作用尚不清楚。
图片来源:https://doi.org/10.1038/s41392-021-00673-6
免疫组化结果显示,golm1在恶性HCC组织中的表达水平明显高于良性肝组织。Kaplan Meier生存分析显示GOLM1高表达(cutoff值= 96.5)的HCC患者预后较差。作者进一步研究了肝癌组织中CD8与GOLM1表达水平的负相关关系,提示GOLM1可能参与了肝癌的免疫调节。重要的是,高表达GOLM1的肿瘤分化较差,提示GOLM1可能预测HCC的恶性进展。总体而言,GOLM1在人HCC肿瘤微环境中肿瘤细胞中表达升高,并与CD8+ T细胞浸润和临床结局呈负相关。
为了进一步确定GOLM1在抗肿瘤免疫中的作用,作者首先构建了几个独立的无GOLM1表达的H22肝癌和MCA205纤维肉瘤细胞系。与它们的 WT 亲本细胞相比,Golm1 / H22 肝癌和 MCA205 纤维肉瘤在免疫活性小鼠中表现出肿瘤生长的显着减少。有趣的是,在T细胞缺陷的nu/nu小鼠中,Golm1 / H22和MCA205细胞生长成肿瘤,其大小与相应的WT细胞相似。虽然两组小鼠早期均产生腹部块状恶性腹水,但H22肿瘤细胞中Golm1表达的缺失使小鼠中位生存期从21天显著延长至29.5天。40%的小鼠在第40天完全恢复。这些发现表明,与Golm1缺陷相关的肿瘤消退以免疫依赖的方式发生。
事实上,Golm1 的敲除增加了肿瘤浸润性 CD4+ 或 CD8+ T 细胞、产生
IFNγ 的细胞毒性 T 淋巴细胞的数量、更高比例的
F4/80+ MHCII+ 巨噬细胞和 CD11c+ MHCII+ 树突状细胞。此外,从H22和MCA205 Golm1 / tumor环境分离的TILs分泌的IFNγ比相应Golm1+/+肿瘤的IFNγ多。特别是,Golm1 / tumor中凋亡细胞的比例比Golm1- sufficient对照组大,且明显表达活化的caspase-3,提示细胞死亡的增加可能触发抗原提呈细胞的识别和特异性抗肿瘤免疫应答。总之,Golm1缺陷可能会促进T细胞和APCs招募到肿瘤中,导致ifn - γ等细胞因子的产生增加。
化疗诱导的免疫原性细胞死亡(ICD)有望影响肿瘤免疫浸润的组成和结构,从而有助于残余肿瘤细胞的清除。在该研究中,与WT细胞相比,Golm1 /细胞中Annexin
V+DAPI亚群增加,提示Golm1缺失促进了早期凋亡。western
blotting分析显示,MTX处理Golm1 / H22细胞后,细胞内的cleaved-PARP和cleaved-Caspase8水平随着cleaved-FLIPL的减少而增加。更重要的是,在MTX治疗中,Golm1缺陷显著增加了ATP的分泌,支持ATP可能在Golm1 / tumor的抗肿瘤免疫中发挥关键作用。为了消除肿瘤微环境中的细胞外 ATP,胞外 ATP 酶 CD39 在肿瘤细胞表面过表达。 CD39 在 Golm1/MCA205 细胞上的存在显着恢复了与 Golm1+/+ MCA205 相似的肿瘤生长速度。因此,Golm1缺乏可能通过增加细胞外ATP释放来促进抗肿瘤免疫。
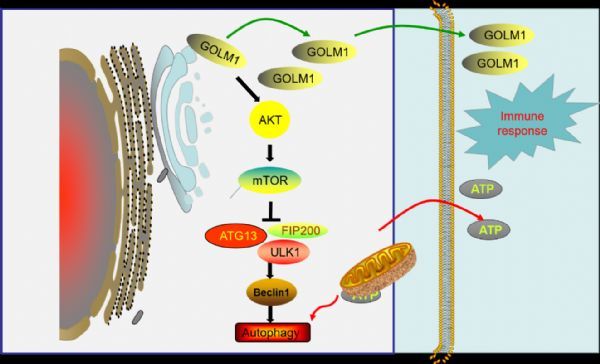
提出的Golm1调控抗肿瘤免疫的工作模型
图片来源:https://doi.org/10.1038/s41392-021-00673-6
综上所述,作者发现肿瘤细胞中GOLM1升高与肿瘤微环境中CD8 T细胞浸润减少和肝癌预后降低相关。更重要的是,作者已经证明了Golm1+/+癌细胞在免疫能力强的小鼠中比Golm1 /癌细胞生长肿瘤的速度快得多,但在免疫缺陷小鼠中生长速度相似,这表明Golm1在抑制抗癌免疫中具有一种新的作用。
该研究也提供了证据,表明GOLM1可能通过AKT/ mtor介导的自噬形成和细胞外ATP释放调控的潜在机制,抑制肿瘤微环境中的免疫反应,促进肿瘤生长。有趣的是,此前有人发现现GP73通过提高EGFP水平和促进STAT3磷酸化来上调PD-L1表达,表明GP73通过多种途径参与抗肿瘤免疫。因此,未来的研究需要进一步确定这些不同参与者之间的分子联系。然而,该研究确定GOLM1是HCC免疫治疗中一个重要的检查点阻断剂靶点。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。