《自然》子刊:可扩增筛选肿瘤新抗原特异性T细胞的技术,终于出现了
来源:奇点糕 2021-12-13 08:31
随着肿瘤的生长,机体的淋巴细胞会识别出这些异常的细胞,并浸润到肿瘤中,这就是我们常说的肿瘤浸润淋巴细胞(TIL)。TIL中有一部分是以肿瘤特异性新抗原为靶点的T细胞,这部分细胞具有很强的肿瘤杀伤能力。然而实际上,TIL的数量很少,且常常在肿瘤微环境中被抑制。那么,我们是否可以通过某些手段来特异性地识别和扩增TIL,从而实现肿瘤免疫治疗
随着肿瘤的生长,机体的淋巴细胞会识别出这些异常的细胞,并浸润到肿瘤中,这就是我们常说的肿瘤浸润淋巴细胞(TIL)。
TIL中有一部分是以肿瘤特异性新抗原为靶点的T细胞,这部分细胞具有很强的肿瘤杀伤能力。然而实际上,TIL的数量很少,且常常在肿瘤微环境中被抑制。
那么,我们是否可以通过某些手段来特异性地识别和扩增TIL,从而实现肿瘤免疫治疗的效果呢?
近日,来自瑞士洛桑大学的Alexandre Harari和George Coukos研究团队开发了一种名为NeoScreen的TIL体外扩增和筛选技术,这种方法可以特异性扩增识别肿瘤新抗原的TIL,为癌症的个性化免疫疗法提供了新方法,这一成果发表在《自然·生物技术》杂志上[1]。
在传统手段中,想要获得识别新抗原的T细胞,研究人员通常会从肿瘤中分离出TIL,并通过白细胞介素-2(IL-2)刺激T细胞的扩增。然而,由于这种扩增方法不具备特异性,而识别新抗原的T细胞比例非常低,因此,大量的非新抗原特异性的T细胞也会得到显着扩增,这样靶向新抗原的T细胞就可能被淹没在其中[2]。
那么,是否可以找到一种更加特异的扩增方法呢?
Harari、Coukos和他们的同事从抗原呈递过程中得到了启发。抗原呈递细胞(APC)向T细胞呈递肿瘤相关的抗原,并可驱动这些T细胞的激活和增殖。那么,是否可以基于自体APC对肿瘤中的TIL进行抗原选择性扩增呢?
说到APC细胞,大家最先想到的可能是树突状细胞,然而在这项技术中,研究人员选择了B细胞作为APC,因为相对于树突状细胞,B细胞更容易获取和扩增,而且更容易进行基因编辑。
研究人员首先分析了肿瘤细胞的基因组来鉴定蛋白质的随机突变片段,这些蛋白质片段可以作为新抗原被呈递。接下来,他们用这些蛋白质片段刺激改造后的B细胞,或者将编码这些片段的DNA转入B细胞中,让B细胞来呈递这些抗原。最后,他们将B细胞与肿瘤细胞以及从肿瘤中分离出来的TILs进行共培养。
在对TIL进行扩增之后,研究人员分离出这些TIL来鉴定它们识别的新抗原,并对识别新抗原的T细胞受体(TCR)的基因进行测序。
结果发现,NeoScreen在7例患者中鉴定了19个抗原表位。这19个表位中有9个表位,在NeoScreen中观察到的特异性TILs频率显着高于传统扩增方法。更重要的是,另外10个肿瘤抗原特异性TILs仅在NeoScreen中发现。
因此,在肿瘤抗原存在的情况下,经过改造的APCs能够使新抗原特异性CD8 T细胞大量扩增,从而建立了一种高度敏感和可复制的方法来识别肿瘤抗原。
不过,NeoScreen要做的不仅限于此,更重要的是,NeoScreen对于基于TCR的个体化过继T细胞疗法(ACT)还有着重要意义。
简单来说,ACT是指从患者体内分离T细胞,并在体外进行扩增,然后再回输到患者体内,从而达到杀伤肿瘤的目的。如果我们可以通过NeoScreen获得新抗原特异性的TCR,并将它们在患者的其他T细胞中表达,这样就能获得大量靶向肿瘤的T细胞。
体外实验表明,将TCR克隆进活化的原代T细胞中后,所有通过NeoScreen发现的针对新抗原的TCR均具有肿瘤反应性。
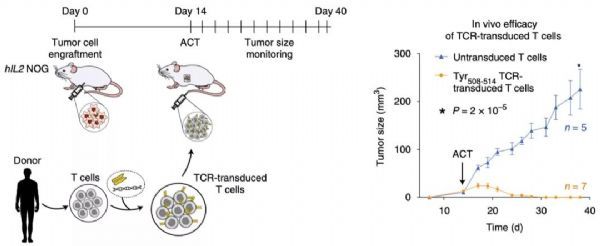
进一步地,研究人员通过小鼠异种移植瘤模型发现,在给小鼠过继回输表达新抗原特异性TCR的T细胞后,肿瘤的生长得到了显着抑制。
因此,NeoScreen鉴定的抗原特异性TCR在体外和体内试验中均表现出抗肿瘤反应,说明NeoScreen在基于TCR的个体化ACT治疗中具有良好的应用前景。
总的来说,这项研究报道了一种能够高度敏感地筛查肿瘤新抗原的方法,相比于传统手段,这一方法可以更加有效地扩增肿瘤新抗原特异的TIL。
此外,这一方法还能够高度敏感地鉴定肿瘤反应性TCR,从而为个性化改造T细胞,实现更加精准高效的肿瘤打击提供了可能。
本文的作者Coukos还提到:“NeoScreen还可以用于设计个性化的癌症疫苗,我们将进一步测试NeoScreen在癌症免疫治疗方面的这些应用。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。