Sci. Transl. Med: MeCP2相关的通路调节失调与强直性肌营养不良密切相关
来源:生物谷原创 2022-08-09 14:46
强直性肌营养不良1型(DM1)是由肌营养不良症蛋白激酶(DMPK)3‘端非翻译区(3’UTR)的微卫星CTG三核苷酸重复扩增引起的,其转录产物形成核核灶
强直性肌营养不良1型(DM1)是由肌营养不良症蛋白激酶(DMPK)3‘端非翻译区(3’UTR)的微卫星CTG三核苷酸重复扩增引起的,其转录产物形成核核灶,使CUG相互作用的RNA结合蛋白(RBPs),即肌盲样蛋白(MBNL)和CUGBP Elav样蛋白(CELF)产生失调。
虽然传统上被归类为肌病,但DM1是一种多系统疾病,也会导致神经功能障碍,大大降低患者的生活质量。成人发病的DM1的认知缺陷被认为是神经退行性的,部分原因是MBNL1/2隔离导致胎儿Tau亚型的重新表达。

图片来源: https://pubmed.ncbi.nlm.nih.gov/35767654/
近日,来自加州大学圣地亚哥分校的研究者们在Sci. Transl. Med杂志上发表了题为“MECP2-related pathways are dysregulated in a cortical organoid model of myotonic dystrophy”的文章,该研究提供了证据,表明早发性DM1可能涉及神经发育障碍相关的通路,并确定N-甲基-d-天冬氨酸(NMDA)拮抗剂是治疗DM1神经元缺陷的潜在途径。
强直性肌营养不良1型(DM1)是一种常染色体显性遗传性疾病,由肌营养不良症蛋白激酶(DMPK)基因3‘端非翻译区CTG微卫星重复序列扩增(MRE)引起。尽管DM1是最常见的成人起病的肌营养不良症,但先天性到青少年起病的DM1患者可以沿着自闭症谱系表现出衰弱的神经认知症状,其特征可能是宫内皮质缺陷。然而,CTG MRE导致这些发育中枢神经系统(CNS)表现的分子机制尚不清楚。
在本研究中,研究者发现在DM1患者诱导的多能干细胞(IPSCs)三维(3D)皮质器官成熟早期发现的CUG焦点导致CUGBP Elav样家族成员2(CELF2)蛋白过度磷酸化。完整的单细胞RNA测序和增强的交联和免疫沉淀(ECLIP)分析表明,CELF2蛋白-RNA底物相互作用的减少导致谷氨酸能神经元兴奋性突触信号关键基因的错误调节,包括甲基-CpG结合蛋白2(MECP2)途径的关键成分。
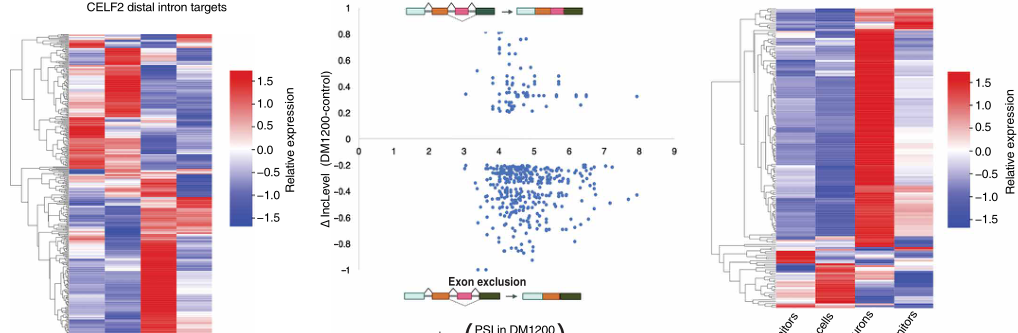
皮层神经元中CELF2蛋白-RNA相互作用的丧失扰乱了神经元兴奋性的调节
图片来源: https://pubmed.ncbi.nlm.nih.gov/35767654/
在本研究中,研究者报告了治疗DM1的潜在途径,包括使用RNA靶向基因疗法来消除有毒的CUG扩展的DMPK转录本,并表明正在开发的针对MECP2相关疾病的治疗方法也可能对DM1的早期神经表现有效。研究者证明了NMDA拮抗剂氢溴酸右美沙芬可以防止谷氨酸分泌和神经元丢失的毒性升高,并提出使用NMDA拮抗剂来治疗DM1的早发性中枢神经系统症状。(生物谷 Bioon.com)
参考文献
Kathryn H. Morelli et al. MECP2-related pathways are dysregulated in a cortical organoid model of myotonic dystrophy. Sci Transl Med. 2022 Jun 29;14(651):eabn2375. doi: 10.1126/scitranslmed.abn2375.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


