《BMC》发文:NCAS可作为饮食糖替代品
来源:生物探索 2021-02-18 12:27
糖尿病是一组以高血糖为特征的代谢性疾病,是现代疾病中的第二杀手,其对人体的危害仅次于癌症。因此遏制糖尿病的流行成为医学界研究的热点问题。“控糖限糖”是预防糖尿病最直接的方式,也是对甜食爱好者最“残忍”的方式。为解决这一难题,糖替代品——非卡路里人造甜味剂(NCAS)逐渐走进人们的生活。近日,《BMC》发布了一篇题为High-dose
糖尿病是一组以高血糖为特征的代谢性疾病,是现代疾病中的第二杀手,其对人体的危害仅次于癌症。因此遏制糖尿病的流行成为医学界研究的热点问题。“控糖限糖”是预防糖尿病最直接的方式,也是对甜食爱好者最“残忍”的方式。为解决这一难题,糖替代品——非卡路里人造甜味剂(NCAS)逐渐走进人们的生活。
近日,《BMC》发布了一篇题为High-dose saccharin supplementation does not induce gut microbiota changes or glucose intolerance in healthy humans and mice的文章,发现人和小鼠短期内食用糖精量在最大可接受水平(ADI)时,不会改变其肠道菌群稳态或引起葡萄糖耐受不良。
研究者进行了一项随机、双盲、安慰剂对照的干预研究,探讨了纯糖精化合物(NCAS的一种)对肠道菌群和葡萄糖耐量的影响。他们首先招募了54名志愿者,并将其随机分成安慰剂组、糖精组、STRs抑制剂组以及糖精+ STRs抑制组,根据ADI(62 mg / d)的计量标准连续服用干预剂2周。研究发现参与者的体重并为发成变化。
同时,考虑到涉及人类志愿者治疗剂量和持续时间的安全性限制,研究人员构建小鼠模型对实验进行进一步的探讨。研究人员设计每日喂养野生型和T1R2-KO小鼠(C57B1 \ 6J)饮用纯糖精10周,其摄入量是正常人体ADI标准的4倍。且糖精干预前后,小鼠体重并无明显差异。结果证明,人和小鼠的糖耐实验(OGTT)的结果并不受其纯糖精摄入的影响。
但在2014年,《nature》发布的一篇文章曾提出,NCAS可能通过肠道菌群诱导葡萄糖耐受不良,自那以后,NCAS的安全性引起了大众的怀疑。
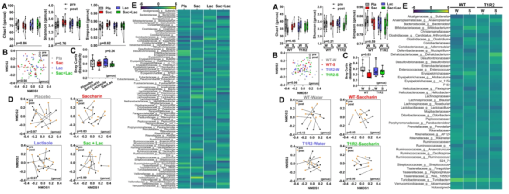
为了验证这一观点,研究人员基于NGS平台对人和小鼠的粪便样品进行了16S rRNA基因测序,以评估微生物群落之间的治疗效果以及受试者对治疗的反应。为了严格控制变量,实验在进行干预之前,所有治疗组参与者的肠道菌群α多样性,β多样性,物种丰富度,生物分类多样性和均一性均相似。治疗前后的测序结果显示:微生物α多样性相似;MDS图
有显示出明显的聚类;用ANOVA或Kruskal-Wallis检验评估Bray-Curtis差异和UniFrac距离,无明显变化;微生物单个分类单元的相对丰度物无特定变化。最后,研究人员通过线性判别分析(LEfSe)确定治疗模型并未产生任何差异调节的特征。这些结果表明,纯糖精补充剂不会在人类和小鼠任何分类学水平上改变微生物多样性或组成。
尽管糖精的干预并未在人或小鼠中引起肠道群落的实质性变化,但研究者猜测,糖精是否可以通过进行粪便样品的非靶向代谢组学来改变肠道的代谢特性呢?
由于NCAS是甜味受体(STRs)的真正配体,而T1R2是一种甜味受体蛋白,因此研究者推测,STRs介导的化学感受能在胃肠道产生NCAS,且肠道菌群和代谢调节之间可能存在某种关联机制。
于是研究者通过使用正交偏最小二乘判别分析(OPLS-DA)野生型和T1R2-KO小鼠的粪便代谢产物在治疗前后的变化,并使用液相色谱串联质谱法(LC / MS)测量了粪便中的SCFA,结果发现,粪便代谢产物或短链脂肪酸(SCFA)等微生物活性读数未显示出干预前后的差异。且具有STRs基因消融作用的小鼠的糖耐结果和肠道菌群没有出现异常。但是我们发现野生型小鼠的粪便代谢组学具有年龄依赖性,而T1R2-KO型小鼠并没有出现这种情况。
尽管研究存在以糖精为NCAS代表进行测试证据不足、干预时间短不足以诱发生理效应、研究样本量小等明显的局限性。但临床意义不容小觑,未来治疗糖尿病的突破口也许就在眼前!(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


