eBioMedicine | 中山大学罗镇华/冯旭阳/刘钧澄团队揭示黏膜相关恒定T细胞促进胆道闭锁疾病的胆管反应新机制
来源:生物探索 2024-05-11 10:50
该研究创新性构建体外细胞共培养模型,通过单细胞测序分析,发现这一系统的淋巴细胞群比例变化、基因表达谱与BA疾病相一致,可以模拟BA免疫微环境。

胆道闭锁(Biliary atresia, BA)是一种严重的新生儿胆道疾病,胆管细胞损伤导致肝内外胆管阻塞,导致胆汁淤积,并造成肝纤维化。虽然肝门肠吻合手术可以帮助胆汁引流,提高短期疗效,但是,无论胆汁引流恢复程度如何,免疫介导的胆管损伤仍然持续存在,而且与成人肝病相比,术后BA的肝纤维化进展迅速,导致术后两年内,至少75%的患儿将快速发展为肝硬化,需要进行肝移植。胆管细胞损伤后,免疫应答启动,同时,胆管细胞增殖、肝脏祖细胞激活分化为反应性胆管细胞,参与组织修复。如果胆管细胞损伤持续存在,超过其自我修复过程,那么,胆管细胞异常增殖,并通过与各种浸润的免疫细胞相互作用诱导慢性炎症,最终导致肝脏的血管生成和纤维化,整个过程称为胆管反应(Ductular Reaction, DR)。
最初的免疫反应引起胆管细胞损伤和凋亡,随后,免疫反应一直持续到促纤维化反应的发生,最终免疫反应和胆管反应共同导致了肝纤维化。这其中胆道闭锁的免疫环境如何促进胆管反应和共同导致肝纤维化的发生是领域研究的热点。黏膜相关恒定T细胞(MAIT细胞)是一群非传统的T细胞亚群,在肝脏中非常丰富,占肝内T细胞的15-45%,功能多样,既有抗菌、抗病毒宿主防御作用,又可促进组织修复和维持稳态。目前,MAIT细胞是否参与胆道闭锁的免疫反应尚不清楚。
作者探索MAIT细胞在胆道闭锁疾病中的功能,发现BA肝脏MAIT细胞高水平与低生存、胆管增殖和肝纤维化相关。进一步RNA测序分析显示,BA MAIT细胞呈现组织修复表型,上调组织修复相关生长因子AREG。机制研究表明,MAIT细胞通过AREG促进胆管细胞增殖和胆管类器官的生长,也促进和胆管类器官-LX-2混合模型的炎症因子和促纤维化分子表达。以上结果揭示,BA中MAIT细胞异常活化,高表达组织修复相关基因AREG,促进胆管反应。AREG高表达的MAIT细胞可以作为BA治疗的潜在靶点。
该研究创新性构建体外细胞共培养模型,通过单细胞测序分析,发现这一系统的淋巴细胞群比例变化、基因表达谱与BA疾病相一致(图1),可以模拟BA免疫微环境。该模型首先通过RRV感染胆管细胞,随后与外周血单个核细胞共培养,建立方法相对简单,克服胆道闭锁疾病临床标本稀少的限制。因此,该系统可广泛应用于研究,有望成为研究胆道闭锁病理机制的新型工具。
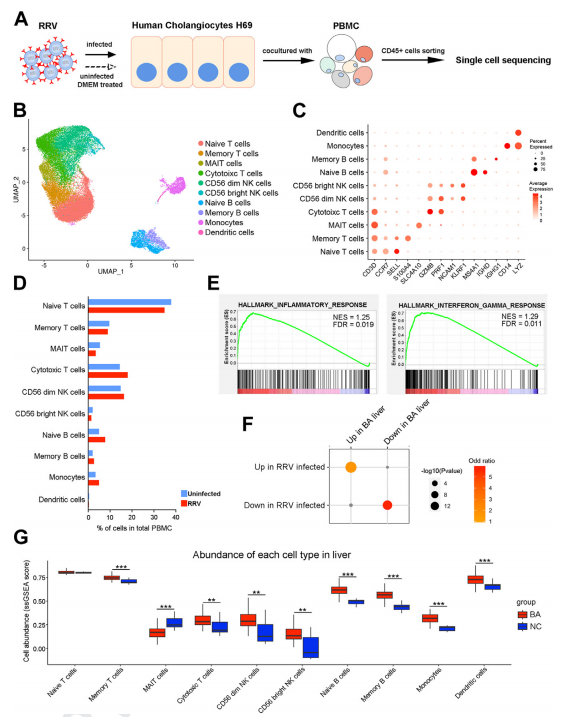
RRV感染胆管细胞的体外细胞共培养模型模拟BA的免疫微环境(Credit: eBioMedicine)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


