AlphaFold3来了!预测几乎所有分子结构,带来药物研发新范式
来源:智药局 2023-11-03 13:31
虽然新的AlphaFold预示着一个充满前所未有可能性的时代,但必须承认它的局限性。
2020年底,谷歌旗下公司DeepMind推出的AlphaFold2震惊了业界,改变了人们对蛋白质及其相互作用的理解方式。
2021年11 月 4 日,谷歌母公司Alphabet在英国成立了一家名为Isomorphic Labs的新药研发公司。
2023年10月31日,Deepmind联合Isomorphic Labs共同发布了新一代AlphaFold模型,有望改变药物发现的游戏规则。
新一代AlphaFold可以预测蛋白质数据库(PDB)中几乎任何分子的结构,通常具有原子精度,包括配体(小分子)、蛋白质、核酸(DNA 和 RNA)以及含有翻译后修饰 (PTM) 的生物分子。
该模型的扩展功能和性能有助于加速生物医学的突破,并实现“数字生物学”的下一个时代,为疾病通路、基因组学、潜在治疗靶点、药物设计机制以及实现蛋白质工程和合成生物学的新平台的功能提供新的见解。
Isomorphic Labs 正在将下一代AlphaFold模型应用于治疗药物设计。
超越蛋白质折叠
AlphaFold是单链蛋白预测的根本性突破。紧接着,AlphaFold-Multimer扩展到具有多条蛋白质链的复合物,随后是 AlphaFold2.3,后者提高了性能并将覆盖范围扩大到更大的复合物。
2022 年,AlphaFold与EMBL的欧洲生物信息学研究所合作,通过AlphaFold蛋白质结构数据库免费提供几乎所有科学已知的编目蛋白质的结构预测。
迄今为止,已有190多个国家的4万用户访问了AlphaFold数据库,世界各地的科学家已经利用AlphaFold的预测来帮助推进各种研究。
DeepMind展示了 AlphaFold 在预测蛋白质折叠之外的准确结构方面的卓越能力,从而在配体、蛋白质、核酸和翻译后修饰方面生成高度准确的结构预测。
对于蛋白质-核酸界面,新版本的AlphaFold优于RoseTTAFold2NA等同类模型,而对于RNA结构预测,它优于其他AI方法,但略微落后人类专家。
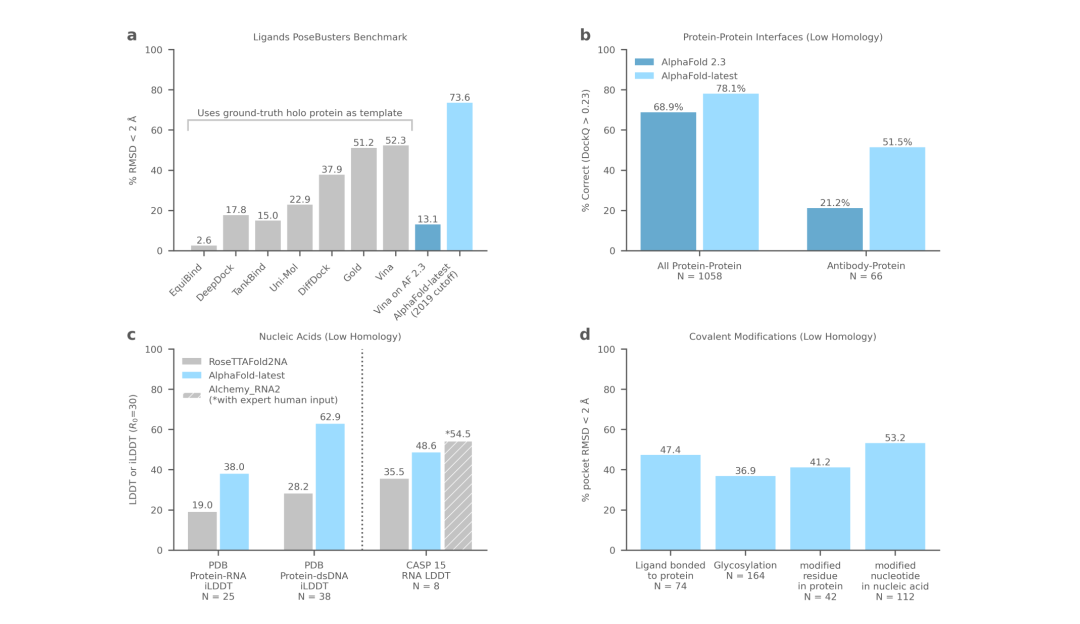
研究人员强调,AlphaFold并不是从头开始解决这些结构,而是从大量实验确定的结构中推断模式。
尽管如此,它适应新分子类别建模的灵活性凸显了支撑最近人工智能突破的泛化能力。
02
加速药物发现
早期分析还表明,新一代AlphaFold模型在一些与药物发现相关的蛋白质结构预测问题上大大优于AlphaFold2,例如抗体结合。
准确预测蛋白质-配体结构是药物发现的一个非常有价值的工具,因为它可以帮助科学家识别和设计可能成为药物的新分子。
目前的行业标准是使用“对接方法”来确定配体和蛋白质之间的相互作用。这些对接方法需要刚性参比蛋白结构和配体结合的建议位置。
DeepMind最新模型为蛋白质-配体结构预测设定了新的标准,在预测蛋白质-配体相互作用方面,新AlphaFold的性能比传统方法高出约20%,并且还可以预测尚未进行结构表征的全新蛋白质。
它还可以联合模拟所有原子的位置,使其能够代表蛋白质和核酸在与其他分子相互作用时的全部固有灵活性, 这是使用对接方法无法实现的。
例如,在PORCN、KRAS、和PI5P4Kγ的验证中,AlphaFold最新模型的预测结构与实验确定的结构非常匹配:
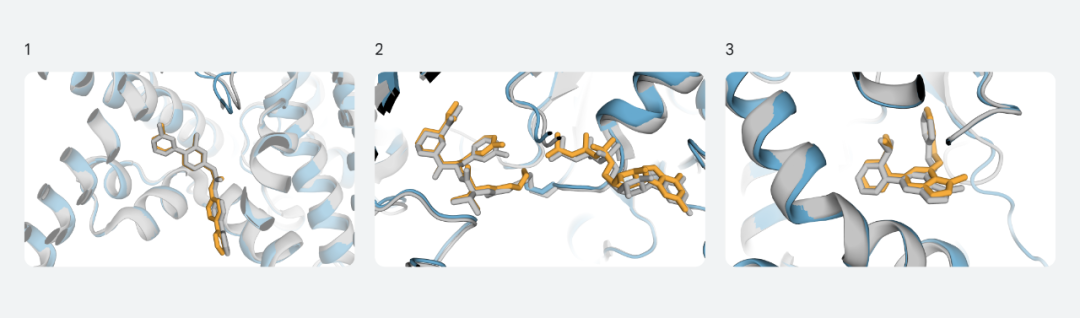 图:PORCN (1)、KRAS (2) 和 PI5P4Kγ (3) 的预测
图:PORCN (1)、KRAS (2) 和 PI5P4Kγ (3) 的预测
Isomorphic Labs 正在将下一代 AlphaFold 模型应用于治疗药物设计,帮助快速准确地表征对治疗疾病很重要的多种类型的大分子结构。
对生物学的新认识
通过解锁蛋白质和配体结构以及核酸和包含翻译后修饰的模型,新一代AlphaFold基础生物学提供了一种更快速、更准确的工具。
一个例子涉及与crRNA和DNA结合的Cas12l结构,crRNA和DNA是CRISPR家族的一部分。Cas12l的较小尺寸可能允许其更有效地用于基因组编辑。
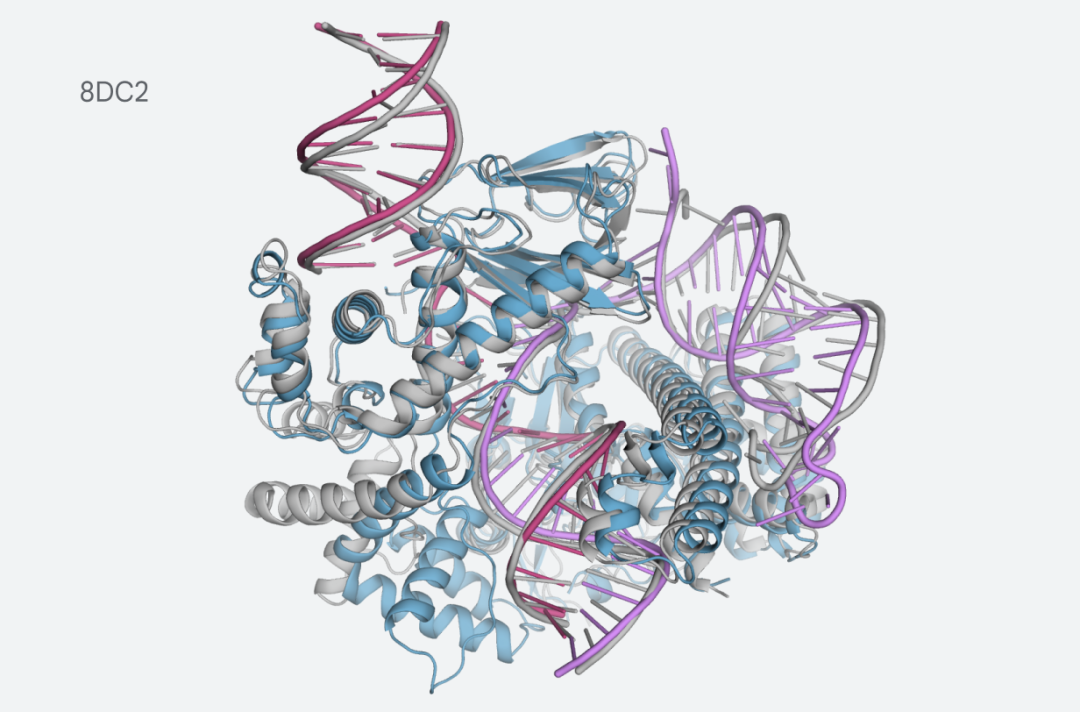
最新版本的AlphaFold能够模拟这些复杂的系统,展示了人工智能可以帮助更好地理解这些类型的机制,并加速它们在治疗应用中的应用。
AlphaFold 3的推出代表了分子建模和药物发现的巨大飞跃。凭借其预测复杂分子结构和相互作用的能力,它有望彻底改变制药市场。
虽然新的AlphaFold预示着一个充满前所未有可能性的时代,但必须承认它的局限性。
在一份综合白皮书中,DeepMind和Isomorphic Labs研究人员坦诚地讨论了该系统的优点和缺点。
值得注意的是,该系统在预测RNA分子的结构方面存在缺陷,不过,DeepMind和Isomorphic Labs都在努力应对这一挑战,进一步巩固他们对改变分子生物学格局的承诺。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


