MedComm:韩欣欣等开发患者来源的携带免疫系统和血管的卵巢癌类器官
来源:生物世界 2024-10-14 09:33
在这项新研究中,研究团队开发了一种新方法,可以快速从新鲜获取的肿瘤样本中创建卵巢癌类器官,使用特定培养基,无需进行单细胞分离。
近日,上海礼升生物韩欣欣、蔡春晖,复旦大学附属妇产科医院曹琦等人在 MedComm 期刊发表了题为:Patient-derived ovarian cancer organoid carries immune microenvironment and blood vessel keeping high response to cisplatin 的研究论文。
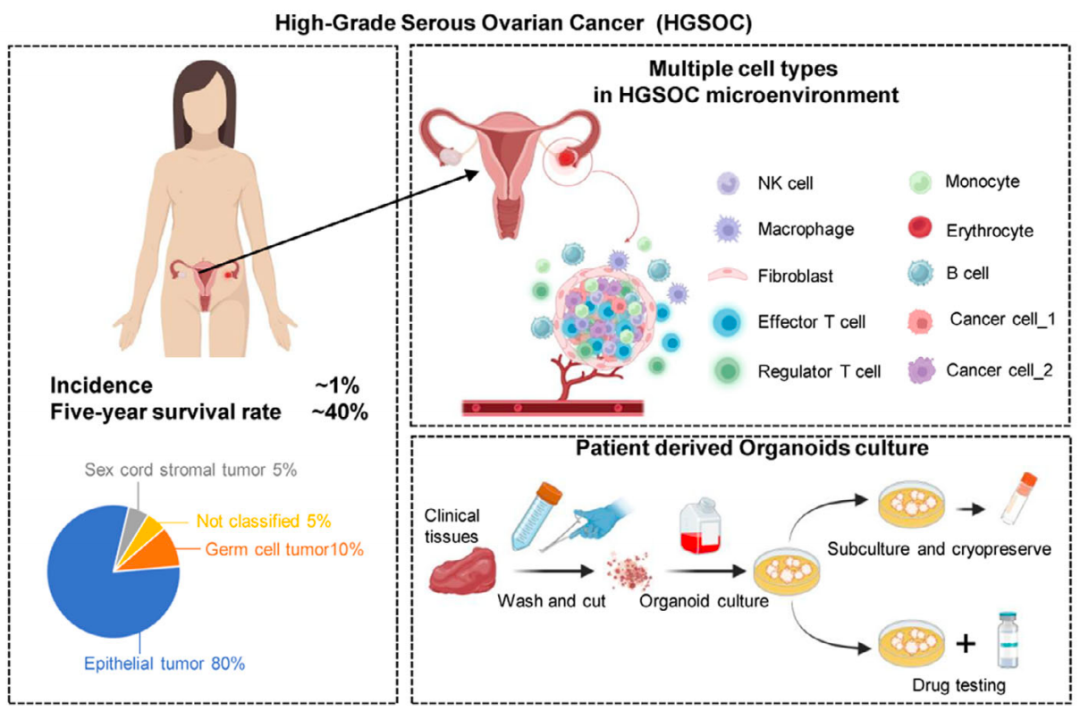
该研究从卵巢癌患者样本中开发了一种新型高级别浆液性卵巢癌(HGSOC)类器官系统,其能够再现高级别浆液性卵巢癌的组织学和分子异质性,同时保留了关键的免疫微环境和血管,这一点可以通过CD34+内皮细胞的存在得到证明。全外显子测序确定了关键基因突变(CSMD3、TP53、GABRA6)。类器官在测试对卡铂和紫杉醇产生耐药性的患者对顺铂的敏感性方面显示出潜力,免疫微环境与血管的整合为免疫疗法和血管生成抑制剂等新型疗法提供了更大的潜力。总的来说,该研究可能为卵巢癌的检测系统和理论基础提供新见解,并为个体化癌症治疗提供依据。

高级别浆液性卵巢癌(HGSOC)因其具有侵袭性和高复发率的特点,体现了通用治疗策略的局限性。这种情况凸显了个性化治疗方案的迫切需求,这种方案基于对个体肿瘤生物学和患者对各种疗法的特异性反应模式的深入理解。影响肿瘤行为的遗传、分子和环境因素的复杂相互作用需要我们从传统的治疗模式转向更加个性化的策略。
类器官技术的出现为精准医学提供了一种开创性方法,该技术可将患者来源的肿瘤细胞培养成与原始肿瘤的细胞异质性、基因组特征和微环境密切复制的三维结构。通过实现高保真度的疾病模型和药物反应测试,类器官有可能改变卵巢癌的治疗格局,为高度个体化和有效的治疗策略铺平道路。这种方法不仅提高了治疗的疗效,而且将不良反应和耐药的发生风险降至最低。
在卵巢癌研究领域,准确反映高级别浆液性卵巢癌(HGSOC)复杂生物学的模型仍然是一个关键挑战。
在这项新研究中,研究团队开发了一种新方法,可以快速从新鲜获取的肿瘤样本中创建卵巢癌类器官,使用特定培养基,无需进行单细胞分离。在此基础上,研究团队建立了一个小型卵巢癌类器官生物库,并通过全面的组织学、分子和基因组评估证明,这些类器官密切反映了肿瘤之间和肿瘤内部观察到的异质性。这些类器官忠实地保留了其来源的肿瘤的关键特征,包括特定的免疫细胞标记和血管内皮标记,从而证明了类器官平台先进的方法学设计和生物学保真度。
该研究精心设计了这些类器官,携带了一系列可通过单细胞RNA测序(scRNA-seq)识别细胞标志物,有助于深入了解HGSOC的细胞异质性。这包括识别特定的免疫细胞标记和血管内皮标记,这对于理解肿瘤微环境中的相互作用至关重要。例如,在这些类器官中发现T细胞的CD4、CD8A和CD8B以及内皮细胞的PECAM1、CD34和CDH5提供了对肿瘤免疫景观和血管网络的细致了解。这种全面的描述体现了开发能够紧密模拟卵巢恶性肿瘤复杂生物学景观的模型。
该研究的核心是将这些类器官应用于评估化疗药物顺铂的反应性,特别是对于之前接受过卡铂和紫杉醇治疗的患者。这种方法产生了与患者个体反应高度一致的见解,从而为解决标准化疗方案的耐药性问题提供了预测性框架。这证明了该研究开发的卵巢类器官在促进个性化治疗策略方面的实用性,标志着朝着精准肿瘤学迈出了一步。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


