Immunity: Foxp3通过IL-2介导胸腺Treg细胞免疫耐受活性的形成
来源:本站原创 2021-04-12 02:00
调节性T(Treg)细胞在建立和维持免疫耐受中起着至关重要的作用。大多数Treg细胞表达CD25分子(IL-2R受体),它与白介素IL-2之间存在高亲和力,CD25激活后通过诱导转录因子STAT5的激活来发出信号。 IL-2在Treg的细胞生物学的多个方面起着核心作用。
2021年4月12日讯/生物谷BIOON/---调节性T(Treg)细胞在建立和维持免疫耐受中起着至关重要的作用。大多数Treg细胞表达CD25分子(IL-2R受体),它与白介素IL-2之间存在高亲和力,CD25激活后通过诱导转录因子STAT5的激活来发出信号。 IL-2在Treg的细胞生物学的多个方面起着核心作用。
除TCR信号,Treg细胞的分化还需要IL-2 – STAT5诱导Foxp3表达。 Foxp3是Treg的标志性转录因子,其在分化的Treg细胞中持续表达是Treg细胞谱系稳定性和功能所必需的。此外,在成熟的Treg细胞中,IL-2R信号传导支持其持久性和免疫抑制能力。
此前研究表明, Treg细胞分化需要通过“两步法”模型,其中相对较强的TCR刺激在前体细胞中诱导CD25表达,从而使其接受随后的IL-2刺激,最终诱导Foxp3表达。与该模型一致,由自身反应性CD4SP胸腺细胞产生的IL-2可限制胸腺中Treg细胞的分化。
IL-2 – STAT5信号诱导并维持Foxp3表达的事实表明,该途径直接作用于Foxp3基因。然而,鉴于IL-2信号在数百个靶标上具有多效性转录作用,人们仍然不清楚IL-2 – STAT5途径在多大程度上直接作用于Foxp3基因,从而影响了Treg的表达。先前研究揭示了Foxp3基因簇中的CNS2(保守的非编码序列2)内部的内含子增强子元件能够与STAT5结合,该过程是成熟Treg细胞中维持Foxp3表达的必需条件,但对其诱导则是可有可无的。因此,在 DNA去甲基化激活CNS2之前,IL-2 – STAT5信号传导必须在Treg前体细胞中诱导Foxp3表达。
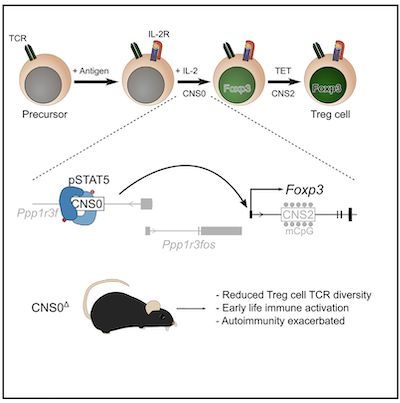

(图片来源:www.cell.com)
在最近一项研究中,来自美国St. Jude儿童医院的Yongqiang Feng团队鉴定出了STAT5结合的增强元件并探索了其生物学功能。相关结果发表在免疫学权威杂志《Immunity》上。
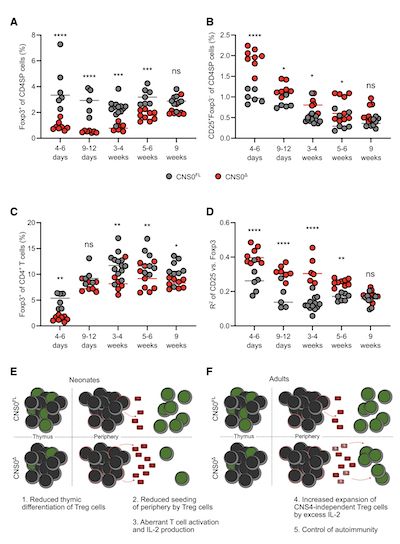
事实证明,这种保守的调控元件与先前确定的SATB1(CNS0)和MLL4结合位点(–8.5kb MLL4)基本重叠。尽管已经证明了SATB1在胸腺Treg细胞分化中的作用,但尚未验证SATB1结合该区域的重要性。鉴于SATB1的全基因组结合,尚不清楚哪种Foxp3增强子解释了SATB1的功能。同样,MLL4与该区域的结合已显示出促进体外Treg细胞极化的作用,但其在体内的作用仍不清楚。

(图1,CNS0缺陷影响Treg细胞分化)
使用小鼠遗传模型,作者观察到CNS0的缺失导致胸腺Treg细胞生成的选择性损伤和外周Treg细胞数量的减少,该现象在围产期最为明显。随着年龄的增长,这种缺陷得以缓解,这可能是由于外周Treg细胞扩增所致。虽然删除这种增强元件会导致免疫力持续轻微增加,而不会产生明显的自身免疫,但是当与Aire缺乏同时存在时,它会显著增强自身免疫。研究结果表明,这种IL-2 – STAT5反应元件可确保在出生后早期实现强大的Treg细胞分化,并通过与其他耐受机制协同作用使自身免疫性疾病得到最大程度的缓解。(生物谷 Bioon.com)
原始出处:Stanislav Dikiy, Jun Li, Lu Bai. et al., A distal Foxp3 enhancer enables interleukin-2 dependent thymic Treg cell lineage commitment for robust immune tolerance. Immunity (2021). DOI:https://doi.org/10.1016/j.immuni.2021.03.020
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


