Nature子刊:间充质干细胞治疗瘫痪,临床试验结果积极
来源:生物世界 2024-04-07 10:40
该论文介绍了CELLTOP试验所有的10名参与者的入组和96周随访结果。证明了自体AD-MSC的采集和鞘内注射给药在脊髓损伤治疗中的安全性。
梅奥医学中心的研究人员在 Nature Communications 上发表了题为:Intrathecal delivery of adipose-derived mesenchymal stem cells in traumatic spinal cord injury: Phase I trial 的研究论文。
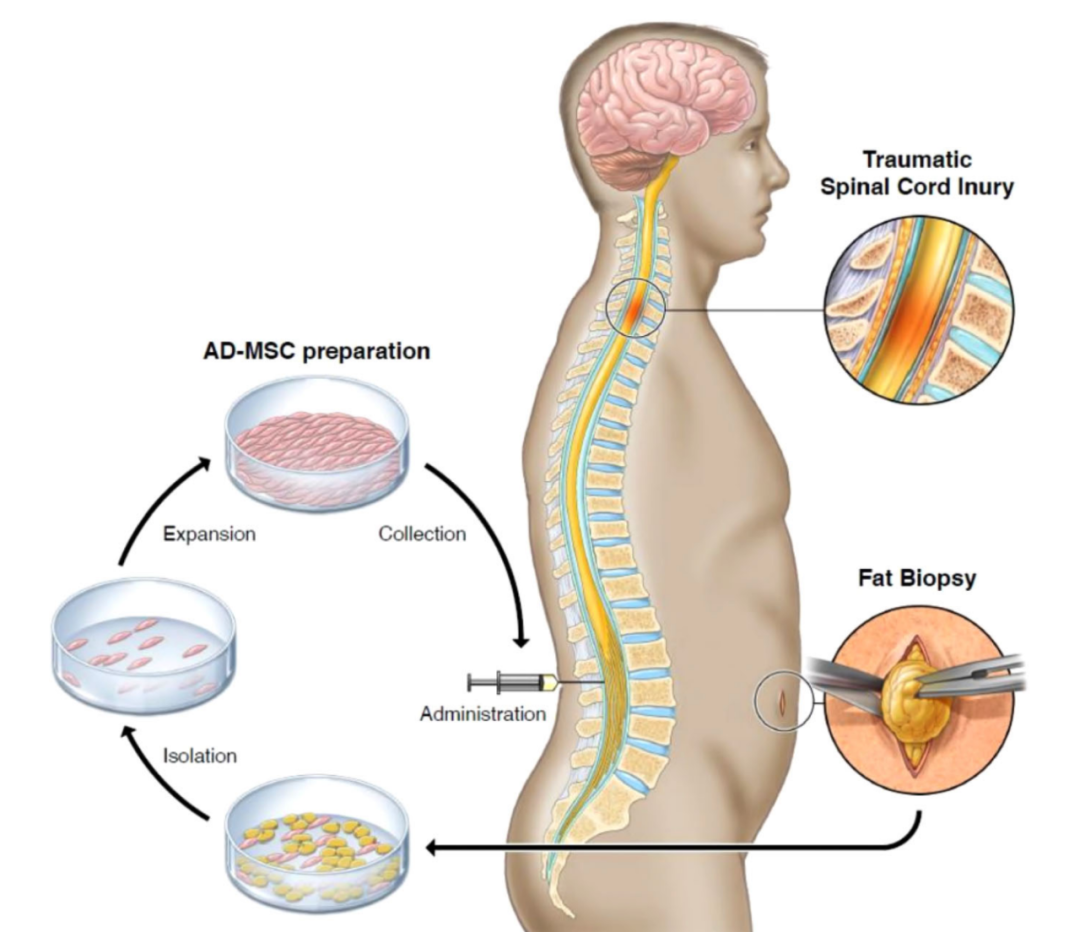
鞘内注射自体培养扩增的脂肪组织来源的间充质干细胞(AD-MSC)可用于治疗创伤性脊髓损伤(SCI)。在10名接受治疗的脊髓损伤患者中,微观察到严重不良事件,在治疗后两年内的随访中,有7名患者的ASIA评定量表(一种常用的脊髓损伤评估表)等级较治疗前有所改善。该临床试验达到了主要终点,表明了AD-MSC的采集和鞘内注射给药在创伤性脊髓损伤患者中是安全、可耐受的。

脂肪组织是间充质干细胞最主要的来源,即脂肪来源的间充质干细胞(AD-MSC),其具有由于其可获得性、易获取性和多能性等优点。在创伤和退行性疾病中,AD-MSC的使用已经被深入研究。在脊髓损伤的动物模型中进行的临床前试验表明,AD-MSC可以调节炎症反应并促进再生环境。
该团队在2020年报告了一位接受鞘内注射AD-MSC的脊髓损伤患者的案例,患者在经过一段时间的神经平台期后表现出显著的运动和感觉改善。
该患者参加的是异性名为CELLTOP的1期临床试验(临床试验编号NCT03308565),该临床试验使用患者自体脂肪来源的间充质干细胞(AD-MSC)治疗因创伤性脊髓损伤而瘫痪的人,共有10名患者参与,以验证该疗法的安全性、可行性和生物学效应。
该论文介绍了CELLTOP试验所有的10名参与者的入组和96周随访结果。证明了自体AD-MSC的采集和鞘内注射给药在脊髓损伤治疗中的安全性。在研究期间,没有报告任何严重不良事件,并且10名患者中7名经历了运动和/或感觉的改善。
在这项临床试验中,10名参与者因机动车事故、跌倒或其他原因导致脊髓损伤。其中6人颈椎损伤,4人胸椎损伤,他们参与临床试验时的年龄范围为18-65岁。研究团队从他们的腹部或大腿处取少量脂肪组织,从中收集间充质干细胞。在实验室中将这些脂肪来源的间充质干细胞(AD-MSC)扩增至约1亿个细胞,然后通过鞘内注射将这些干细胞注射到患者的脊髓腔。在治疗后的两年内,每位参与者在梅奥医学中心接受了10次评估。
脊髓的修复细胞或制造新细胞的能力有限。脊髓损伤患者通常在受伤后的6-12个月内经历大部分恢复,而在12-24个月,这种修复和改善通常就停止了。该临床试验的一个意外结果是,两名颈部颈椎损伤的患者在受伤22个月后接受了干细胞治疗,并在治疗后ASIA评定量表(一种常用的脊髓损伤评估表)提高了一个等级。而在3名胸椎完全损伤(他们在胸部以下位置完全没有感觉或运动能力)的患者中有2名在治疗后ASIA评定量表提高了两个等级,恢复了损伤部位以下身体的一些感觉和运动控制。
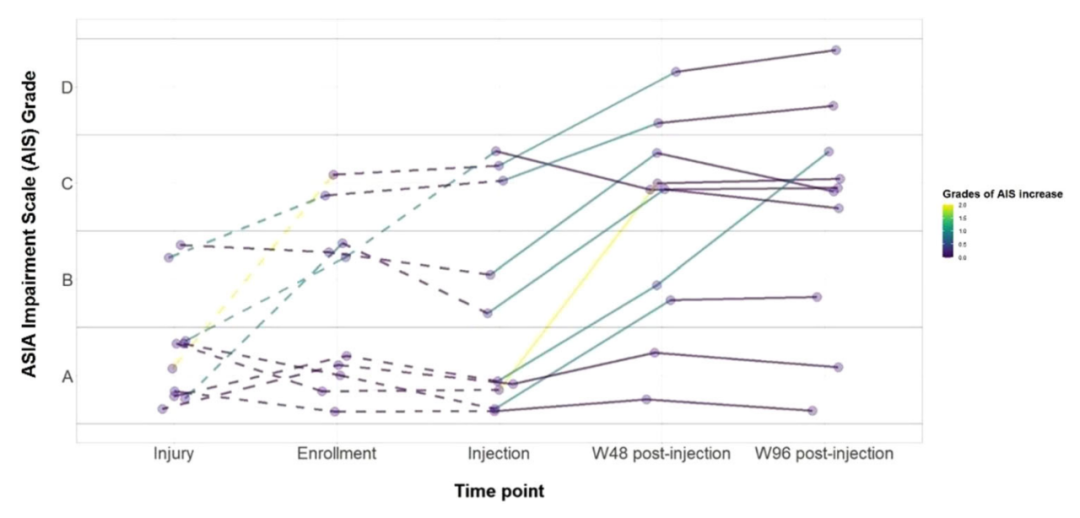
研究团队表示,对于脊髓损伤患者,即使是轻微的改善也可以显著提高患者的生活质量。研究团队下一步的目标是评估干细胞疗法的有效性以及哪些患者最受益。目前团队正在进行一个更大的随机对照临床试验,随机分配患者接受干细胞治疗或不含干细胞的安慰剂。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


