Cell Stem Cell:陈水冰团队构建基于人iPS干细胞的GWAS研究平台
来源:生物世界 2022-10-11 10:39
全基因组关联研究(Genome-Wide Association Studies,GWAS)是指在基因组水平进行大量样本与复杂疾病和性状的关联性分析,从而全方位地分析疾病的发生发展机制
全基因组关联研究(Genome-Wide Association Studies,GWAS)是指在基因组水平进行大量样本与复杂疾病和性状的关联性分析,从而全方位地分析疾病的发生发展机制,筛选出与疾病相关的致病基因及变异位点,即单核苷酸多态性(SNP)。在 GWAS 分析中,为了体现所分析的疾病和性状的遗传结构,研究人员往往需要收集大量相关样本,因此这类研究普遍耗费大量的经济和人力成本。此外,由于收集传染性疾病患者样本具有挑战性以及缺乏明确定义的健康对照组样本,传染性疾病相关的 GWAS 研究非常具有挑战性。
与此相比,基于细胞培养的实验平台由于其可控性,能够较大限度地减少个体间由于生活习惯、饮食和环境等引起的差异,因此可以使用相对较小的样本规模进行 GWAS 研究,并能够为传染性疾病的研究提供安全的实验平台和精准的分析结果。
2022年10月6日,美国康奈尔大学威尔医学院陈水冰教授和韩玉岭博士等在 Cell Stem Cell 期刊发表了题为:A human iPSC-array-based GWAS identifies a virus susceptibility locus in the NDUFA4 gene and functional variants 的研究论文。
该研究首次构建了基于人诱导多能干细胞(hiPSCs)进行全基因组关联研究(GWAS)研究的平台,鉴定到一系列与寨卡病毒(ZIKV)感染相关的单核苷酸多态性(SNP)及调控基因NDUFA4,并深入研究了NDUFA4正向调控病毒感染的分子机制。

与传统 GWAS 研究使用的淋巴细胞系相比,诱导多能干细胞(iPSCs)的基因组更稳定,能够更真实地反映个体的遗传信息。此外,iPSCs 能够分化为疾病相关的各种细胞类型,能更好地模拟 GWAS 相关疾病。最后,基于 CRISPR 的基因编辑技术可以将基因敲除或 SNP 定点突变引入 iPSCs,能够提供一个高通量平台,从功能上验证 GWAS 研究中鉴定的疾病相关 SNP 和基因。
在最新这项研究中,团队筛选了77个 hiPSCs 细胞系对 ZIKV 感染的敏感性。结果表明,不同个体来源的 iPSCs 对寨卡病毒的敏感性不同。结合 GWAS 分析,团队确定了 NDUFA4 及其相关 SNP 与 ZIKV 感染的易感性相关。为了研究 NDUFA4 在病毒感染中的功能,团队利用 CRISPR-Cas9 对 hiPSC 进行基因编辑,构架了 NDUFA4-/- iPSCs,携带非风险等位基因(T/T; T/T)与风险等位基因(G/G; C/C)的 iPSCs,以及敲除 NDUFA4 顺式调节区域的 NDUFA4Δ iPSCs,从而研究了 NDUFA4、SNP(rs917172和rs12386620)以及 NDUFA4 的顺式调节区域在 ZIKV 感染中的确切作用。团队发现,在不同 iPSCs 中,NDUFA4 的表达量与 ZIKV 的感染程度呈正相关。此外,团队还将 iPSC 分化为 ZIKV 感染相关的脑类器官(cerebral organoids),发现在不同 iPSCs 分化而来的脑类器官中 ZIKV 的易感性与在不同 iPSCs 中一致,具体体现在在 NDUFA4 敲除或者低表达(T/T; T/T)以及敲除 NDUFA4 顺式调控元件的细胞中,病毒感染水平显著降低。
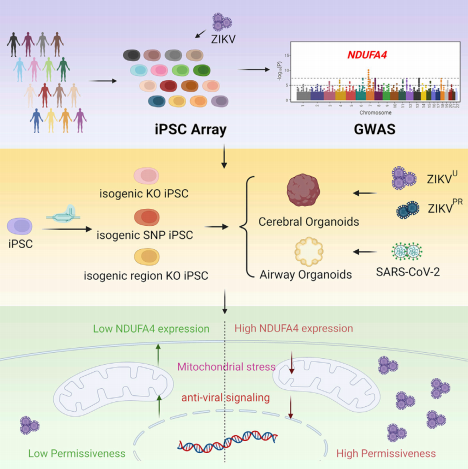
除了 ZIKV,团队还发现 NDUFA4 的缺失或减少也可导致其他黄病毒如登革病毒(DENV) 感染减少。利用 iPSCs 分化的肺类器官,团队同样发现 NDUFA4 的缺失或减少同样导致新冠病毒(SARS-CoV-2)感染水平的降低。对比健康人和 COVID-19 患者肺组织的转录组结果,发现 COVID-19 患者肺组织中 NDUFA4 的表达水平比未感染者更高。机制研究表明,NDUFA4 的缺失或减少会诱导线粒体应激,引起胞质内线粒体 DNA 的泄漏,从而导致先天免疫系统可以识别冗余的线粒体 DNA,诱导 I 型干扰素信号通路上调以阻断病毒感染。
该研究首次构建了基于 hiPSCs 进行 GWAS 研究的平台,该平台快速高效,低成本,不过分依赖样本数量,能够系统地评估遗传变异与疾病的关联。该研究还鉴定了 NDUFA4 及其相关位点/调节元件在病毒感染中的作用及机制。
康奈尔大学威尔医学院的韩玉岭博士、中科院深圳先进院的谭磊博士、斯隆-凯瑟琳癌症中心的周厅博士、康奈尔大学威尔医学院的杨柳柳博士和纽约大学的Lucia Carrau为论文共同第一作者,康奈尔医学院的陈水冰教授为论文通讯作者。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


