Cell:特殊免疫细胞ILC3s或能维持免疫系统和肠道微生物之间的“健康对话” 从而保护机体抵御结直肠癌发生
来源:本站原创 2021-09-04 18:01
来自康奈尔大学等机构的科学家们通过研究发现,ILC3s或能保护宿主机体抵御结直肠癌,其中部分原因是ILC3s能帮助维持机体免疫系统和肠道微生物之间的“健康对话”。
2021年9月4日 讯 /生物谷BIOON/ --结直肠癌是美国第四大最常见的癌症类型,每年大约有15万人被确诊,而且约有5万人会死于该病。尽管结肠镜筛查早期发下你这些癌症或癌前息肉非常有效,但晚期结直肠癌因治疗方法非常有限,对于患者和临床医生而言仍然是一大挑战;肿瘤学家非常关注这些肿瘤对免疫疗法产生的相对耐受性,这些疗法能通过增强宿主机体的免疫系统功能来攻击恶性细胞,从而就有望抵御其它癌症。
图片来源:https://www.sciencedirect.com/science/article/abs/pii/S0092867421008886
第三组先天性淋巴细胞(ILC3s,Group 3 innate lymphoid cells)能调节机体的免疫力和炎症,然而其在癌症发生过程中所扮演的关键角色研究人员却并不清楚;近日,一篇发表在国际杂志Cell上题为“Dysregulation of ILC3s unleashes progression and immunotherapy resistance in colon cancer”的研究报告中,来自康奈尔大学等机构的科学家们通过研究发现,ILC3s或能保护宿主机体抵御结直肠癌,其中部分原因是ILC3s能帮助维持机体免疫系统和肠道微生物之间的“健康对话”。
这篇研究结果表明,ILC3s在结直肠癌患者中往往会急剧减少并发生功能性改变,此外,通过实验性地破坏小鼠机体中ILC3s的功能或会导致侵袭性结肠癌的发生,并能明显降低癌症免疫疗法的效率。研究者Gregory Sonnenberg说道,本文研究为结直肠癌的临床治疗提出了新的可能性,也有助于帮助解释为何这类癌症往往不会对免疫疗法产生反应。
影响免疫疗法耐受性的一个因素可能是肠道微生物组,即生活在肠道中的细菌和其它微生物群落,其在正常情况下能帮助机体消化、支持多种代谢功能并在调节机体免疫系统功能上扮演关键角色。结直肠癌与慢性肠道炎症和正常微生物组的主要干扰直接相关,此外,最近研究还表明,患者机体的微生物组还在控制癌症免疫疗法的治疗结局上扮演着关键角色,其或能帮助解释为何有些患者对疗法有反应,而有些患者则没有反应。这篇研究报告中,研究人员分析了ILC3s的角色,其位于肠道中,能帮助调节机体免疫系统和肠道微生物之间的关联。
研究者Manish Shah说道,正常情况下ILC3s在维持下层肠道组织中微生物组和免疫环境之间的健康对话上扮演着关键角色。文章中,研究人员分析了来自人类和小鼠机体的结直肠癌肿瘤和癌前息肉组织,结果发现,与健康组织相比,来自癌变组织中的ILC3s相对较为贫乏,而且其功能还发生了进一步的改变。这或许是一个非常令人兴奋的研究发现,对于研究人员理解控制胃肠道恶性肿瘤的发病机制、进展以及治疗反应性具有非常重要的意义。
当肠道组织中正常ILC3s的活性丧失时,研究者观察到,ILC3s调节T细胞的能力会明显被干扰,ILC3s和T细胞之间对话的干扰也会进一步引起肠道炎症水平的增加,从而就会改变机体的肠道微生物组,这些肠道微生物的改变还会进一步诱导能抵御肿瘤的T细胞的水平发生下降。研究者指出,这些结果对于肿瘤的进展具有重大影响,在患结肠癌的小鼠机体中,阻断ILC3信号或会导致肿瘤的异常侵袭和恶性生长,且预后较差;当结肠肿瘤被植入到ILC3信号被阻断的小鼠机体中时,肿瘤就会对抗PD-1检查点阻断疗法的反应相对较差,而相同的肿瘤植入到正常ILC3信号的小鼠机体后,小鼠就会对疗法反应良好。
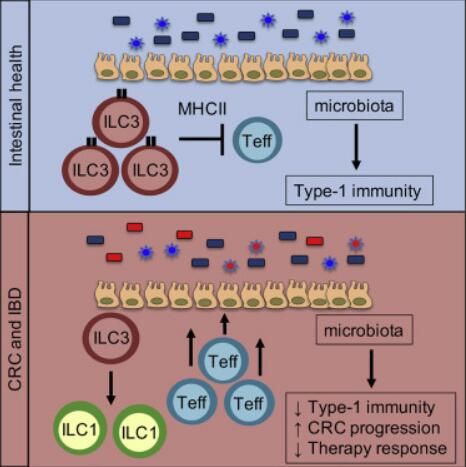
特殊免疫细胞ILC3s或能维持免疫系统和肠道微生物之间的“健康对话” 从而保护机体抵御结直肠癌发生。
图片来源:Jeremy Goc,et al. Cell (2021). DOI:10.1016/j.cell.2021.07.029
最后,在来自炎性肠病患者机体的结直肠活组织分析中,研究者发现,ILC3相关的异常或与结直肠癌患者机体表现出的异常相似;而将来自炎性肠病患者机体的微生物移植到小鼠机体中后就会介导其对疗法产生抗性,而移植了来自健康人类供体的微生物的小鼠则会对抗PD-1检查点阻断疗法产生反应。研究者Goc说道,更好地理解微生物组对癌症发育和疗法反应的贡献或许有望革命性地改变癌症患者的治疗管理策略;本文研究阐明了一种由微生物功能失调所驱动的疗法耐受性的机制,这种机制直到现在依然并未被很多科学家所重视,未来有一天研究人员或能利用肠道微生物来预测肿瘤的进展以及对免疫疗法的反应,甚至利用健康的微生物群落来改善疗法的反应。
目前研究人员正在努力识别出在这方面最有益的肠道菌群种类;综上,本文研究确定了ILC3s在癌症中的保护性角色,并揭示了ILC3s的固有破坏/干扰如何驱动机体适应性的免疫功能失调、肿瘤进展以及免疫疗法的耐受性发生等。(生物谷Bioon.com)
原始出处:
Jeremy Goc,Mengze Lv,Nicholas J.Bessman, et al. Dysregulation of ILC3s unleashes progression and immunotherapy resistance in colon cancer, Cell (2021). DOI:10.1016/j.cell.2021.07.029
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



