《神经元》:小胶质细胞“明修栈道”!科学家发现拯救神经元的隧道纳米管,清除垃圾并送来健康线粒体
来源:奇点糕 2024-10-11 09:35
神经退行性疾病的重要标志之一,就是病理性蛋白质聚集体积累。α-突触核蛋白(α-syn)和tau蛋白聚集体均表现出“类朊病毒”特性,在细胞间扩散并诱导临近神经元的蛋白质错误折叠,从而在相连脑区传播神经元损伤。
小胶质细胞是大脑先天免疫系统的一部分,在清除病理性蛋白质聚集体方面发挥着关键作用。人们认为,神经元细胞死亡后将病理性蛋白质聚集体释放到细胞外,之后才会被小胶质细胞识别并清除。
但是,来自卢森堡大学的研究团队发现,小胶质细胞可以通过隧道纳米管(TNT)与远距离的神经元建立连接,并通过TNT进行细胞器和蛋白质的快速交换。
病理条件下,小胶质细胞通过TNT将神经元中的毒性蛋白质聚集体转移,并为神经元输送健康线粒体,从而有效减轻神经元的病理负担,恢复神经元功能。
研究发表在《神经元》杂志上。
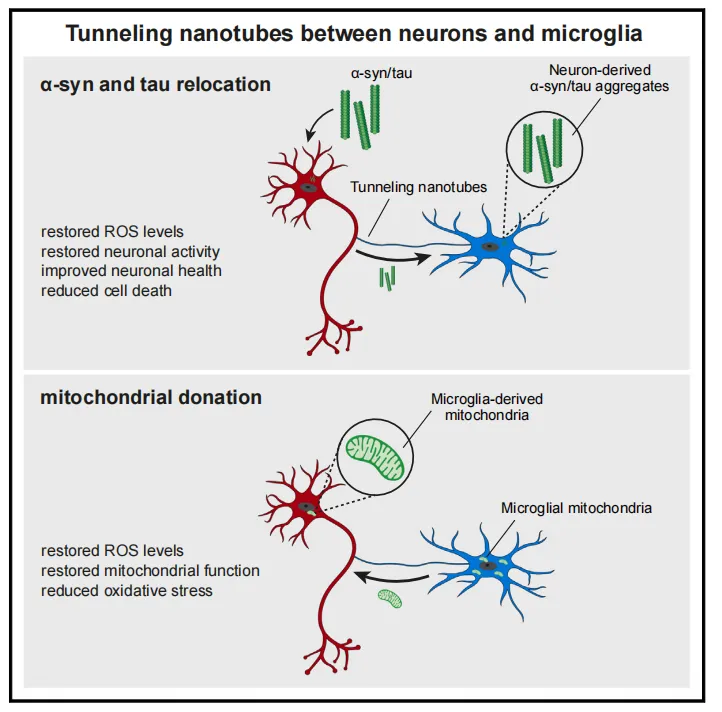
α-syn或tau聚集体可谓是让神经元吃尽了苦头。RNA测序显示,共有951个基因表达水平在毒性蛋白质聚集体存在时发生变化,尤其是线粒体功能相关基因,氧化应激水平增加,神经元功能受损甚至死亡。
在正常情况下,皮质神经元和小胶质细胞共培养,可以在细胞之间形成TNT,不同于小胶质细胞的其他伪足,TNT是自由悬浮状态,并且可以促进连接细胞之间的细胞成分交换。在病理条件下,毒性蛋白质聚集体积累使悬浮TNT数量增加,这些TNT中含有α-syn和tau免疫反应颗粒,表示正在进行毒性蛋白质的物质交换。
与单独培养的含有α-syn或tau的神经元相比,与小胶质细胞共培养可以显著降低神经元中的毒性蛋白质水平。
那么,毒性蛋白质被转移走之后的神经元,恢复健康了吗?
α-syn或tau积累与神经元网络活动下降或神经损伤有关。研究人员评估了神经元的Ca2+振荡,发现当小胶质细胞与神经元发生物理接触之后,原本α-syn诱导降低的Ca2+振荡频率重新升高。
不仅如此,TNT还可以将小胶质细胞中的健康线粒体运输至神经元中,弥补α-syn诱导的神经元线粒体破碎,使神经元中的ROS水平降低,有效减少神经元死亡。
接下来,研究人员尝试在小鼠和人体中验证TNT的存在。将含有α-syn的皮质神经元移植到小鼠皮质中,虽然可以看到被标记的α-syn从神经元转移至小胶质细胞,但是这条转移道路的特征和研究人员观察到的TNT存在一些出入。
无奈之下,研究人员在皮层网络机器智能(MICrONS)联盟数据集筛选了小鼠大脑皮层的连续切片电子显微镜图像,终于发现了TNT样开放式管状连接。在健康捐赠者和痴呆症患者的死后脑组织中,也观察到神经元和小胶质细胞之间存在大量TNT样接触。
根据以上实验结果,研究人员已经肯定,小胶质细胞的TNT是一种新型神经保护机制。那么在最需要神经保护的地方,也就是神经退行性疾病中,TNT是否正常发挥作用了呢?
在已知的神经退行性疾病相关基因变异中,携带LRRK2突变的小胶质细胞线粒体输送增加,但是对α-syn聚集体的转移减少;携带TREM2突变的小胶质细胞清除tau聚集体的效率下降,线粒体输送未受影响。总体而言,这些遗传变异损害了小胶质细胞对神经元的保护作用。
作者表示,“我们知道小胶质细胞在清除蛋白质聚集物方面发挥作用,但是最近才知道它们是通过纳米管远距离作业”,“这项研究不仅加深了我们对TNT进行细胞间通讯的理解,还挑战了小胶质细胞是神经炎症诱因的传统观点,强调了一种新的神经保护机制”。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


