长得胖不怪你,因为其实这也得拼爹! Nat Commun 最新研究:父亲在备孕期的饮食选择直接关系到未来子女的代谢状况和肥胖风险
来源:生物谷原创 2024-04-25 10:01
后代的肥胖与否,一定程度上也是一件拼爹的事,只有准父亲们保持健康的饮食习惯,后代才会更健康哦~
减肥太难了。都说要管住嘴,迈开腿。不过你有没有想过,光是管住自己的嘴还不够,可能还要穿越到出生前,管住爸爸们的嘴?
最近一份发表在《自然·通讯》上的研究表明,在备孕的时候,准爸爸们不但要戒烟戒酒,而且也不能吃得太油腻,不然会影响到孩子们的健康,增加患病风险。

这项研究由悉尼大学的研究团队主导,他们运用创新的营养学方法体系,系统性地探索了调整父亲饮食中三大宏量营养素(蛋白质、脂肪、碳水化合物)比例,是如何影响其后代的(包括雄性后代和雌性后代)。
实验过程中,研究者将雄性小鼠分成10个组别,每组分别投喂热量相同、但宏量营养素比例各异的食物,例如蛋白质含量在10%-50%之间变动,脂肪占比10%-60%,碳水化合物占比30%-70%。在历经13周的特定饮食后,这些雄性小鼠与一直保持常规饲料饮食的雌性小鼠进行交配。而后研究人员对其雌性后代进行了全面细致的表型特征分析。
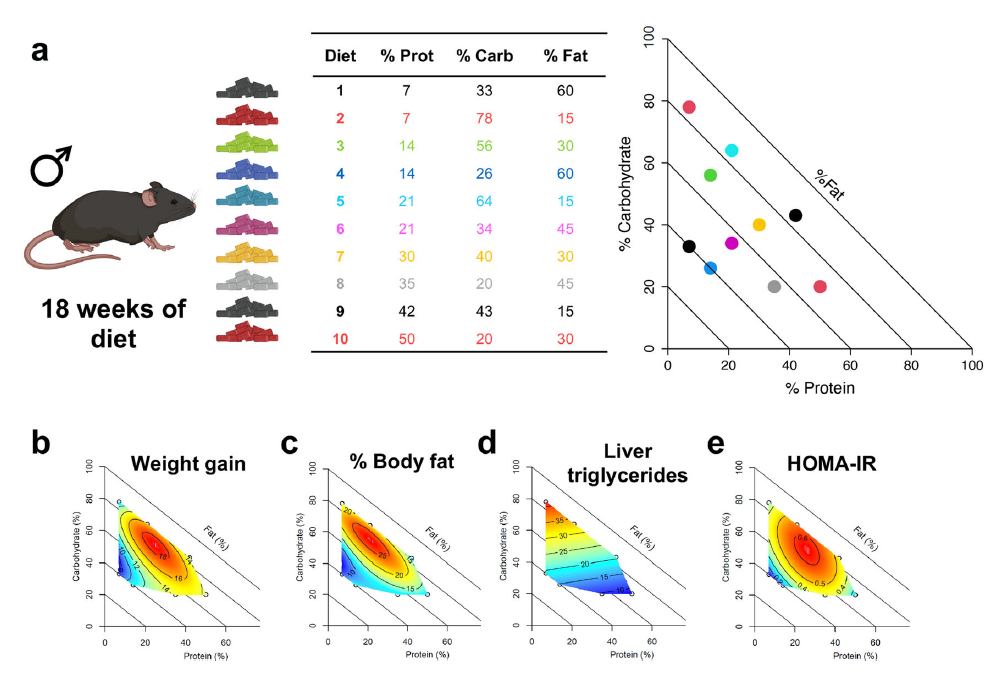 图1:父代的饮食对雌性后代的代谢表型的影响
图1:父代的饮食对雌性后代的代谢表型的影响
研究结果表明,摄取高脂肪饮食的雄性小鼠所生育的雌性后代相较于其它饮食组别的后代,通常体内脂肪含量较高。特别是在父亲饮食热量中脂肪占比达到45%、碳水化合物占比34%、蛋白质占比21%的情况下,其雌性后代表现出最高的空腹血糖水平,并积累了最大量的皮下白色脂肪。
与此形成对比的是,如果是父亲食用高蛋白、低脂的食品,那么它们的雌性后代则显示出较低的空腹血糖水平和较少的白色脂肪积累。更为关键的是棕色脂肪,其能量相对容易消耗。然而,在雌性后代体内,其存储情况却出现了相反的趋势:当它们的父亲摄入高脂肪饮食时,这些后代体内的棕色脂肪储量反而会相对较少。
这些针对代谢和身体构成的性别特异性影响并未在父代身上体现出来,这表明父代的饮食方式直接影响了子代发育过程中的内在调控机制,而非仅仅是父代自身表型特征的简单复制。研究人员推测,父亲精子中的表观遗传变化可能是导致这些父源效应的关键机制之一。
已知某些饮食宏量营养素会作用于基因组,从而引发基因表达模式的变化,并可能传递给下一代。例如,高脂肪摄入可能会诱发表观遗传修饰,使得女儿更易增加脂肪储存并出现胰岛素抵抗。

其实不只是高脂肪的饮食,父亲的高血糖一样会让后代更容易肥胖。2017年,来自重庆医科大学附属医院的研究人员在《内分泌学期刊》上发表了他们的研究。
在研究中,他们利用雄性大鼠作为实验对象,通过腹腔注射链脲佐菌素(STZ)或柠檬酸缓冲液(CB)来模拟高血糖状态。随后,选择血糖水平高于特定阈值的STZ注射大鼠与正常雌性大鼠交配,以观察其后代的代谢变化。
研究结果显示,来自高血糖父亲的后代(STZ-O)在成长过程中展现出了与正常对照组(CB-O)不同的代谢特征。成年STZ-O的体重明显高于CB-O,这说明高血糖父亲的后代可能更容易患上肥胖症。
进一步的分析发现,STZ-O在葡萄糖和胰岛素耐受性测试中的表现也较差,显示出胰岛素敏感性的降低。此外,这些大鼠在禁食后重新进食时的食物摄入量显著增加,这进一步加剧了它们的体重问题。
与刚才提到的研究相似的是,他们也发现STZ-O大鼠的棕色脂肪组织的变化,其中,UCP1水平发生了下调。UCP1是一种与产热活动相关的因子,其下调可能导致能量消耗的减少,从而增加肥胖的风险。
更让人意外的是,研究还发现STZ-O大鼠下丘脑中的瘦素信号受到抑制。瘦素是一种重要的激素,能够调节食欲和能量平衡。当瘦素信号受阻时,个体可能更容易感到饥饿,从而导致过度进食和体重增加。
研究人员相信这同样是来自表观遗传的代际传播。至于其传播机制,之前就有研究发现表观遗传变化可以通过父亲精子中的microRNA来传递。
在2015年发表在《美国科学院院刊》的一项研究中,来自宾夕法尼亚大学科学家建立了一种父代压力模型,他们发现一些特殊的microRNA(简称miRs)。当雄性小鼠受到压力时,这些miRs在它们的精子中就会增多。而且,这些增多的miRs竟然与后代的下丘脑-垂体-肾上腺(简称HPA)应激反应减弱有关。

在研究中,他们进一步检验这些精子miRs在受精后是否会影响后代的应激反应,并通过向受精卵注射这9种特定的miRs,证明了后代应激失调表型的显著再现。此外研究人员还发现,这些miRs可能会长期改变下丘脑的转录组,导致HPA轴功能出现问题。而且与血脑屏障通透性有关的细胞外基质和胶原蛋白基因的表达也下降了。
为了更深入地了解这些miRs的作用,科学家们还使用了一种新技术来观察它们在早期受精卵中的影响。结果发现这些miRs会降解一些储存的母体mRNA转录本,其中就包括与染色质重塑有关的sirtuin 1和泛素蛋白连接酶E3a基因。这种强大的调节功能可能引发了一系列的分子事件,最终改变了后代的应激反应。这说明精子中的miRs在传递父代经历给后代时起到了重要的作用。
父代的不良饮食习惯所产生的表观遗传变化也可能以类似的方式传递给后代。不过这还需要进一步的研究。由此可见,后代的肥胖与否,一定程度上也是一件拼爹的事,只有准父亲们保持健康的饮食习惯,后代才会更健康哦~
参考文献:
1. Crean, A.J., Senior, A.M., Freire, T. et al. Paternal dietary macronutrient balance and energy intake drive metabolic and behavioral differences among offspring. Nat Commun (2024). https://doi.org/10.1038/s41467-024-46782-y
2. Shi, X., Li, X., Hou, Y., Cao, X., Zhang, Y., Wang, H., Wang, H., Peng, C., Li, J., Li, Q., Wu, C., & Xiao, X. (2017). Paternal hyperglycemia in rats exacerbates the development of obesity in offspring. Journal of Endocrinology, 234(2), 175-186.
3. Rodgers AB, Morgan CP, Leu NA, Bale TL. Transgenerational epigenetic programming via sperm microRNA recapitulates effects of paternal stress. Proc Natl Acad Sci U S A. 2015 Nov 3;112(44):13699-704. doi: 10.1073/pnas.1508347112. Epub 2015 Oct 19. PMID: 26483456; PMCID: PMC4640733.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


