Trends in Immunology:沿胃肠道巨噬细胞的区域特化
来源:生物谷 2021-08-21 23:25
在各种哺乳动物组织中,组织微环境是印迹组织特异性巨噬细胞功能的主要驱动因素,当单核细胞在稳态和炎症状态下被募集到胃肠(GI)道时,它们迅速采用组织特异性和独特的转录组。本文强调了可能影响巨噬细胞功能的胃肠道差异,特别关注饮食和微生物群,这种分析可能会推动对肠道免疫系统和GI组织微环境之间相互作用的进一步研究,理想地提供独特的治疗靶点来调节特定的肠道巨噬细胞种群和/或功能。
在各种哺乳动物组织中,组织微环境是印迹组织特异性巨噬细胞功能的主要驱动因素,当单核细胞在稳态和炎症状态下被募集到胃肠(GI)道时,它们迅速采用组织特异性和独特的转录组。然而,胃肠道沿其长度变化很大,但大多数肠道巨噬细胞研究并没有直接比较这些巨噬细胞在小肠和大肠中的表型和功能,从而导致数据解释的差异。本文强调了可能影响巨噬细胞功能的胃肠道差异,特别关注饮食和微生物群,这种分析可能会推动对肠道免疫系统和GI组织微环境之间相互作用的进一步研究,理想地提供独特的治疗靶点来调节特定的肠道巨噬细胞种群和/或功能。
图片来源:https://doi.org/10.1016/j.it.2021.07.006
本文中,研究者关注不断变化的胃肠道微环境对肠道巨噬细胞特化的影响,肠道巨噬细胞代表了人体中最大的组织驻留巨噬细胞(TRM)。该领域目前的一个问题是,大多数肠道巨噬细胞研究并没有直接比较来自小肠和大肠的巨噬细胞,也很少考虑设施、不同饮食方案和肠道炎症小鼠模型之间的住房和微生物群的差异,所有这些都会影响巨噬细胞表型。考虑到这些情况可能导致SI和结肠的表型和功能差异,本文旨在通过描述不同的GI环境以及沿GI轨迹的常驻巨噬细胞和单核细胞命运来确认这种差异。
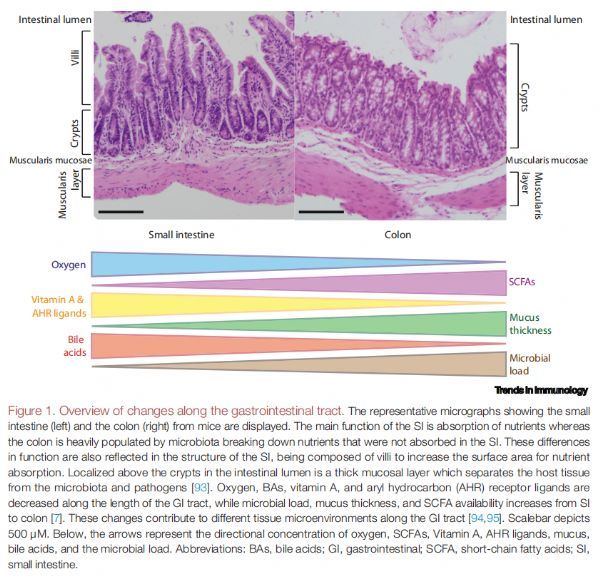
胃肠道变化的概述 图片来源:https://doi.org/10.1016/j.it.2021.07.006
沿哺乳动物胃肠道的组织微环境在小肠(SI)和结肠之间有所不同,在肠腔隐窝-腔轴上的局部组织微环境也不同,位于肠腔隐窝上方的是厚厚的粘膜层,它将宿主组织与微生物群和病原体分开。氧气、胆汁酸(BAs)、维生素A和芳烃(AHR)配体沿胃肠道长度减少,而微生物负荷、粘液厚度、pH和短链脂肪酸(SCFA)可用性从SI到结肠增加。SI对于营养吸收和食物耐受性至关重要,它还会持续接触胆汁等消化液,这会影响哺乳动物SI下部的微生物群。结肠中充满了微生物群,它们与宿主保持共生关系,并分解SI中未吸收的营养物质,结肠的另一个重要功能是水分吸收,它主要发生在结肠的近端部分。尽管胃肠道的解剖学和生理学差异已被广泛评估,但它们对宿主免疫系统的影响却未得到充分研究,例如,已知SCFA和BA可调节微生物群组成,但也会对肠道免疫系统产生明显影响。
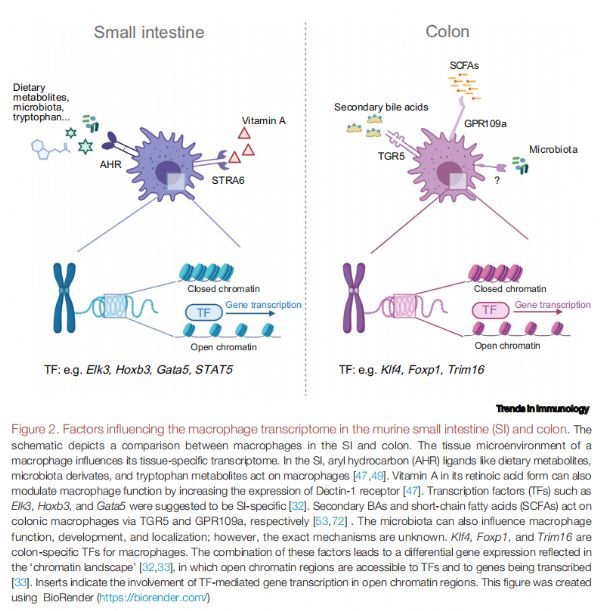
影响小鼠小肠 (SI) 和结肠中巨噬细胞转录组的因素 图片来源:https://doi.org/10.1016/j.it.2021.07.006
单核细胞在进入不同的肠道段后迅速获得组织特异性和特征性的转录组学特征,突出了比较沿胃肠道巨噬细胞功能差异的重要性,稳定状态下SI和结肠单核细胞中各种转录因子(TF)的表达不同,包括结肠巨噬细胞的Klf4、Foxp1和Trim16,以及SI巨噬细胞的Elk3、Hoxb3和Gata5。在SI中,AHR配体如膳食代谢物、微生物群衍生物和色氨酸代谢物作用于巨噬细胞,维甲酸形式的维生素A还可以通过增加树突状细胞相关性C型植物血凝素1(Dectin-1)受体的表达来调节巨噬细胞功能,次级BA和SCFA分别通过TGR5和GPR109a作用于结肠巨噬细胞。微生物群还可以影响巨噬细胞的功能、发育和定位,然而,确切的机制尚不清楚,这些因素的结合导致了“染色质景观”中反映的差异基因表达,其中开放染色质区域可用于TF和被转录的基因,插入表明TF介导的基因转录参与开放染色质区域。
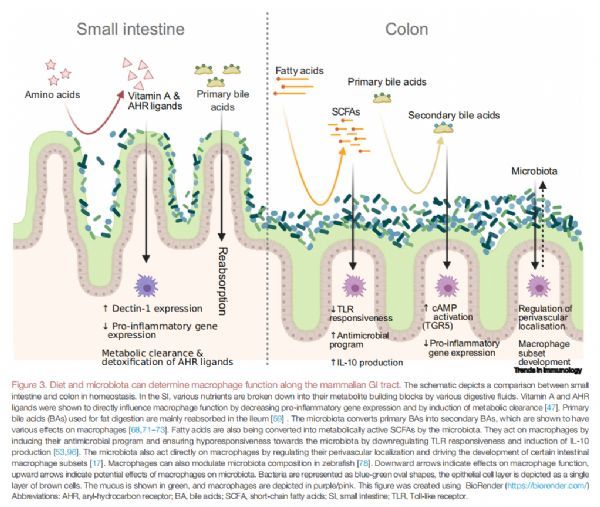
饮食和微生物群可以确定沿哺乳动物胃肠道的巨噬细胞功能 图片来源:https://doi.org/10.1016/j.it.2021.07.006
在功能上,胃肠道是营养消化的核心,部分依赖微生物群来分解哺乳动物无法获得的营养。 因此,饮食摄取的营养物质以及次级代谢物和微生物群本身可能对巨噬细胞功能产生重大影响。本文专注于描绘沿胃肠道的膳食营养素和微生物群的差异,并讨论对巨噬细胞功能的已知和可能的影响。在SI中,各种营养物质被各种消化液分解成它们的代谢物构建块,维生素A和AHR配体显示通过降低促炎基因表达和诱导代谢清除直接影响巨噬细胞功能。用于脂肪消化的BA主要在回肠中重吸收,微生物群将初级BA转化为次级BA,后者对巨噬细胞具有多种影响。脂肪酸也被微生物群转化为具有代谢活性的SCFA,它们通过诱导抗微生物程序并通过下调Toll样受体(TLR)反应性和诱导白介素10(IL-10)产生来确保对微生物群的低反应性来作用于巨噬细胞。微生物群还能通过调节巨噬细胞的血管周围定位和驱动某些肠道巨噬细胞亚群的发育直接作用于巨噬细胞。
近年来,人们越来越关注微生物组与肠道免疫系统之间的相互作用,需要在体内平衡和炎症环境中沿胃肠道中建立一个完整的微生物-饮食-宿主相互作用图,以更好地了解不同肠道疾病的病因并开始针对隔室特异性靶向。为此,沿胃肠道同时对多个微生物群亚群进行成像的技术可以为微生物群中的物理和分子相互作用以及它们与宿主免疫系统的相互作用提供新的见解。(生物谷 bioon)
参考文献
Dorothée L. Berthold et al. Regional specialization of macrophages along the gastrointestinal tract. Trends in Immunology (2021 Aug 06) doi:https://doi.org/10.1016/j.it.2021.07.006
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。