歌德-法兰克福大学:乳酸脱氢酶B对肿瘤微环境中巨噬细胞代谢的调节
来源:本站原创 2021-06-24 15:40
肿瘤微环境中的葡萄糖代谢是肿瘤生长的基本标志,对其进行干预仍然是抗肿瘤治疗的一个有吸引力的选择。肿瘤衍生因子如microRNAs(MiRs)是否调节基质细胞,特别是肿瘤相关巨噬细胞(TAMs)的葡萄糖代谢,以劫持它们以获得营养支持,目前仍不清楚。作者的发现证实了LDHB在巨噬细胞中的重要作用,并建立了肿瘤来源的miR-375作为乳腺癌巨噬细胞代谢的一种新的调
肿瘤微环境中的葡萄糖代谢是肿瘤生长的基本标志,对其进行干预仍然是抗肿瘤治疗的一个有吸引力的选择。肿瘤衍生因子如microRNAs(MiRs)是否调节基质细胞,特别是肿瘤相关巨噬细胞(TAMs)的葡萄糖代谢,以劫持它们以获得营养支持,目前仍不清楚。作者的发现证实了LDHB在巨噬细胞中的重要作用,并建立了肿瘤来源的miR-375作为乳腺癌巨噬细胞代谢的一种新的调节因子,这可能为肿瘤细胞/基质细胞的联合干预策略铺平道路。
图片来源: https://doi.org/10.7150/thno.58380
除了谷氨酰胺的消耗外,葡萄糖的有氧代谢对肿瘤生长的能量利用也是非常重要的。尽管实体肿瘤的营养和氧气梯度很大,但癌细胞喜欢有氧糖酵解,这会导致乳酸的产生,尽管在ATP合成方面效率较低。我们有理由认为癌细胞可能会利用基质细胞来满足其新陈代谢的需要。已有研究表明,肿瘤相关成纤维细胞一旦通过与肿瘤细胞的直接接触而被激活,就在肿瘤微环境(TME)中起到乳酸供体的作用。其他间质细胞,如肿瘤相关巨噬细胞(TAM),占肿瘤总质量的50%,是否也在TME中发挥乳酸供体的作用尚不清楚。然而,肿瘤来源的乳酸被巨噬细胞摄取,从而增加了原肿瘤表型转移,目前尚不清楚肿瘤细胞是否以及如何劫持TAMs的葡萄糖代谢机制,将其重新编程为乳酸生成者。
TAMs是一种动态和异质的免疫细胞群,与支持肿瘤进展、侵袭和转移的免疫抑制和营养功能有关。因此,大量浸润的TAM通常与较差的疾病结局相关。肿瘤微环境信号包括肿瘤细胞代谢改变的产物,TAMs调整它们的新陈代谢,这与它们的亲(M1样)或抗炎(M2样)极化密切相关。了解调控这些代谢变化的TME和TAMS之间的复杂关系是迈向TAM导向的抗肿瘤治疗的关键一步。
肿瘤细胞-巨噬细胞(M-Φ)相互作用的一种方式是通过microRNAs(MiR),这是一种在转录后水平减弱靶基因表达的非编码小RNA。最近,作者发现乳腺肿瘤细胞在凋亡时释放miR-375,并被M-Φ摄取,从而刺激其迁移和浸润。在这里,作者提供的证据表明,肿瘤细胞来源的miR-375下调巨噬细胞中的LDHB,这对其代谢适应成为肿瘤支持性细胞至关重要。乳酸脱氢酶(Ldh)是糖酵解过程中催化丙酮酸和乳酸双向转化的关键酶之一。四聚体酶由不同的亚基LDHA和LDHB组成。LDHA对丙酮酸有较高的亲和力,优先将丙酮酸转化为乳酸,在包括乳腺癌在内的许多恶性肿瘤中过度表达。相比之下,关于乳酸脱氢酶(LDHB)的信息非常有限,它在恶性肿瘤细胞和TAMs中将乳酸转化为丙酮酸。作者发现了LDHB在巨噬细胞中的非冗余作用,并探讨了其在乳腺癌中的病理生理相关性。作者还为miR-375-LDHB轴在临床前联合抗肿瘤治疗模型中的临床相关性提供了证据。
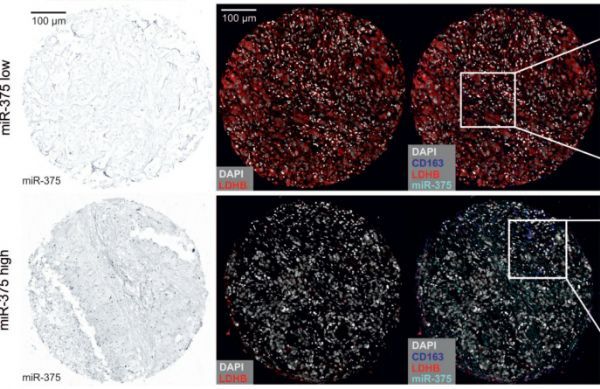
乳腺浸润性癌切片的典型图片,放大后的箭头显示miR-375与CD163和LDHB共定位
图片来源:doi: 10.7150/thno.58380
作者的研究增加了乳腺肿瘤细胞如何通过下调小鼠和人乳腺癌组织中的LDHB来改变TAMS代谢以满足营养需要和动态平衡的分子机制。由于低密度血红蛋白在M-Φ中的功能影响尚不清楚,作者预计miR-375下调低密度血红蛋白以及随后的泌乳作用可能不仅对TAMs有影响,而且对肿瘤细胞也有影响。实时代谢通量分析和糖酵解酶的转录分析显示,通过miR-375抑制LDHB可以增加肿瘤细胞和TAMs的有氧糖酵解,而不改变OCR。这似乎很有趣,因为ECAR是糖酵解的综合指标,TCA循环和乳酸已被证明是TCA循环的主要能量来源。作者观察到,由于miR-375的积聚,TAMS的细胞内和细胞外乳酸增加,并伴随着MCT4的表达增强。MCT1和MCT4在乳腺癌中均上调。MCT1是乳酸输入所必需的,而MCT4是由高乳酸和氧化应激诱导的,以促进乳酸分泌和增加糖酵解通量。有研究表明,有氧糖酵解由TAMs增强提供了对乳腺癌细胞的凋亡抗性。此外,由于启动子超甲基化导致的低密度脂蛋白血红蛋白(LDHB)抑制已经被证明可以诱导胰腺癌的糖酵解转变。LDHB在三阴性乳腺癌细胞中上调,其基因敲除降低了细胞增殖。与LDHA不同的是,LDHB在MCF-7等乳腺癌细胞中的表达微乎其微,而且它的基因敲除对细胞增殖没有重大影响。事实上,据报道,mcf-7大约80%的能量是通过线粒体呼吸产生的。不同类型乳腺癌利用葡萄糖的差异和LDHB的差异表达使其成为抗肿瘤治疗的一个有吸引力的靶点。(生物谷 Bioon.com)
参考资料
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。